
�����������ʾ��ȷ����
| A��0.1 mol��L-1�Ĵ����pH��a��0.01 mol��L-1�Ĵ����pH��b����a��1=b |
| B��������0.1 mol��L-1�Ĵ�����Һ���Ũ�ȵ����NaOH��Һ��Ӧ�����Һ�У�c(CH3COOH)+c(CH3COO��)="0.1" mol��L-1 |
| C�����ܵ����AB2�ı�����Һ�У�c(A2+)=xmol��L-1, c(B-)="y" mol��L-1����KspֵΪ4xy2 |
| D����200mL4 mol��L-1��NaOH��Һ��0.6mol CO2��ȫ���գ���Ӧ�����ӷ���ʽΪ:3CO2+4OH��=CO32��+2HCO3��+H2O |
D
�������������A��Ũ�Ȳ�ͬ�Ĵ������̶Ȳ�ͬ����Ũ��ԽС����̶�Խ��a+1>b��B��0.1 mol��L-1�Ĵ�����Һ���Ũ�ȵ����NaOH��Һ��Ӧ��ô�������Һ�����������غ�ɵô�������Ӻʹ�����ӵ�Ũ��֮�͵��������ӵ�Ũ�ȣ�Ϊ0.05 mol��L-1����B������Ksp�ı���ʽ��֪��ӦΪxy2����C�������������ƺͶ�����̼�����ʵ����ֱ�Ϊ0.8mol��0.6mol�����ݻ�ѧ����ʽ����ɵ�����̼���ƺ�̼�����Ƶ����ʵ����ֱ�Ϊ0.2mol��0.4mol���������жϳ�����ʽ�е�ϵ����д�����ӷ���ʽ����D��ȷ��
���㣺����������ʵĵ��롢�����غ��Ӧ�á������ܽ�ƽ�ⳣ���ı���ʽ����������д��ѧ����ʽ��֪ʶ��


 ���ʿ��ÿ��ֳɳ�ϵ�д�
���ʿ��ÿ��ֳɳ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����������̼ͨ��NaCN��Һ�У��������·�Ӧ��CO2 + H2O + CN- =HCO3- + HCN������˵����ȷ���ǣ��¶Ⱦ�Ϊ25�棩
| A�����볣����K(HCN) ��Ka2 (H2CO3) |
| B��Ũ�Ⱦ�Ϊ0.1mol��L-1��NaCN��NaHCO3��Һ��pH��NaCN ��NaHCO3 |
| C��Ũ�Ⱦ�Ϊ0.1mol��L-1��NaCN��Na2CO3��Һ�У���������Ũ����� |
| D��pH��Ϊ10�� Na2CO3��Һ��NaCN��Һ�У�ˮ���������c��OH-����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��AgCl��AgBr�ı�����Һ�������ϣ��ټ�������ŨAgNO3��Һ�������ķ�ӦΪ(����)
| A��ֻ��AgBr�������� |
| B��AgCl��AgBr������������ |
| C��AgCl��AgBr�������У�����AgCl����Ϊ�� |
| D��AgCl��AgBr�������У�����AgBr����Ϊ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪0.1 mol��L-1�Ķ�Ԫ��H2A��Һ��pH=4,������˵������ȷ����(����)
A.��Na2A��NaHA����Һ��,���������ͬ
B.���������ʵ�����ȵ�Na2A��NaHA����Һ��,�������������
C.��NaHA��Һ��һ����:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.��Na2A��Һ��һ����:c(Na+)>c(A2-)>c(H+)>c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������,��0.1 mol��L-1����������Һ��0.06 mol��L-1������Һ��������,�û����Һ��pH����(����)
| A��1.7 | B��2.0 | C��12.0 | D��12.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪CuSO4��Һ�ֱ���Na2CO3��Һ��Na2S��Һ�ķ�Ӧ������£�
(1)CuSO4��Na2CO3
��Ҫ��Cu2����CO32-��H2O=Cu(OH)2����CO2��
��Ҫ��Cu2����CO32-=CuCO3��(������������Ӧ����ͬ)
(2)CuSO4��Na2S
��Ҫ��Cu2����S2��=CuS��
��Ҫ��Cu2����S2����2H2O=Cu(OH)2����H2S��
�����м������ʵ��ܽ�ȴ�С�ıȽ��У���ȷ���ǣ� ��
| A��CuS��Cu(OH)2��CuCO3 |
| B��CuS��Cu(OH)2��CuCO3 |
| C��Cu(OH)2��CuCO3��CuS |
| D��Cu(OH)2��CuCO3��CuS |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£���1.000 mol��L��1�������20.00 mL 1.000 mol��L��1��ˮ�У���ҺpH���¶��������������仯������ͼ��ʾ�������й�˵����ȷ���ǣ� ��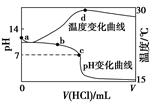
| A��a����ˮ�������c(H��)��1��10��14 mol/L |
| B��b�㣺c(NH4+)��c(NH3��H2O)��c(Cl��) |
| C��c�㣺c(Cl��)��c(NH4+) |
| D��d�����Һ�¶����½�����Ҫԭ����NH3��H2O�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£�ˮ�ĵ���ﵽƽ�⣺H2O H����OH��������������ȷ���ǣ� ��
H����OH��������������ȷ���ǣ� ��
| A����ˮ���ȣ�ƽ�������ƶ���KW��С |
| B����ˮ�м�������NaOH���壬ƽ�������ƶ���c(OH��)���� |
| C��������ˮ���ú�ˮ�ĵ���ƽ�������ƶ���c(OH��)���� |
| D����ˮ�м�������CH3COONa���壬ƽ�������ƶ���KW���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����pH��5��CH3COOH��Һ10 mL��Ҫʹ��pH����3���ɲ�ȡ�ķ����У� ��
| A������Һ�м�ˮϡ����10 L |
| B������һ������NaOH���� |
| C������һ����pH��8��NaOH��Һ |
| D������һ��Ũ�ȵ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com