
��1�֣���֪NaOH��NaHCO3������Ӧ�ķ���ʽΪ��
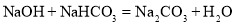
��ʵ�������������ƹ�������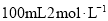 ��NaOH��Һ���ش��������⣺
��NaOH��Һ���ش��������⣺
��1�����в�����˳���ǣ�ÿ����ѡһ�Σ�_____________��
A������
B���ܽ�
C��ϴ��
D������
E��ת��
F��ҡ��
G����ȴ
��2��������ƿ������������ˮ��������Һ��Ũ�Ƚ�_____________�����ƫ����ƫС������Ӱ�족��
��3���ڶ��ݲ���ʱ����������ƿ�̶��ߣ���������Һ��Ũ�Ƚ�_____________���ƫ����ƫС������Ӱ�족����
���� ��Һ�м���һ�����ij���������X��ǡ��ʹ��ת��Ϊֻ��Na2CO3���ʵ���Һ��ʵ��ת�������X�ж��֣���ش��������⣺
��Һ�м���һ�����ij���������X��ǡ��ʹ��ת��Ϊֻ��Na2CO3���ʵ���Һ��ʵ��ת�������X�ж��֣���ش��������⣺
��1������д�±��հס�
��� | �� | �� | �� | �� |
X�Ļ�ѧʽ | NaOH | Na2O2 | ||
����X��������g�� | 9.2 | 15.6 |
��2����Ӧ����Һ�е�Na�������ʵ�����Ϊ_____________mol��
��3���ڢ�~���У�����Na2CO3���ʵ�����������ȵ���_____________�����ţ���
��1��A��B��G��E��C��D��F��1�֣�
��2����Ӱ�죨1�֣�����3��ƫ��1�֣�
��1����ÿ��1�֣���4�֣�
��� | �� | �� | �� | �� |
X�Ļ�ѧʽ | Na | Na2O | ||
����X��������g�� | 1.6 | 12.4 |
��2��0.8��2�֣� ��3���ۺ͢ܣ�1�֣�
��������
�����������1��������Һ��˳��Ϊ�������ܽ⣬��ȴ��ת�ƣ�ϴ�ӣ����ݣ�ҡ�ȣ�����˳��Ϊ��A��B��G��E��C��D��F����2������ƿ����ˮ����ʵ��û��Ӱ�죻��3������ʱ��Һ�����ƫС��������Һ��Ũ��ƫ��1��̼�����Ƶ����ʵ���Ϊ2.0��0.2=0.4Ħ������������Xǡ��ת��Ϊֻ����̼�������ʵ���Һ����ӵ�������ֻ�����ƻ��������ƻ������ƻ�������ƣ�ʵ�ʷ�Ӧ��ʵ��Ϊ̼�����ƺ��������Ʒ�Ӧ����Ҫ0.4Ħ���������ơ���������0.4Ħ������������Ҫ��0.4Ħ������0.4��23=9.2�ˣ���Ҫ��������0.4��40=1.6�ˣ���Ҫ��������0.2Ħ������0.2��78=15.6�ˣ���Ҫ0.2Ħ�������ƣ���0.2��62=12.4�ˡ��������Ϊ��
��� | �� | �� | �� | �� |
X�Ļ�ѧʽ | Na | Na2O | ||
����X��������g�� | 1.6 | 12.4 |
��2��0.4Ħ��̼�����Ʒ�Ӧ������0.4Ħ��̼���ƣ�������Һ�����������ʵ���Ϊ0.8Ħ������3��0.4Ħ���ƻ�ʹ��Һ��������Ϊ9.2-0.4=8.8�ˣ������������Ƶ���������Ϊ16.0�ˣ��������������������Ϊ15.6-3.2=12.4�ˣ����������Ƶ���������Ϊ12.4�ˣ����Լ���������ƺͼ��������ƺ���Һ������ȣ�����̼���Ƶ�����������ȣ�ѡ�ۺ͢ܡ�
���㣺��Һ�����ƣ��ƵĻ���������ʺ��ת����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
25 ��ʱ���ڵ������ �� pH=0��H2SO4��Һ����0.05 mol/L��Ba(OH)2��Һ����pH=10��Na2S��Һ����pH=5��NH4NO3��Һ�У����������ˮ�����ʵ���֮����
A��1:10:10 :10
:10 B��1:5:5��10
B��1:5:5��10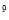 :5��10
:5��10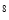
C��1:20:10 :10
:10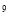 D��1:10:10
D��1:10:10 :10
:10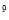
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ĵ�ʡ��֦���и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ֻ�ı������е�һ����������ʹN2(g)��3H2(g) 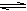 2NH3(g) ��H��0ƽ�����淴Ӧ�����ƶ�����
2NH3(g) ��H��0ƽ�����淴Ӧ�����ƶ�����
A�������¶� B������ѹǿ C������H2��Ũ�� D��ʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ĵ�ʡ��ɽ�и�һ�꼶��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�������һ���ܴ����������
A����ɫ��Һ�У�Na+��Cu2+��NO3-��Cl-
B����pH=8����Һ�У�Na+��K+��AlO2-��Cl-
C���ں�����Fe3������Һ�У�NH4+��Na+��Cl����SCN��
D����Al��Ӧ�����������Һ��Na+��K+��CO32-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ĵ�ʡ��ɽ�и�һ�꼶��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������ֵ������˵������ȷ����
A��1 mol N2�����е�ԭ����ΪNA
B��1 mol��L��1 NaCl��Һ�к��е���������ĿΪNA
C����״���£�22.4 LCO������ԭ����ΪNA
D��24 g O2��24 g O3��������ԭ��������1.5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
˫�ǻ���̼������ҽ���ϳ��õ�һ����������仯ѧʽΪ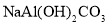 �����ڸ����ʵ�˵����ȷ����
�����ڸ����ʵ�˵����ȷ����
A������������������������
B����������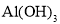 ��
��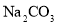 �Ļ����
�Ļ����
C��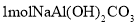 ����������4mol
����������4mol 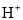
D����ҩ�����ʺ���θ������θ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ʵ�����˵����ȷ����
A���÷�Һ©���������ͺ�ֲ����
B�����Թ��еμ�Һ��ʱ����ͷ�ιܽ����Թ��ڱ�
C�������Թ�������ʱ���Թܵײ���ƾ��Ƶ�о�Ӵ�
D������ʱ��©���¶˽����ձ��ڱ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ��װ��ͼ��������
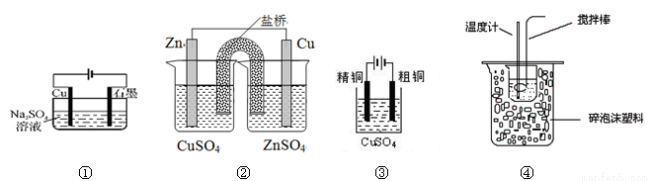
A��װ�â���ʾװ�ÿ�ʵ�ַ�Ӧ��Cu+2H2O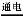 Cu(OH)2+H2��
Cu(OH)2+H2��
B��װ�â��ܹ���пͭԭ���
C��װ�âۿ����ڴ�ͭ�ĵ�⾫��
D��װ�âܿ�������ʵ���Ҳⶨ�кͷ�Ӧ�ķ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��Ǩ�и߶���ѧ��ѧҵˮƽģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����Ƭ��̼������ͼ��ʾ��ʽ��������ͭ��Һ�У�������ָ�뷢��ƫת��������Ը�װ�D��˵������ȷ����
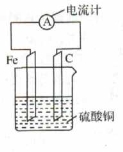
A��̼��������
B����װ���ܽ�����ת��Ϊ��ѧ��
C�����·�е�������Ƭ������������������̼��
D����װ�õ��ܷ�ӦΪ��2Fe+3Cu2+=2Fe3++3Cu
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com