
【题目】新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下,则下列判断正确的是( )
![]()
A.MFe2Ox是氧化剂
B.SO2是该反应的催化剂
C.x<y
D.MFe2Oy是还原产物
【答案】C
【解析】
A.SO2转化为S,S元素化合价降低,说明SO2在反应中为氧化剂,则MFe2Ox为还原剂,故A错误;
B.SO2在反应中转化为S为氧化剂,不是催化剂,故B错误;
C.MFe2Ox为还原剂生成MFe2Oy,反应后Fe元素的化合价升高,根据化合价代数和,则有(2y-2)>(2x-2),即x<y,故C正确;
D.SO2转化为S,S元素化合价降低,说明SO2在反应中为氧化剂,则MFe2Ox为还原剂,所以MFe2Oy是氧化产物,故D错误;
故选C。
【点晴】
本题主要考查学生根据题目所给的信息和所学的化学知识进行解题的能力,解答时注意根据化合价的变化和化合物化合价代数和为0分析解答问题,要细心分析。在反应中,SO2转化为S,S元素化合价降低,说明SO2在反应中为氧化剂,则MFe2Ox为还原剂,反应后Fe元素的化合价升高,根据Fe元素常见化合价为+2、+3价判断x、y大小关系。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧。反应的化学方程式为:2FeSO4·7H2O![]() Fe2O3+ SO2↑+ SO3↑+ 14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管。下列关于该反应说法正确的是
Fe2O3+ SO2↑+ SO3↑+ 14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管。下列关于该反应说法正确的是
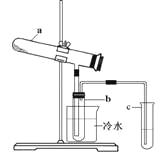
A.若将反应后的三种气体通入BaCl2溶液中,产生的沉淀为BaSO3、BaSO4
B.b中产物用紫色石蕊试液即可检验出其中H+和SO42—
C.为检验反应的另一种生成物,试管c中应加入的试剂为NaOH溶液
D.b中所得到的硫酸的质量分数为29.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯苯在染料、医药工业中用于制造苯酚、硝基氯苯、苯胺、硝基酚等有机中间体。实验室中制备氯苯的装置如图所示(夹持仪器已略去)。请回答下列问题:
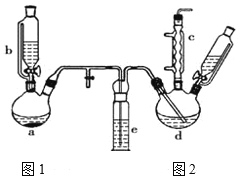
(1)仪器a中盛有KMnO4晶体,仪器b中盛有浓盐酸。打开仪器a中的活塞,使浓盐酸缓缓滴下,仪器中产生黄绿色气体,用离子方程式表示产生该现象的原因:____。
(2)仪器b中细玻璃导管的作用是_____。
(3)仪器d内盛有苯、FeCl3粉末,仪器a中生成的气体经过仪器e进入到仪器d中。
①仪器e的名称是洗气瓶,内盛装的试剂是____;
②仪器d中的反应进行过程中,保持温度在40-60℃,以减少副反应发生。仪器d的加热方式最好采用___加热。
(4)仪器c的作用是___;d中发生的化学反应方程式是____。
(5)该方法制备的氯苯中含有很多杂质,工业生产中通过水洗,然后通过碱洗,再水洗,最后通过分液得到含氯苯的有机物的混合物,混合物成分及沸点如图2表格所示:
有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
沸点/℃ | 80 | 132.2 | 180.4 | 173.0 | 174.1 |
①碱洗前先进行水洗的目的是____;
②取该有机物的混合物中的氯苯时,采用蒸馏的方法,收集___℃左右的馏分。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3,4―二羟基肉桂酸乙酯(I)具有抗炎作用和治疗自身免疫性疾病的潜力。由化合物A制备该物质的合成路线如图:
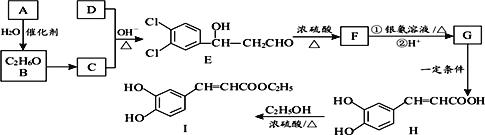
已知:R—CHO+R’—CH2—CHO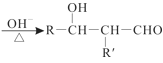
回答下列问题:
(1)A的结构简式为___,I中含氧官能团的名称是___。
(2)E生成F的反应类型为___。
(3)下列有关H的说法中,不正确的是___。
a.能使酸性高锰酸钾溶液褪色
b.1molH最多能和3molBr2反应
c.H分子中最多有9个碳原子共平面
d.1molH分别与足量NaOH、NaHCO3反应时,消耗的NaOH、NaHCO3的物质的量之比为1:1
(4)写出C+D→E的化学方程式___。
(5)已知W是H的同分异构体,符合下列条件的W结构共有___种。
①属于芳香族化合物。
②1molW与足量NaHCO3溶液反应生成气体44.8L(标准状况)。
其中,核磁共振氢谱有4组吸收峰,且峰面积比为1∶2∶2∶3的结构简式为:___(写一个即可)
(6)季戊四醇(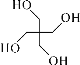 )是合成高效润滑剂、增塑剂、表面活性剂等的原料。设计由甲醛和乙醇为原料制备季戊四醇的合成路线(无机试剂任选)。合成路线的表示方法为:___。
)是合成高效润滑剂、增塑剂、表面活性剂等的原料。设计由甲醛和乙醇为原料制备季戊四醇的合成路线(无机试剂任选)。合成路线的表示方法为:___。
A![]() B……
B……![]() 目标产物。
目标产物。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究H2O2分解的速率及影响因素,在相同温度下按照下表所示的方案完成实验。

(1)上述实验方案中,探究的变量因素只有催化剂的实验组合是_____和_____。
(2)实验④过程中氧气的生成速率和时间的趋势关系如图所示,判断该反应是反应(填“放热”或“吸热”)______。
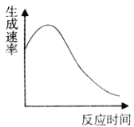
(3)实验⑤:在试管中加入10mL 0.4mol/L H2O2溶液,加入固体催化剂,在一定温度下测得不同时刻生成O2的体积(以折算为标准状况)如下表所示(假设反应过程溶液的体积保持不变):
![]()
①反应6min,H2O2分解了_______%。
②0至6min,以H2O2的浓度变化表示的反应速率为υ(H2O2)=________molL-1min-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行实验,下列对实验现象的解释不合理的是

选项 | ①试剂 | ①中现象 | 解释 |
A | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
B | Na2SiO3溶液 | 产生胶状沉淀 | 酸性: H2SO3 >H2SiO3 |
C | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
D | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成 白色BaSO3沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液,所得滴定曲线如图所示(忽略混合时溶液体积的变化)。下列叙述不正确的是( )
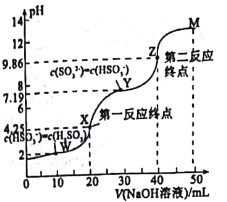
A.Ka2(H2SO3)的数量级为10-8
B.向X点加入少量澄清石灰水溶液,![]() 的值增大
的值增大
C.若将n(NaHSO3)与n(Na2SO3)=1:1混合,对应的点应在Y、Z之间
D.图中溶液中水的电离程度:W<X<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化合物2—苯基丙烯(![]() ),下列说法正确的是
),下列说法正确的是
A.不能使稀酸性高锰酸钾溶液褪色B.与甲苯互为同系物
C.最多能与4molBr2发生加成反应D.与![]() 互为同分异构体
互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积固定的密闭容器中发生反应:C(s)+H2O(g) ![]() CO(g)+H2(g),下列说法中,不能说明反应达到化学平衡状态的是
CO(g)+H2(g),下列说法中,不能说明反应达到化学平衡状态的是
A. 容器内CO的物质的量分数保持不变B. 容器内体系的压强保持不变
C. 容器内气体的密度保持不变D. 单位时间内消耗1molH2O(g),同时生成1molCO(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com