
Fe、C、N、O、H可以组成多种物质。回答以下问题:
(1)基态铁原子中,未成对电子数有 个。
(2)铁单质在一定条件下可与CO反应生成配位化合物——羰基
铁[Fe(CO)5],其结构如右图。已知CO分子与N2分子结构相
似,分子中C、O原子均能提供孤电子对形成配位键。
①CO分子中σ键与π键数目之比为 ;
②从电负性角度分析,Fe(CO)5中与Fe形成配位键的是 (填“碳”或“氧”)原子。
 ③与羰基铁分子的极性相似的分子是 。
③与羰基铁分子的极性相似的分子是 。
A.SO2 B.CS2 C.BF3 D.PCl3
(3)CH4、H2O分子的键角分别为a、b。则a b
(填>、=或<),原因是 。
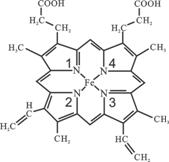
(4)血红素分子结构如右图所示。
①血红素分子间存在的作用力有 (填名称);
②与Fe通过配位键结合的氮原子的编号是 。
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是( )
A.电流从左侧电极经过负载后流向右侧电极
B.负极发生的电极反应式为N2H4+4OH--4e-===N2+4H2O
C.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D.该燃料电池持续放电时,K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关碱金属的说法正确的是
A、碱金属元素随原子序数的递增原子半径逐渐减小
B、碱金属元素随原子序数的递增离子氧化性逐渐减弱
C、碱金属元素的单质在氧气点燃都生成过氧化物
D、碱金属元素随原子序数的递增最高价氧化物对应的水化物碱性逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布为msnmpn;
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+的核外电子排布式是____________________。
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的________形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是________。
a.稳定性:甲>乙,沸点:甲>乙
b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙
d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小至大的顺序为________(用元素符号作答)。
(5)Q的一种氢化物相对分子质量为26,其分子中σ键与π键的键数之比为________。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于________(填晶体类型)。
查看答案和解析>>
科目:高中化学 来源: 题型:
向H2O2溶液中加入适量稀硫酸酸化的硫酸亚铁溶液,依次观察到如下现象:①反应刚开始,仅有少量气泡产生;②反应片刻后,有大量气泡产生;③试管底部最终出现红褐色沉淀。下列判断正确的是
A.①中仅发生一个反应 B.Fe3+能催化H2O2的分解
C.反应过程中溶液pH不断减小 D.FeSO4与等物质的量的H2O2恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |

(1)表中元素,化学性质最不活泼的是________,只有负价而无正价的是________,氧化性最强的单质是________, 还原性最强的单质是________;
还原性最强的单质是________;
(2)最高价氧化物的水化物中碱性最强的是________,酸性最强的是________,呈两性的是________。
(3)A与H形成________化合物(填“离子”或“共价”),用电子式表示它的形成过程________________________________________;B与G形成________化合物(填“离子”或“共价”),用电子式表示它的形成过程_______________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表中同周期或同主族元素,随着原子序数的递增,下列说法正确的是
A.ⅦA族元素的氢化物沸点逐渐升高
B.ⅥA族元素的原子核外最外层电子数逐渐增多
C.碱金属元素的最高价氧化物的水化物的碱性逐渐增强
D.第二周期元素(除稀有气体元素)的最高化合价数值逐渐增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com