
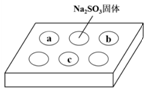
 ijͬѧ����SO2������ʵ�飮�ڵ�ΰ�a��b��c���ֱ���в�ͬ���Լ�������Na2S
ijͬѧ����SO2������ʵ�飮�ڵ�ΰ�a��b��c���ֱ���в�ͬ���Լ�������Na2S| ��� | �Լ� | ʵ������ |
| a | Ʒ����Һ | ��ɫ��ȥ |
| b | ����KMnO4��Һ | ��ɫ��ȥ |
| c | NaOH��Һ����2�η�̪�� | ��ɫ��ȥ |
| A�� | Ũ������Na2SO3���巢����������ԭ��Ӧ | |
| B�� | a��b������SO2����Ư���� | |
| C�� | c��ֻ���ܷ�����Ӧ��SO2+2OH-�TSO32-+H2O | |
| D�� | c��������Һ������Ũ��һ�����ڹ�ϵ��c��Na+��+c��H+��=2c��SO32-��+c��HSO3-��+c��OH-�� |
���� A��Ũ������Na2SO3���巢�����������ƺͶ�������
B�������������������Ƿ���������ԭ����ɫ������������Ʒ���Ƕ��������Ư���ԣ�
C��Ҳ�����Ƕ��������Ư���ԣ�
D�����ݵ���غ�������
��� �⣺A��Ũ������Na2SO3���巢�����������ƺͶ��������Ƿ�������ԭ��Ӧ����A����
B�������������������Ƿ���������ԭ����ɫ������������Ʒ���Ƕ��������Ư���ԣ�����a��Ư���ԡ�b�ǻ�ԭ�ԣ���B����
C��Ҳ�����Ƕ��������Ư���ԣ�����c�к�ɫ��ȥ��ԭ�������������кͣ�Ҳ�����Ƕ��������Ư���ԣ���C����
D�����ݵ���غ㣬c��������Һ������Ũ��һ�����ڹ�ϵ��c��Na+��+c��H+��=2c��SO32-��+c��HSO3-��+c��OH-������D��ȷ��
��ѡD��
���� ���⿼�������������ʣ���Ŀ�ѶȲ������״���ΪC�ע���̪��ɫ��ԭ����������к�Ҳ�����Ƕ��������Ư���ԣ�


 ����ѧ���ʱѧ����ϵ�д�
����ѧ���ʱѧ����ϵ�д� �ʰ�Ӣ��ͬ����ϰ��ϵ�д�
�ʰ�Ӣ��ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 700 | 800 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.7 | 1.1 | K | 0.6 | 0.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | pH=4 ʱ������ĵ��볣��Ka��1.8��10-5 | |
| B�� | B��ʱ��c��CH3COO����=c��CH3COOH�� | |
| C�� | B��ʱ������Һ�е����̪�Լ�����Һ�Ժ�ɫ | |
| D�� | C��ʱ��c��CH3COO������c��Na+����c��H+����c��OH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
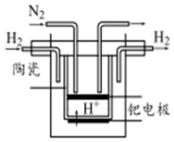 ���Ĺ̶��Թ�ũҵ��������������ش����壮
���Ĺ̶��Թ�ũҵ��������������ش����壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ���� | B�� | ������� | C�� | �ȼҵ | D�� | ��ˮɹ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������Ҵ���Ϊͬ���칹�� | |
| B�� | CH3OCH3��ֻ���м��Թ��ۼ� | |
| C�� | CH3OH���Ҵ����ɷ�����ȥ��Ӧ | |
| D�� | ˮú���ϳɶ����ѵ��Ȼ�ѧ����ʽ��3H2��g��+3CO��g���TCH3OCH3 ��g��+CO2��g����H=-248.4kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ƿ | B�� | ��Ͳ | C�� | ��ʽ�ζ��� | D�� | ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��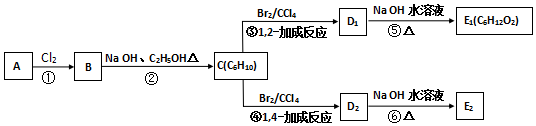
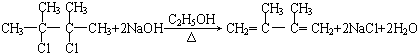 ��C�Ļ�ѧ����Ϊ2��3-����-1��3-����ϩ��E2�Ľṹ��ʽ��
��C�Ļ�ѧ����Ϊ2��3-����-1��3-����ϩ��E2�Ľṹ��ʽ�� ���ڵķ�Ӧ��������ȥ��Ӧ��
���ڵķ�Ӧ��������ȥ��Ӧ�� +2NaOH$��_{��}^{H_{2}O}$
+2NaOH$��_{��}^{H_{2}O}$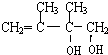 +2NaBr��
+2NaBr���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2S��HCl | B�� | Na2CO3��H2SO4 | C�� | NaHCO3��HCl | D�� | Na2SO3�� H2SO4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com