
| A. | a点:c(Cl-)>c(NH3•H2O)>c(NH4+) | B. | b点:c(OH-)=c(H+)+c(CH3COOH) | ||
| C. | c点:c(NH4+)=c(CH3COO-) | D. | d点:c(NH4+)>c(Cl-)>c(H+) |
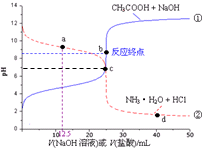
分析 A.a点盐酸的物质的量是氨水的一半,溶液中溶质为等物质的量浓度的氨水和NH4Cl,溶液呈碱性,说明一水合氨电离程度大于NH4+水解程度,结合物料守恒判断;
B.b点醋酸和NaOH的物质的量相等,二者恰好反应生成醋酸钠,溶液中存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断;
C.c点溶液呈中性,则溶液中存在c(OH-)=c(H+),结合电荷守恒得c(NH4+)=c(Cl-)、c(Na+)=c(CH3COO-),且n(NaOH)=n(HCl);
D.d点溶液中溶质为氯化铵和HCl,且盐酸和氯化铵的物质的量之比为3:5,铵根离子水解但程度较小,结合物料守恒判断.
解答 解:A.a点盐酸的物质的量是氨水的一半,溶液中溶质为等物质的量浓度的氨水和NH4Cl,溶液呈碱性,说明一水合氨电离程度大于NH4+水解程度,结合物料守恒得离子浓度大小顺序是c(NH4+)>c(Cl-)>c(NH3•H2O),故A错误;
B.b点醋酸和NaOH的物质的量相等,二者恰好反应生成醋酸钠,溶液中存在电荷守恒和物料守恒,根据电荷守恒得c(OH-)+c(Na+)=c(CH3COO-)+c(H+),根据物料守恒得c(Na+)=c(CH3COO-)+c(CH3COOH)
,所以得c(OH-)=c(H+)+c(CH3COOH),故B正确;
C.c点溶液呈中性,则溶液中存在c(OH-)=c(H+),结合电荷守恒得c(NH4+)=c(Cl-)、c(Na+)=c(CH3COO-),且n(NaOH)=n(HCl),所以得:c(NH4+)=c(CH3COO-),故C正确;
D.d点溶液中溶质为氯化铵和HCl,且盐酸和氯化铵的物质的量之比为3:5,铵根离子水解但程度较小,结合物料守恒得c(Cl-)>c(NH4+)>c(H+),故D错误;
故选AD.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断能力,明确对应点溶液中溶质成分及其性质是解本题关键,注意溶液中存在的电荷守恒和物料守恒,题目难度中等.


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子最外层比次外层多3个电子;Y、Z均为金属,Y是同周期中原子半径最大的元素,Z的简单离子半径在同周期元素中最小;W的最高价氧化物在无机含氧酸中酸性最强。下列说法正确的是
A. X的气态氢化物的热稳定性比O(氧)的强
B. 元素Z、W的简单离子具有相同的电子层结构
C. Y、Z、W的最高价氧化物对应的水化物之间能相互反应
D. 等质量的Y和Z单质分别与足量稀盐酸反应,前者产生的氢气多
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A和B可能是同分异构体 | |
| B. | A和B的最简式可能相同 | |
| C. | A和B不可能一个是烃,一个是烃的含氧衍生物 | |
| D. | 将A和B混合,当混合物质量一定时,无论A、B以何种比例混合,完全燃烧时产生的H2O的量均相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
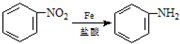
 ;
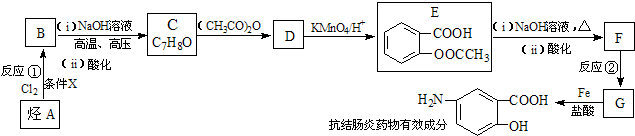
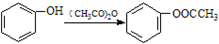
;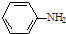 )易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸(
)易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸( 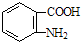 )合成路线中两种中间产物的结构简式(部分反应条件已略去)
)合成路线中两种中间产物的结构简式(部分反应条件已略去)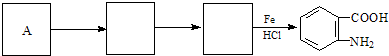
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
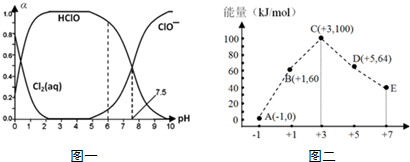
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8.15 | B. | 9.3 | C. | 10.15 | D. | 11.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
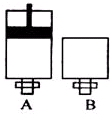
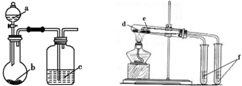 用图所示装置进行实验,能得出相应实验结论的是( )
用图所示装置进行实验,能得出相应实验结论的是( )| 选项 | 实验试剂 | 实验结论 | ||
| A | a.稀硫酸 | b.碳酸氢钠 | c.硅酸钠溶液 | 酸性:硫酸>碳酸>硅酸 |
| B | a.稀盐酸 | b.二氧化锰 | c.溴化钠溶液 | 氧化性:MnO2>Cl2>Br2 |
| C | d.小苏打 | e.苏打 | f.石灰水 | 热稳定性:苏打>小苏打 |
| D | d.氯化钠 | e.氯化铵 | f.硝酸银溶液 | 沸点:氯化钠>氯化铵 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 压减燃煤、严格控车、调整产业是治理雾霾的有效措施 | |
| B. | 铝及其合金使用广泛,是因为铝比铁更耐酸、碱的腐蚀 | |
| C. | 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 | |
| D. | 通常所说的三大合成材料是指塑料、合成橡胶和合成纤维 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com