
ĻĀĮŠŹµŃéÖŠ£¬¢ŁpHŹŌÖ½µÄŹ¹ÓĆ ¢Ś¹żĀĖ ¢ŪÕō·¢ ¢ÜÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗ£¬¾łÓƵ½µÄŅĒĘ÷ŹĒ
A. Õō·¢Ćó B. ²£Į§°ō C. ŹŌ¹Ü D. ·ÖŅŗĀ©¶·

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ±XŹĒ»īĘĆµÄ½šŹōŹ±£¬ĖüŅ»¶ØŹĒĒæ¼ī | |
| B£® | XŹĒµĆµē×ÓÄÜĮ¦ŗÜĒæµÄ·Ē½šŹōŌŖĖŲ£¬X-0-HŅ»¶ØĪŖĖį | |
| C£® | X-0-HµÄĖ®ČÜŅŗ²»Äܵ¼µē | |
| D£® | X-0-H²»æÉÄÜŹĒÖ±ĻߊĪµÄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĢģ½ņŹŠø߶žÉĻ9ŌĀµ÷ŃŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
×ī½üŅā“óĄūĀŽĀķ“óѧµÄFulvioCacaceµČČĖ»ńµĆĮĖ¼«¾ßĄķĀŪŃŠ¾æŅāŅåµÄN4·Ö×Ó”£N4·Ö×Ó½į¹¹ČēĶ¼ĖłŹ¾£¬ŅŃÖŖ¶ĻĮŃ1mol N©NĪüŹÕ167 kJČČĮæ£¬Éś³É1mol N”ŌN·Å³ö942 kJ”£øł¾ŻŅŌÉĻŠÅĻ¢ŗĶŹż¾Ż£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
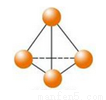
A£®N4ÓėN2»„ĪŖĶ¬·ÖŅģ¹¹Ģå
B£®1mo1N4ĘųĢå×Ŗ±äĪŖN2½«ĪüŹÕ882 kJČČĮæ
C£®N4£Øg£©ØT 2N2£Øg£© ¦¤H = - 882KJ
D£®P4£Ø°×Į×£©µÄ·Ö×Ó½į¹¹ÓėN4ĻąĖĘ£¬1mol N4ŗĶ1mol P4¾łŗ¬ÓŠ6mol·Ē¼«ŠŌ¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğÉĀĪ÷Ź”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ŹµŃéŹŅŠčŅŖ450 mL0.2 mol”¤L£1µÄĮņĖį£¬ĻÖÓĆÖŹĮæ·ÖŹżĪŖ98%”¢ĆܶČĪŖ1.84 g”¤cm£3µÄÅØĮņĖįĄ“ÅäÖĘ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ĖłŠčµÄŅĒĘ÷³żĮĖ²£Į§°ō”¢ÉÕ±”¢ĮæĶ²£¬»¹æÉÄÜÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒ£ŗ___________
(2)ÅäÖĘČÜŅŗŹ±£¬Ņ»°ćæÉŅŌ·ÖĪŖŅŌĻĀ¼øøö²½Öč£ŗ¢ŁĮæČ” ¢Ś¼ĘĖć ¢ŪČܽā ¢Üµ¹×ŖŅ”ŌČ ¢Ż×ŖŅĘ ¢ŽĻ“µÓ ¢ß¶ØČŻ ¢ąĄäČ“£¬ĘäÕżČ·µÄ²Ł×÷Ė³ŠņĪŖ__________________£®
(3)¾¼ĘĖć£¬ŠčÅØĮņĖįµÄĢå»żĪŖ £»
(4)ŌŚČŻĮæĘæµÄŹ¹ÓĆ·½·ØÖŠ£¬ĻĀĮŠ²Ł×÷²»ÕżČ·µÄŹĒ£ØĢī±ąŗÅ£©________”£
A£®ĶłČŻĮæĘæÖŠ×ŖŅĘČÜŅŗŹ±Ó¦ÓĆ²£Į§°ōŅżĮ÷ |
B£®ČŻĮæĘæÓĆÕōĮóĖ®Ļ“¾»ŗó£¬ŌŁÓĆ“żÅäČÜŅŗČóĻ“ |
C£®ÅäÖĘČÜŅŗŹ±£¬Čē¹ūŹŌŃłŹĒ¹ĢĢ壬°Ń³ĘŗƵďŌŃłÓĆÖ½ĢõŠ”ŠÄµ¹ČėČŻĮæĘæÖŠ£¬»ŗĀż¼ÓČėÕōĮóĖ®µ½½Ó½ü±źĻß2”«3cm“¦£¬ÓƵĪ¹Ü¼ÓÕōĮóĖ®µ½±źĻß |
D£®ÅäÖĘČÜŅŗŹ±£¬Čē¹ūŹŌŃłŹĒŅŗĢ壬ÓĆĮæĶ²ĮæČ”ŹŌŃłŗó£¬Ö±½ÓŃŲ²£Į§°ōŅżĮ÷ÖĮČŻĮæĘæÖŠ£¬»ŗĀż¼ÓČėÕōĮóĖ®µ½±źĻß |
E£®øĒŗĆĘæČū£¬ÓĆŹ³Öø¶„×”ĘæČū£¬ÓĆĮķŅ»Ö»ŹÖµÄŹÖÖøĶŠ×”Ęæµ×£¬°ŃČŻĮæĘæ·“ø“µ¹×Ŗ¶ą“Ī
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğÉĀĪ÷Ź”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Óė3.2 g SO2 Ėłŗ¬µÄŃõŌ×ÓŹżĻąµČµÄNO2µÄÖŹĮæĪŖ
A£®2.3 g B£®3.2 g C£®4.6 g D£®6.4 g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğÉĀĪ÷Ź”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®H2SO4ŗĶH3PO4µÄĦ¶ūÖŹĮæĻąµČ
B£®2gĒāĘųÖŠŗ¬ÓŠ1 molĒā
C£®O2µÄĦ¶ūÖŹĮæŌŚŹżÖµÉĻµČÓŚĘäŅ»øö·Ö×ÓµÄÖŹĮæ
D£®1 mol COµÄÖŹĮæŹĒ28 g”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ČēĶ¼ŹĒĪŅŠ£ŹµŃéŹŅ»ÆѧŹŌ¼ĮÅØĮņĖį±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®ĻÖŠčŅŖ480mL 1mol•L-1µÄĻ”ĮņĖį£®ÓĆøĆÅØĮņĖįŗĶÕōĮóĖ®ÅäÖĘ£¬æɹ©Ń”ÓƵÄŅĒĘ÷ÓŠ£ŗ¢Ł½ŗĶ·µĪ¹Ü£»¢Ś²£Į§°ō£»¢ŪÉÕ±£»¢ÜĮæĶ²£®
ČēĶ¼ŹĒĪŅŠ£ŹµŃéŹŅ»ÆѧŹŌ¼ĮÅØĮņĖį±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®ĻÖŠčŅŖ480mL 1mol•L-1µÄĻ”ĮņĖį£®ÓĆøĆÅØĮņĖįŗĶÕōĮóĖ®ÅäÖĘ£¬æɹ©Ń”ÓƵÄŅĒĘ÷ÓŠ£ŗ¢Ł½ŗĶ·µĪ¹Ü£»¢Ś²£Į§°ō£»¢ŪÉÕ±£»¢ÜĮæĶ²£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ÓČėĮņĖįĶæÉŹ¹ŠæÓėĻ”ĮņĖįµÄ·“Ó¦ĖŁĀŹ¼Óæģ£¬ĖµĆ÷Cu2+¾ßÓŠ“ß»Æ×÷ÓĆ | |
| B£® | øł¾ŻHA”¢HBµÄµēĄė³£ŹżµÄĻą¶Ō“óŠ”æÉŅŌÖ±½ÓÅŠ¶ĻĮ½ÖÖČÜŅŗµÄĖįŠŌĒæČõ | |
| C£® | ³£ĪĀĻĀ2S2O£Øg£©ØT3S£Øs£©+SO2£Øg£©ÄÜ×Ō·¢½ųŠŠ£¬æÉĶʶĻøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦ | |
| D£® | ½«ÅØĮņĖįŗĶÅØĻõĖį»ģŗĻŗóĮ¢¼“·ÅČėĢśĘ¬£¬ĢśĘ¬±»¶Ū»ÆµÄŠ§¹ūŅ»¶Ø»įøüŗĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻąĶ¬ĪĀ¶ČĻĀ£¬½«×ćĮæĀČ»ÆŅų¹ĢĢå·Ö±š·ÅČėĻąĶ¬Ģå»żµÄ¢ŁÕōĮóĖ® ¢Ś0.1 mol/LŃĪĖį¢Ū0.1 mol/LĀČ»ÆĆ¾ČÜŅŗ ¢Ü0.1 mol/LĻõĖįŅųČÜŅŗÖŠ£¬Ag+ÅØ¶Č£ŗ¢Ł£¾¢Ü=¢Ś£¾¢Ū | |
| B£® | ŌŚŗ¬ÓŠBaSO4³ĮµķµÄČÜŅŗÖŠ¼ÓČėNa2SO4¹ĢĢ壬c£ØBa2+£©Ōö“ó | |
| C£® | ĻņMg£ØOH£©2Šü×ĒŅŗÖŠµĪ¼ÓFeCl3ČÜŅŗ£¬³Įµķ±äĪŖŗģŗÖÉ«£¬ĖµĆ÷Čܽā¶ČMg£ØOH£©2£¾Fe£ØOH£©3 | |
| D£® | ŅŃÖŖI3-?I2+I-£¬ĻņŹ¢ÓŠKI3ČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČėŹŹĮæCCl4£¬Õńµ“¾²ÖĆŗóCCl4²ćĻŌ×ĻÉ«£¬ĖµĆ÷KI3ŌŚCCl4ÖŠµÄČܽā¶Č±ČŌŚĖ®ÖŠµÄ“ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com