
| A�� | ��V��NaOH��=20 mLʱ����Һ�и�����Ũ�ȵĴ�С˳��Ϊc��Na+����c��HA-����c�� A2-����c�� OH-��������H+�� | |
| B�� | �������Ũ�ȵ�NaOH��Һ��H2A��Һ��Ϻ�����Һ��ˮ�ĵ���̶ȱȴ�ˮ�еĴ� | |
| C�� | ��Ũ��H2A��NaHA�Ļ����Һ�����ۼ���������ǿ���ǿ���Һ��pH�仯������ | |
| D�� | ��V��NaOH��=40 mLʱ�������¶ȣ�$\frac{c��N{a}^{+}��}{c��{A}^{2-}��}$��С |
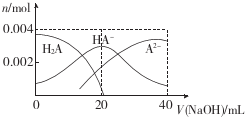
���� A������ͼ��֪����V��NaOH��=20ʱ��������ӦΪNaOH+H2A�TNaHA+H2O����Һ��ҪΪNaHA������Ϊ������Һ�����ԣ�
B����������ˮ���룬�����������ӵ��δٽ�ˮ���룻
C������ijЩ��Һ�м���һ��������ͼ�ʱ�����谭��ҺpH�仯�����ã���Ϊ�������ã���������Һ����������Һ��������HA������NaA����ɵĻ�����Һ����Ļ������ã���������Һ�д����㹻���ļ�A-��Ե�ʣ�����������Һ�м���һ������ǿ��ʱ��H ���ӻ����ϱ�A-�������ģ�������Һ��pHֵ�������䣻������һ����ǿ��ʱ����Һ�д��ڵ�����HA����OH-���Ӷ��谭pH�ı仯����Ũ��H2A��NaHA�Ļ����Һ�γɻ�����Һ����Һ�д��ڵ���ƽ���ˮ��ƽ�⣬�������Լ��
D����20mL 0.2mol��L-1��Ԫ��H2A��Һ�еμ�0.2mol��L-lNaOH��Һ40ml����Ӧ��õ���ҺΪNa2A��Һ��A2-����ˮ����Һ�Լ��ԣ����ȴٽ�ˮ��A2-����Ũ�ȼ�С��
��� �⣺A������ͼ��֪����V��NaOH��=20 mLʱ��������ӦΪNaOH+H2A�TNaHA+H2O��������ҪΪNaHA��HA-����̶ȴ���ˮ��̶ȣ���Һ�����ԣ�ˮ��HA-������������ӣ�ֻ��HA-�����A2-����������Ũ�ȴ�С˳����c��Na+����c��HA-����c��H+����c��A2-����c��OH-������A����
B���������Ũ�ȵ�NaOH��Һ��H2A��Һ��Ϻõ�NaHA����Һ����ͼʾ��ϵ֪��c��A2-����c��H2A����˵���������ˮ��̶ȣ���Һ�����ԣ�ˮ�ĵ����ܵ������ƣ���B����
C����Ũ��H2A��NaHA�Ļ����Һ�γɻ�����Һ����Һ�д��ڵ���ƽ��H2A?H++HA-��ˮ��ƽ�� NaHA+H2O?NaOH+H2A��������HA-����������������H2A�����������H2A��Ӧ��NaHA���谭��ҺPH�ı仯���������ۼ���������ǿ���ǿ���Һ��pH�仯������C��ȷ��
D����20mL 0.2mol��L-1��Ԫ��H2A��Һ�еμ�0.2mol��L-lNaOH��Һ40ml����Ӧ��õ���ҺΪNa2A��Һ��A2-����ˮ����Һ�Լ��ԣ����ȴٽ�ˮ��A2-����Ũ�ȼ�С��������Ũ�Ȳ��䣬���ֵ����D����
��ѡC��
���� ���⿼���������Һ��Ӧ�Ķ����жϣ���ȷͼ���������ʱ��Һ�е������ǽ����Ĺؼ���ץסͼ����з������ɣ�ע�����Һ��ԭ������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ӧǰ���Ƿ�����ԭ�ӵĵ�ʧ | |
| B�� | ����Ӧǰ���Ƿ���ԭ�ӵ�������� | |
| C�� | ����Ӧǰ���Ƿ���Ԫ�صĻ��ϼ۷����ı� | |
| D�� | ����Ӧ���Ƿ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
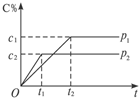 ��һ���¶��µĿ��淴Ӧ��mA��g��+nB��g��?pC��g��+qD��g����������C�����������ѹǿp1��p2��ʱ��t1��t2�Ĺ�ϵ��ͼ��ʾ���������й�ϵ����ȷ���ǣ�������
��һ���¶��µĿ��淴Ӧ��mA��g��+nB��g��?pC��g��+qD��g����������C�����������ѹǿp1��p2��ʱ��t1��t2�Ĺ�ϵ��ͼ��ʾ���������й�ϵ����ȷ���ǣ�������| A�� | p1��p2 | B�� | ��Ӧ���� | C�� | m+n��p+q | D�� | m+n��p+q |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����£�1molC6H1206����ԭ����Ϊ6NA | |
| B�� | 0.1moICl2������ˮ��ֻ�ϣ�ת�Ƶ�����Ϊ0.1NA | |
| C�� | 25�棬pH=13��Ba��OH��2��Һ����OH-��ĿΪ0.2NA | |
| D�� | 22.4L N2��NH3������庬���õ��Ӷ���ĿΪ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
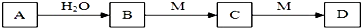
| A�� | ��MΪ���г�������ζ�����壬��D����Ϊ��ʽ�Σ���M��A��=M��C�� | |
| B�� | ��MΪ��������D����Һ��ͨ��A���ܵ�C | |
| C�� | ��CΪ���Cת��ΪD�ķ�Ӧ��CO32-+H2O+CO2�T2HCO3-����A����Ϊ���� | |
| D�� | ��MΪ���������Σ���A��ˮ��Ӧ���ܲ���������Ҳ���ܲ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3�� | B�� | 4�� | C�� | 5�� | D�� | 6�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol•L-1NaHCO3��Һ�У�c��Na+��+c��H+��=c��HCO3-��+2c��CO32-��+c��OH-�� | |
| B�� | ������������ʵ���Ũ�ȵ�NaX������HX��Ϻ�����Ե���Һ�У�c��X-����c��Na+����c��HX����c��H+����c��OH-�� | |
| C�� | ��0.2 mol•L-1 NaA��Һ��0.1 mol•L-1��������������ü�����Һ�У�c��Na+��+c��H+��=c��A-��+c��Cl-��+c��OH-�� | |
| D�� | 1.5 L 0.1 mol•L-1 NaOH��Һ�л���ͨ��CO2����Һ����4.4 gʱ����Һ�У�c��Na+����c��CO32-����c��HCO3-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������費��ǿ�ᷴӦ������ʯӢ����ʢ������� | |
| B�� | MgO��Al2O3���۵�ܸߣ����������²��� | |
| C�� | �����������Ư���ԣ�������Ư��ֽ���Ͳ�ñ�� | |
| D�� | ͭ����ʹ�����ʱ��ԣ���Ӿ���ݳ�������ͭ����ˮ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com