
【题目】下列关于有机化合物的说法正确的是( )
A.聚氯乙烯分子能使溴水褪色
B.己烷共有4种同分异构体,它们的熔点、沸点各不相同
C.在一定条件下苯分别与液溴、硝酸作用生成溴苯、硝基苯的反应都属于取代反应
D.![]() 代表纯净物
代表纯净物
【答案】C
【解析】
A.聚氯乙烯不含碳碳双键;
B.己烷有五种同分异构体,同分异构体的物理性质不同;
C.苯分别与液溴、硝酸作用生成溴苯、硝基苯,可看作溴原子、硝基替代苯的氢原子;
D.二氯乙烷存在同分异构体.
A.聚氯乙烯不含碳碳双键,与溴水不反应,故A错误;
B.己烷有五种同分异构体,其碳链结构分别为![]() 、
、![]() 、
、![]() 、
、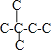 、
、![]() ,己烷的同分异构体为不同物质,所以其熔沸点不同,且含有支链越多其熔沸点越低,故B错误;
,己烷的同分异构体为不同物质,所以其熔沸点不同,且含有支链越多其熔沸点越低,故B错误;
C.苯分别与液溴、硝酸作用生成溴苯、硝基苯,可看作溴原子、硝基替代苯的氢原子,都为取代反应,故C正确;
D.二氯乙烷存在同分异构体,分别为1,1-二氯乙烷、1,2-二氯乙烷,故D错误。
故选:C。


科目:高中化学 来源: 题型:
【题目】化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等离不开化学。
(1)普通玻璃是常见的硅酸盐产品,其主要成分的化学式为Na2CaSi6O14,以氧化物形式可表示为______。
(2)缺铁性贫血患者补充的铁,通常为硫酸亚铁的形式,而硫酸铁则没有这种药效.当用硫酸亚铁制成药片时外表要包有一层特殊的糖衣,这层糖衣的作用是______.若在酸性的硫酸亚铁溶液中通入氧气,也能得到棕黄色溶液,请写出此反应的离子方程式______.检验棕黄色溶液是否有Fe2+,可选用的试剂为______(填字母)。
A.稀硝酸B.浓硫酸C.KSCN溶液D.酸性高锰酸钾溶液
(3)从降低成本和减少环境污染的角度考虑,制取硫酸铜最好的方法是______(填字母)。
A.铜和浓硫酸反应B.铜和稀硫酸反应
C.氧化铜和硫酸反应D.铜与Fe2(SO4)3溶液反应
(4)实验室用硫酸铜晶体配制一定物质的量浓度的硫酸铜溶液,下列操作将使所配溶液物质的量浓度偏高的是______(填字母)。
A.所用的硫酸铜晶体已经部分风化失水
B.移液时不小心溅出少许溶液
C.容量瓶查漏后未经干燥就直接使用
D.定容时俯视容量瓶刻度线
E.未洗涤烧杯和玻璃棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下列是八种环状的烃类物质:
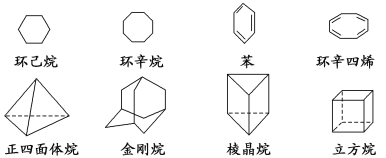
(1)互为同系物的有________和________(填名称)。互为同分异构体的有________和________、______和________……(填写名称,可以不填满,也可以再补充)。
(2)正四面体烷的一氯取代产物有________种,二氯取代产物有________种;立方烷的一氯取代产物有________种,二氯取代产物有________种;金刚烷的一氯取代产物有________种。
Ⅱ.如图所示都是简化的碳骨架结构,请回答:
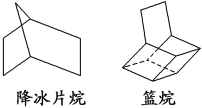
(1)其分子式分别是________、________。
(2)降冰片烷发生一氯取代时,取代位置有______种。
(3)篮烷发生一氯取代时,其一氯取代物有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】愈创木酚作原料合成香草醛的路线如图所示,下列说法正确的是( )
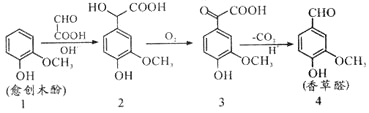
A.检验制得的香草醛中是否混有化合物3,可用氯化铁溶液
B.化合物2在一定条件下可发生加聚反应
C.理论上反应1→2中原子利用率100%
D.等物质的量的四种物质与足量NaOH溶液反应,消耗NaOH物质的量比为1:3:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列有关说法正确的是( )
A. 0.5 mol苯分子中含有C=C双键数为1.5 NA
B. 1 mol甲基(﹣CH3)所含的电子总数为10 NA
C. 标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为![]() NA
NA
D. 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢溴酸在医药和石化工业上有广泛的用途。下图是工业制备氢溴酸粗品并精制的流程:(沸点:Br2:58.5℃;HBr:-66.8℃;H2SO4:338℃)

(1)混合①中反应的离子方程式是__________________________________。
(2)混合①中不直接用水而使用冰水的目的是________________________。
(3)操作b适用于______混合物的分离(填序号)。
A.固体和液体 B.固体和固体 C.互不相溶的液体 D.互溶的液体
(4)混合②中加入亚硫酸钠的目的是__________________。
(5)纯净的氢溴酸应为无色液体,但工业生产中制得的氢溴酸(工业氢溴酸)常带有黄色,甲同学猜测可能是含有Fe3+,乙同学猜测可能是含有Br2。请写出证实乙同学猜想的实验方法是________________________。
(6)若起始使用m kg溴单质作原料,完成生产后,得到精制氢溴酸溶液250 L。取2.5 mL精制溶液稀释,在稀释液中加入足量的硝酸银溶液充分反应,若充分反应后得到n g淡黄色沉淀,则单质溴的利用率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋硝香豆素是一种治疗心脑血管疾病的药物,能阻碍血栓扩展,其结构简式为:
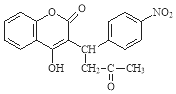
醋硝香豆素可以通过以下方法合成(部分反应条件省略)。

已知: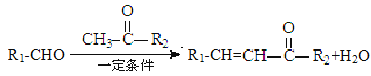
回答以下问题:
(1)反应①的反应类型是______。
(2)从A到B引入的官能团名称是______。
(3)物质C的结构简式为______。
(4)反应③的化学方程式为______。
(5)关于E物质,下列说法正确的是______(填字母序号)。
a 在核磁共振氢谱中有四组吸收峰
b 可以用酸性高锰酸钾溶液鉴别D和E
c 可以发生加成反应、聚合反应、氧化反应和还原反应
d 存在顺反异构
(6)分子结构中只含有一个苯环,且同时符合下列条件的G的同分异构体共有______种。
①可与氯化铁溶液发生显色反应;
②可与碳酸氢钠溶液反应生成二氧化碳气体。其中,苯环上的一氯代物只有两种的同分异构体的结构简式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接排放含SO2的烟气会形成酸雨,危害环境。利用钠、碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:____。
(2)在钠、碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是_____。
(3)吸收液吸收SO2的过程中,pH随n(SO32-)∶n(HSO3-)变化关系如表:
n(SO32-)∶n(HSO3-) | 91∶9 | 1∶1 | 1∶91 |
pH | 8.2 | 7.2 | 6.2 |
上表判断NaHSO3溶液显___性,用化学平衡原理解释:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有媒体报道一种新型污水处理装置问世,该装置可利用一种微生物将有机废水的化学能直接转化为电能,该装置的构造如图所示。下列说法中正确的是( )
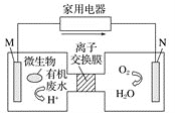
A. 装置外层电路中箭头的方向代表电流的方向
B. 该装置为原电池装置,其中N为负极
C. 该装置为电解池装置,其中M为阳极
D. 若有机废水中含有葡萄糖,则M电极发生的电极反应式为C6H12O6+6H2O-24e-![]() 6CO2+24H+
6CO2+24H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com