

 ��
�� ���� �������ھƻ�ø�������������л���A��AΪCH3CH2OH��B��ʯ�ͻ�ѧ��ҵ����Ҫ�Ļ���ԭ�ϣ���BΪCH2=CH2��A������ȥ��Ӧ����B������C�ķ���ʽ��֪��A������CΪCH3COOH��B��C������Ϣ�еķ�Ӧ����DΪCH3COOCH=CH2��D�����Ӿ۷�Ӧ��EΪ ����������һ�������¿�����ΪX��Y��X����Է�����������A��B֮�䣬Y����Է���������A��ͬ��X�ɴ�������Y����XΪHCHO��YΪHCOOH��X����H2��Ӧ����Z����ZΪCH3OH���ݴ˽��д��⣮
����������һ�������¿�����ΪX��Y��X����Է�����������A��B֮�䣬Y����Է���������A��ͬ��X�ɴ�������Y����XΪHCHO��YΪHCOOH��X����H2��Ӧ����Z����ZΪCH3OH���ݴ˽��д��⣮
��� �⣺�������ھƻ�ø�������������л���A��AΪCH3CH2OH��B��ʯ�ͻ�ѧ��ҵ����Ҫ�Ļ���ԭ�ϣ���BΪCH2=CH2��A������ȥ��Ӧ����B������C�ķ���ʽ��֪��A������CΪCH3COOH��B��C������Ϣ�еķ�Ӧ����DΪCH3COOCH=CH2��D�����Ӿ۷�Ӧ��EΪ ����������һ�������¿�����ΪX��Y��X����Է�����������A��B֮�䣬Y����Է���������A��ͬ��X�ɴ�������Y����XΪHCHO��YΪHCOOH��X����H2��Ӧ����Z����ZΪCH3OH��
����������һ�������¿�����ΪX��Y��X����Է�����������A��B֮�䣬Y����Է���������A��ͬ��X�ɴ�������Y����XΪHCHO��YΪHCOOH��X����H2��Ӧ����Z����ZΪCH3OH��
��1����DΪCH3COOCH=CH2��D�й����ŵ�������������̼̼˫�����ʴ�Ϊ��������̼̼˫����
��A��B�Ļ�ѧ����ʽΪ��CH3CH2OH$��_{170��}^{Ũ����}$CH2=CH2��+H2O���ʴ�Ϊ��CH3CH2OH$��_{170��}^{Ũ����}$CH2=CH2��+H2O��
�۸�������ķ�����֪��E�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2����A��XΪHCHO�������£�HCHOΪ���壬��A��ȷ��
B�������������У��������Ǻ�HCHO��HCOOH�����Է���������Ӧ����B����
C��AΪCH3CH2OH��YΪHCOOH�����Dz���ͬ���칹�壬��C����
D��AΪCH3CH2OH��ZΪCH3OH����������ͬ�������ǻ�������ͬϵ���D��ȷ��
�ʴ�Ϊ��AD��
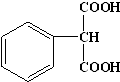
������������Է���������ͬ�ķ����廯����N������Է�������Ϊ180�����ı�����ֻ��һ��ȡ������1mol N������NaHCO3��Ӧ������44.8L CO2����״������2mol������ÿ��N���������Ȼ�����N�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϼ��л���ṹ�����ʣ�Ϊ��Ƶ���㣬��Ŀ�Ѷ��еȣ����ݷ�Ӧ���������ƶϣ���ȷ�ж����ʽṹ��ʽ�ǽⱾ��ؼ���ע��������Ϣ�����ã�����������ѧ���ķ���������������������


 ��ս100��Ԫ����Ծ�ϵ�д�
��ս100��Ԫ����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ����Ӧ�ܵõ���ѧʽΪC7H5O3Na���ǣ�������
����Ӧ�ܵõ���ѧʽΪC7H5O3Na���ǣ�������| A�� | NaHCO3��Һ | B�� | Na2CO3��Һ | C�� | NaOH��Һ | D�� | NaCl��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ʱ�����ɵ��������������ӵ����� | |
| B�� | ���������ʱ�����ɵ������������������ӵ��Ǽ� | |
| C�� | ���������ʱ��ֻ���ɽ��������Ӻ���������ӵ����� | |
| D�� | NH4Cl�ĵ��뷽��ʽ��NH4Cl�TNH${\;}_{4}^{+}$+Cl-������NH4Cl���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Na+��K+��SO42-��HCO3- | B�� | Cu2+��K+��SO42-��NO3- | ||
| C�� | Na+��K+��Cl-��SO42- | D�� | Na+��K+��NO3-��I- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | x��ֵΪ4 | B�� | A��ת����Ϊ60% | ||
| C�� | B��ƽ��Ũ��Ϊ0.8 mol/L | D�� | D���������Ϊ20% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NA | B�� | 2NA | C�� | 1 | D�� | 2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com