
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 分子中可能含有氧原子 | D. | 有机物的分子式为CH4Ox(x=O、1) |
分析 某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,则该有机物分子中含有C、H个数之比为1:4,有机物的分子式为CH4Ox(x=O、1),无法确定是否含有氧元素,据此对各选项进行判断.
解答 解:A.不能确定该有机物分子中是否含有氧元素,故A错误;
B.生成的CO2和H2O的物质的量之比为1:2,则该有机物分子中含有C、H个数之比为1:4,故B错误;
C.该有机物分子中可能含有氧元素,故C正确;
D.该有机物分子中含有C、H个数之比为1:4,有机物的分子式为CH4Ox(x=O、1),故D正确;
故选CD.
点评 本题考查有机物分子式的确定的计算与判断,题目难度不大,注意掌握确定有机物分子式、结构简式的方法,明确题中缺少有机物的质量、无法确定是否含有氧元素,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 20 mL 3 mol•L-1 | B. | 20 mL 2 mol•L-1 | ||
| C. | 10 mL 4 mol•L-1 | D. | 10 mL 2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 实验操作 | 实验目的 | |
| A | 苯和溴水混合后加入铁粉 | 制溴苯 |
| B | 乙醇与高锰酸钾(KMnO4)酸性溶液混合 | 验证乙醇具有还原性 |
| C | 蔗糖溶液加稀硫酸,水浴加热一段时间后,加新制备的Cu(OH)2悬浊液,加热 | 证明蔗糖水解后产生葡萄糖 |
| D | 向纯碱中滴加醋酸,将产生的气体分别通入饱和NaHCO3溶液、苯酚钠浓溶液 | 证明酸性:醋酸>碳酸>苯酚 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
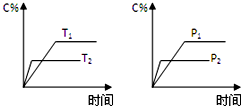 可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )| A. | 化学方程式中a+b>c+d | |
| B. | 达平衡后,加入催化剂则C%增大 | |
| C. | 达平衡后,若升温,平衡逆向移动 | |
| D. | 其他条件不变,在不同温度达平衡后,C在T1时的反应速率大于T2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 陈述I | 陈述II | |
| A | 二氧化硫使高锰酸钾溶液褪色 | 二氧化硫具有漂白性 |
| B | 铁与高温水蒸气能反应 | 四氧化三铁可以作为颜料 |
| C | 同一周期从左至右核电荷数增大 | 同一周期主族元素从左至右原子半径减小 |
| D | 经过打磨的铝片与盐酸反应速率由慢到快 | 铝片与盐酸反应是放热反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
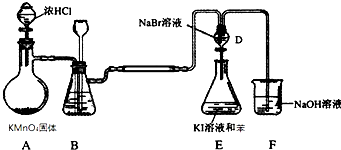
| A. | 装置E下层呈现紫红色 | |
| B. | 装置B中可盛放水吸收氯气中的HCl气体 | |
| C. | F2不能与NaCl溶液反应置换出氯气 | |
| D. | 装置E中有机试剂层呈现紫红色,能说明非金属性Br>I |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 金属钾与水反应:2K+2H2O═2K++2OH-+H2↑ | |
| C. | 氧化铝溶于NaOH溶液:Al2O3+2OH-═2AlO2-+H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com