
【题目】实验室中通常加热无水乙醇与浓硫酸的混合物的方法制取乙烯,在具体的化学实验中常因加热的温度过高导致副反应发生而使乙烯气体中混有二氧化硫气体,有人设计下列实验以确认乙烯气体中混有二氧化硫气体。请回答下列问题:
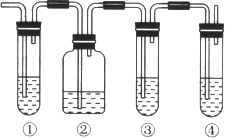
(1) 图中①和④的容器内盛放的化学试剂分别是(填写代号)
①_____________________、④_________________________。
A.品红溶液 B.烧碱溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明二氧化硫气体存在的现象是____________________________________________。
(3)使用装置②的目的是______________________;使用装置③的目的是__________________。
(4)确认乙烯气体存在的现象是_____________________________________________________。
(5)确认乙烯气体的存在还可用溴水,请写出乙烯与溴水反应的方程式_________________;其反应类为______________________________________。
【答案】A D 装置①中的品红溶液褪色 除去二氧化硫 检验二氧化硫是否除干净 装置③中的品红溶液不褪色,装置④中的酸性高锰酸钾溶液褪色 CH2=CH2+Br2→CH2BrCH2Br 加成反应
【解析】
二氧化硫为酸性氧化物,可与碱反应,可使品红溶液褪色,具有还原性,可与酸性高锰酸钾溶液发生氧化还原反应,而乙烯含有碳碳双键,也能与酸性高锰酸钾溶液发生氧化还原反应,所以应该先检验二氧化硫,然后检验乙烯,结合装置图和问题分析解答。
(1)装置①中盛放品红溶液,用来检验二氧化硫,然后将气体通入盛有氢氧化钠溶液的洗气瓶中除去二氧化硫,再通入品红溶液检验二氧化硫是否除尽,最后通入酸性高锰酸钾溶液检验乙烯,则装置④中盛放酸性高锰酸钾溶液。答案选A、D;
(2)二氧化硫具有漂白性,能够使品红溶液褪色,则能说明二氧化硫气体存在的现象是装置①中的品红溶液褪色。
(3)根据以上分析可知使用装置②的目的是除去二氧化硫,避免干扰乙烯的检验;使用装置③的目的是检验二氧化硫是否除干净,防止干扰乙烯的性质检验。
(4)根据以上分析可知确认乙烯气体存在的现象是装置③中的品红溶液不褪色,装置④中的酸性高锰酸钾溶液褪色。
(5)乙烯含有碳碳双键,与溴水发生加成反应,反应的方程式为CH2=CH2+Br2→CH2BrCH2Br。


科目:高中化学 来源: 题型:
【题目】实验是化学研究的一种重要手段,现有图所示A-G七种仪器,请根据要求填空。

(I)写出仪器名称:F_________。
(II)下列实验操作中用到仪器G的是_______(选填下列选项的编号字母)。
a.分离水和CC14的混合物b.分离水和酒精的混合物c.分离水和泥砂的混合物
(III)配制480mL、0.2molL-1CuSO4溶液。
(1)应用托盘天平称取CuSO45H2O晶体____________,
(2)使用容量瓶前必须进行的一步操作是________,在容量瓶上需标记的是____________(填字母),
a.温度b.刻度线c.浓度d.容积
(3)所需仪器除了烧杯、玻璃棒、托盘天平外,还缺少__________________,
(4)实验中两次用到玻璃棒,起作用分别是____________、____________。
(5)配制溶液时除了称量、溶解、冷却、转移溶液、摇匀操作外,还缺少:__________________(填操作名称)。
(6)若实验中有下列情况,对配制溶液的浓度有何影响?(填“偏高”、“偏低”或“无影响”)
a.胆矾失去了部分结晶水____________;
b.定容时加水超过刻度线____________;
c.最终定容时仰视观察液面____________;
d.容量瓶不干燥,含有少量蒸馏水____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中书写正确的是( )
A.碳酸氢钙溶液跟盐酸反应:HCO3-+H+=H2O+CO2↑
B.氯气跟水反应:Cl2+H2O=2H++Cl-+ClO-
C.碳酸氢钠溶液和氢氧化钙溶液混合HCO3-+OH-=CO32-+H2O
D.碳酸钠溶液中滴加少量盐酸CO32-+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为VL的固定容积的容器中发生反应:A(g)+B(g)![]() 3C(g)(正反应为放热反应)下列说法能说明该反应已经达到平衡状态的是( )
3C(g)(正反应为放热反应)下列说法能说明该反应已经达到平衡状态的是( )
①单位时间内生成C的分子数与分解C的分子数相等②外界条件不变时,ABC的浓度不随时间变化③体系温度不再变化④体系的分子总数不再变化 ⑤反应速率3v(B)=v(C)
A.①②B.①②③
C.①②③④D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为了探究锌与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气。(实验记录的体积为累计值,已换算成标准状况):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大___,原因是___。
(2)哪一段时段的反应速率最小___,原因是___。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)___。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.NaNO3溶液D.Na2CO3溶液
你认为可行的是(填编号)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据媒体报道,日本食品巨头明治公司生产的“明治STEP”奶粉中检测出含量超标的放射性元素铯(Cs)。铯较为稳定的核素有![]() 、
、![]() 、
、![]() 、
、![]() 。下列判断不正确的是( )
。下列判断不正确的是( )
A. ![]() 、
、![]() 、
、![]() 、
、![]() 互为同位素
互为同位素
B. ![]() 、
、![]() 、
、![]() 、
、![]() 的核外电子排布相同
的核外电子排布相同
C. ![]() 、
、![]() 、
、![]() 、
、![]() 的性质和用途相同
的性质和用途相同
D. ![]() 、
、![]() 、
、![]() 、
、![]() 的质量数和中子数均不同
的质量数和中子数均不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用240 mL1.0mol·L-1的NaOH溶液,实验操作步骤有:
A.用烧杯在天平上称出ag氢氧化钠固体,加入适量蒸馏水使它完全溶解并冷却至室温;
B.继续向容量瓶中加蒸馏水至液面距刻度线1~2 cm处,改用胶头滴管小心滴加蒸馏水至凹液面与刻度线相切;
C.把制得的溶液小心转移至容量瓶中;
D.将容量瓶瓶塞塞紧,充分摇匀。
E.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,轻轻振荡;
请填写下列空白:
(1)操作步骤的正确顺序为_____(填字母)。
(2)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、____、____。
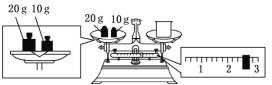
(3)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示(左码右物)。烧杯的实际质量为___g,要完成本实验该同学应称出___gNaOH。
(4)使用容量瓶前必须进行的一步操作是____。
(5)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是___。
A.用滤纸称量NaOH固体
B.定容时俯视刻度线
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容后塞上瓶塞反复倒转摇匀,静置后,液面低于刻度线,再加水至刻度线
(6)若加蒸馏水定容时不慎超过刻度线,处理方法是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )

A.FeCl3溶液、Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是有没有丁达尔效应
B.将NaOH溶液与FeCl3溶液混合可制成Fe(OH)3胶体
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.胶体、分散系、混合物概念间的从属关系可用如图表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃烧![]() 某有机物,得到
某有机物,得到![]() 和
和![]() ,由此可得出结论是
,由此可得出结论是![]()
![]()
A. 该有机物含有2个碳原子和6个氢原子
B. 该有机物中碳元素和氢元素的原子个数比为3:1
C. 该有机物中含有2个![]() 和3个
和3个![]()
D. 该有机物的1个分子里含有2个碳原子和6个氢原子,可能含有氧原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com