
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:
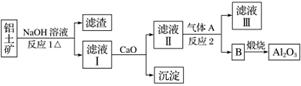
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:
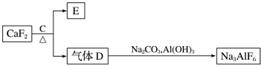
回答下列问题:
(1)写出反应1的化学方程式_______________________________________________________。
(2)滤液Ⅰ中加入CaO生成的沉淀是________,反应2的离子方程式为________________________________________________________________________。
(3)E可作为建筑材料,化合物C是________,写出由D制备冰晶石的化学方程式________________________________________________________________________。
(4)电解法制铝的化学方程式是________,以石墨为电极,阳极产生的混合气体的成分是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
求算下列常温下溶液中由H2O电离的c(H+)和c(OH-)。
(1)pH=2的H2SO4溶液
c(H+)=__________,c(OH-)=__________。
(2)pH=10的NaOH溶液
c(H+)=__________,c(OH-)=__________。
(3)pH=2的NH4Cl溶液
c(H+)=__________。
(4)pH=10的Na2CO3溶液
c(OH-)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
求下列常温条件下溶液的pH(已知lg1.3=0.1,lg2=0.3,混合溶液忽略体积的变化)。
(1)0.005 mol·L-1的H2SO4溶液
(2)0.1 mol·L-1的CH3COOH溶液(已知CH3COOH的电离常数Ka=1.8×10-5)
(3)0.1 mol·L-1NH3·H2O溶液(NH3·H2O的电离度为α=1%,电离度=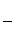 ×100%)
×100%)
(4)将pH=8的NaOH与pH=10的NaOH溶液等体积混合
(5)常温下,将pH=5的盐酸与pH=9的NaOH溶液以体积比11∶9混合
(6)将pH=3的HCl与pH=3的H2SO4等体积混合
(7)0.001 mol·L-1的NaOH溶液
(8)pH=2的盐酸与等体积的水混合
(9)pH=2的盐酸加水稀释到1 000倍
查看答案和解析>>
科目:高中化学 来源: 题型:
KMnO4溶液常用作氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中的某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液的操作如下所示:
①称取稍多于所需量的KMnO4固体溶于水中,将溶液加热并保持微沸1 h;②用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;③过滤得到的KMnO4溶液贮存于棕色试剂瓶并放在暗处;④利用氧化还原滴定方法,在70~80 ℃条件下用基准试剂(纯度高、相对分子质量较大、稳定性较好的物质)溶液标定其浓度。
请回答下列问题:
(1)准确量取一定体积的KMnO4溶液需要使用的仪器是____________。
(2)在下列物质中,用于标定KMnO4溶液的基准试剂最好选用________(填字母)。
A.H2C2O4·2H2O B.FeSO4
C.浓盐酸 D.Na2SO3
(3)若准确称取W g你选的基准试剂溶于水配成500 mL溶液,取25.00 mL置于锥形瓶中,用KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。KMnO4溶液的物质的量浓度为________mol·L-1。
(4)若用放置两周的KMnO4标准溶液去测定水样中Fe2+的含量,测得的浓度值将________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,向一定体积0.1 mol·L-1的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )
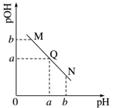
A.M点所示溶液的导电能力强于Q点
B.N点所示溶液中c(CH3COO-)>c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
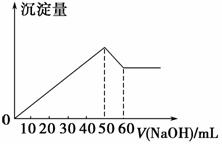
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如右图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )。
A.6∶1 B.3∶1
C.2∶1 D.1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)Na2O2与Na2O中均只存在离子键( )
(2)Na2O2与Na2O晶体中阳离子与阴离子的个数比均为2∶1( )
(3)2Na2O2+2H2O===4NaOH+O2↑
H2O既不是氧化剂也不是还原剂( )
(4)Na2O、Na2O2组成元素相同,与CO2反应产物也相同( )
(5)Na2O2的电子式为Na
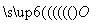 ·
· ·
·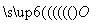
 Na( )
Na( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com