
若某原子在处于能量最低状态时,外围电子排布式为4d15s2,则下列说法正确的是( )
A.该元素原子处于能量最低状态时,原子中共有3个未成对电子
B.该元素原子核外共有5个电子层
C.该元素原子的M能层共有8个电子
D.该元素原子最外层共有3个电子
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
(1)已知:
①Fe(s)+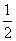 O2(g)===FeO(s)
O2(g)===FeO(s)
ΔH1=-272.0 kJ·mol-1;
②2Al(s)+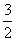 O2(g)===Al2O3(s)
O2(g)===Al2O3(s)
ΔH2=-1 675.7 kJ·mol-1。
Al和FeO发生铝热反应的热化学方程式是_______________________________________________________________
_______________________________________________________________。
某同学认为,铝热反应可用于工业炼铁,你的判断是________(填“能”或“不能”),你的理由是___________________________________________
________________________________________________________________。
(2)反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示。
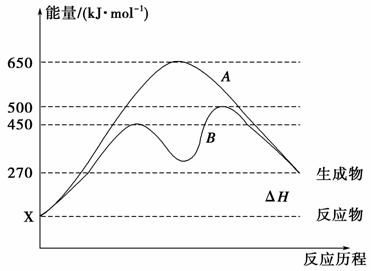
①据图判断该反应是________(填“吸”或“放”)热反应,当反应达到平衡后,其他条件不变,升高温度,反应物的转化率将________(填“增大”、“减小”或“不变”)。
②其中B历程表明此反应采用的条件为________(填字母)。
A.升高温度 B.增大反应物的浓度
C.降低温度 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学实验事实及其解释不正确的是( )
A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3
B.钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气
C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应
D.钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外活动小组设计下列实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。
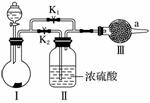
(1)过氧化钠与二氧化碳反应的化学方程式是____________________________________,该反应中,反应物的总能量__________(填“大于”或“小于”)生成物的总能量。
(2)装置Ⅰ中的试剂是__________(填字母)
a.稀盐酸 b.稀硫酸
c.小苏打 d.石灰石
(3)实验时,应先打开弹簧夹__________(填“K1”或“K2”),观察到预期现象后,关闭它,再打开另一个弹簧夹。
(4)实验过程中将带火星的木条置于a口,观察到带火星的木条始终不复燃。
①为观察到最终木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是________________________________________________________________________;
②乙认为即使采纳甲的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是________________________________________________________________________
________________________________________________________________________。
(5)为进一步达到实验目的,应补充的实验是:取最终反应后Ⅲ中所得固体,________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
同周期的三种元素X、Y、Z,已知其最高价氧化物对应水化物的酸性强弱为HXO4>H2YO4>H3ZO4,则下列判断错误的是( )
A.原子半径:X>Y>Z B.气态氢化物的稳定性HX>H2Y>ZH3
C.电负性:X>Y>Z D.非金属性:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利不相容原理________,哪些违反了洪特规则____________________。

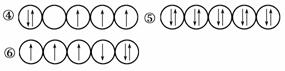
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为____________________________;其最高价氧化物对应的水化物的化学式是________。
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:2s 3d 4s 3s 4p 3p
轨道能量由低到高排列顺序是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除杂操作可行的是( )
A.通过浓硫酸除去HCl中的H2O
B.通过灼热的CuO除去H2中的CO
C.通过灼热的镁粉除去N2中的O2
D.通过水除去CO中的CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
1 mol乙醛分子中含有σ键的数目为________,乙酸的沸点明显高于乙醛,其主要原因是____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com