
分析 (1)①根据化合物中化合价的代数和为零计算;盐是指一类金属离子或铵根离子(NH4+)与酸根离子或非金属离子结合的化合物;
②a.胶体较稳定,溶液稳定;
b.溶液无丁达尔效应;
c.胶粒和溶液都可透过滤纸;
(2)根据MnO2和盐酸的反应和氯气与NaOH溶液的反应,类推反应;
(3)H2O2与Ca(OH)2作用形成酸式盐为Ca(HO2)2,同时生成水.
解答 解:(1)①Fe(CrO2)2中,氧元素的化合价是-2价,总的负价是-8价,铬元素的化合价是+3价,2个铬原子化合价是+6价,所以铁元素化合价是+2价;Fe(CrO2)2是由亚铁离子和CrO2-组成的盐,
故答案为:+2;盐;
②a.胶体较稳定,溶液是稳定的,故A错误;
b.溶液无丁达尔效应,胶体有丁达尔效应,故b错误;
c.胶粒和溶液都可透过滤纸,所以明胶的水溶液和K2SO4溶液中的分散质粒子可通过滤纸,故c正确;
故答案为:c;
(2)①由二氧化锰和浓盐酸的反应可知MnO2和HSCN反应的化学方程式为:MnO2+4HSCN(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn(SCN)2+(SCN)2↑+2H2O,
故答案为:MnO2+4HSCN(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn(SCN)2+(SCN)2↑+2H2O;
②由Cl2+2NaOH=NaCl+NaClO+H2O可知,(CN)2的化学性质和卤素很相似,则(CN)2与NaOH(aq)反应的化学方程式为(CN)2+2NaOH=NaCN+NaCNO+H2O,离子方程式为(CN)2+2OH-=CN-+CNO-+H2O,
故答案为:(CN)2+2OH-=CN-+CNO-+H2O;
(3)H2O2为二元酸,其第一步电离方程式为H2O2?H++HO2-,则H2O2与Ca(OH)2作用形成酸式盐为Ca(HO2)2,同时生成水,故答案为:Ca(HO2)2.
点评 本题考查了元素的化合价、胶体的性质和化学反应方程式的书写,明确信息与反应的关系即可解答,题目难度中等.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
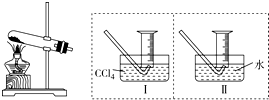 某化学兴趣小组的同学为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,他们开展了如下探究性学习.
某化学兴趣小组的同学为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,他们开展了如下探究性学习.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | b为负极 | |
| B. | 该电池放电时,Cu集流板上Cu失电子 | |
| C. | 充电时,F-通过交换膜从b极区移向a极区 | |
| D. | 充电时,阳极的电极反应式为2MnF2+2F--2e-═2MnF3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com