
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) 1/2N2(g)+CO2(g);ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
1/2N2(g)+CO2(g);ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A 加催化剂同时升高温度 B 加催化剂同时增大压强
C 升高温度同时充入N2 D 降低温度同时增大压强
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
可确认发生了化学平衡移动的是( )
A.化学反应速率发生了改变
B.有气态物质参加的可逆反应达到平衡后,改变了压强
C.由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变
D.可逆反应达到平衡后,使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度和压强下,有1 mol某气体A,发生如下反应2A(g)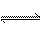 xB(g)+C(g),当达到平衡时,A在混合气中的体积分数为58.84%,混合气的总质量为46 g,平均相对分子质量为39.8,求:
xB(g)+C(g),当达到平衡时,A在混合气中的体积分数为58.84%,混合气的总质量为46 g,平均相对分子质量为39.8,求:
(1)A的分解率;
(2)x的值。
查看答案和解析>>
科目:高中化学 来源: 题型:
两份体积相同的某植物营养液,其配方如下:
|
含量
编号 | KCl | K2SO4 | ZnSO4 | ZnCl2 |
| ① | 0.3mol | 0.2mol | 0.1mol | — |
| ② | 0.1mol | 0.3mol | — | 0.1mol |
①②两份营养液的成分(所含离子):
A. 仅n(K+)相同 B. 仅n(Cl-)相同 C. 不完全相同 D. 完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室通常用MnO2和浓盐酸共热制取Cl2,反应的化学方程式为
MnO2 + 4HCl(浓) 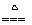 MnCl2 + Cl2↑+ 2H2O。
MnCl2 + Cl2↑+ 2H2O。
(1)该反应的氧化剂是 ,氧化产物是 ,用单线桥法表示上述反应电子转移方向和数目。
(2)计算当有73.0克HCl完全参加反时,消耗MnO2的物质的量为多少?
生成的气体在标准状况下的体积多少升?
查看答案和解析>>
科目:高中化学 来源: 题型:
在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡: CH3COOH CH3COO-+H+
CH3COO-+H+
对于该平衡,下列叙述正确的是
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,叙述错误的是 ( )
A.该溶液的pH=4
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:高中化学 来源: 题型:
对于化学反应3W(g)+2X(g) =4Y(g)+3Z(g),下列反应速率关系中正确的是
A.v(W)=3v(Z) B.2v(X)=3v(Z) C.2v(X)=v(Y) D.3v(W)=2v(X)
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA是阿伏加德罗常数的数值。下列说法正确的是
A.0.1mol·L-1的NaCl溶液中,Na+的数目为0.1NA
B.23 g 金属钠在常温的空气中充分氧化和在氧气中完全燃烧转移电子的数目均为NA
C.7.8g Na2O2中含有的阴、阳离子数目均为0.1NA
D.标准状况下,22.4L水中分子个数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com