
下列有关金属键的相关叙述,正确的是( )
A.金属中的电子属于整块金属
B.金属键是金属离子和自由电子之间存在的强烈的静电吸引作用
C.按熔点逐渐升高的顺序排列的是:Li、Na、Mg
D.固态能导电的单质一定为金属
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
一定条件下向容积为20 L的密闭容器中充入1 mol NO2气体,发生反应2NO2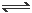 N2O4。反应中测得相关数据如下表所示:
N2O4。反应中测得相关数据如下表所示:
| 反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| 气体相对分子质量 | 46 | 57 | 64 | 69 | 69 | 69 |
(1)此条件下该反应的化学平衡常数Kc=________。(填表达式)
 (2)在50 min末,向容器中加入
(2)在50 min末,向容器中加入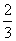 mol NO2,若要保持平衡不发生移动,则应加入N2O4________mol。
mol NO2,若要保持平衡不发生移动,则应加入N2O4________mol。
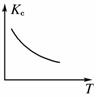
(3)若保持容器体积不发生变化,升高温度,则可得如图图像,据此判断该反应ΔH________0(填“大于”、“小于”或“等于”)。
(4)若在体积不变的情况下,开始充入0.5 mol N2O4,则达到新平衡时N2O4的转化率α=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于有机物的下列说法中正确的是( )
A.溴乙烷和乙烷都是饱和烃
B.甲烷和乙烯都可以与氯气反应
C.苯和甲苯都可被KMnO4酸性溶液氧化
D.氯乙烯可与氢气发生加成反应,溴苯不能与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列指定粒子的个数比不为21的是( )
A.Be2+中的质子数和电子数比
B.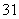 H原子中的中子数和电子数
H原子中的中子数和电子数
C.Na2CO3晶体中阳离子和阴离子个数比
D.BaO2(过氧化钡)固体中阴离子和阳离子个数比
查看答案和解析>>
科目:高中化学 来源: 题型:
有关晶体的叙述中正确的是( )
A.在SiO2晶体中,由Si、O构成的最小单元环中共有8个原子
B.在28 g晶体硅中,含Si—Si共价键个数为4NA
C.金刚石的熔沸点高于晶体硅,是因为C—C键键能小于Si—Si键
D.镁型和铜型金属晶体的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为周期表的一部分,其中的编号代表对应不同的元素。
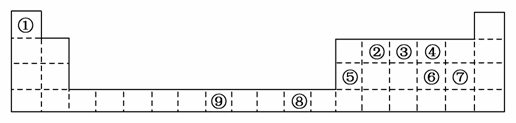
请回答下列问题。
(1)表中属于d区的元素是________(填编号);元素⑧的原子外围电子排布式是________。
(2)③和⑦形成的常见化合物的晶体类型是________;②③④的电负性:________>________>________(用元素符号表示)。判断依据是______________________________,气态氢化物最稳定的是________(写化学式);
(3)某元素的特征电子排布式(价电子排布式)为nsnnpn+1,该元素为周期表中的________(填编号);该元素与元素①形成的化合物X极易溶于水的原因是__________________________。
(4)②③形成一种超硬、耐磨、耐高温的新型无机非金属材料,则其化学式为________________,其熔点比金刚石的__________(填“高”或“低”)。
(5)⑤的氧化物与⑥的最高价氧化物的水化物反应的方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质熔化或汽化时所克服的微粒间的作用力属同种类型的是( )
A.石英和生石灰的熔化 B.晶体硅和晶体硫的熔化
C.钠和铁的熔化 D.碘和氯化铵的汽化
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下的0.1mol·L-1 Na2CO3溶液和0.1mol·L-1的NaHCO3溶液的pH,前者和后者的关系是( )
A.前者大 B.相等
C.前者小 D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
有FeO、Fe2O3的混合物若干克,在足量H2气流中,加热充分反应,冷却后称得剩余固体比原混合物减轻0.8g;将等质量的原混合物与盐酸反应,欲使之完全溶解,需1mol•L﹣1的盐酸的体积至少为( )
|
| A. | 0.05 L | B. | 0.1 L | C. | 0.2 L | D. | 1 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com