
 CO+H2(2分) 氧化(合理即可)
CO+H2(2分) 氧化(合理即可) 2Fe2(SO4)3+2H2SO4(2分)
2Fe2(SO4)3+2H2SO4(2分) CO+H2,在该反应中水是氧化剂。
CO+H2,在该反应中水是氧化剂。 2Fe2(SO4)3+2H2SO4。
2Fe2(SO4)3+2H2SO4。

科目:高中化学 来源:不详 题型:单选题
| A.NO | B.NO2 | C.N2O | D.N2O4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
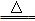 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 PbO2+2Pb(NO3)2+2H2O。铅丹的化学式是 ,此铅丹中铅的化合价是 。由此反应可推测PbO是(填“酸”或“碱”) 性氧化物。
PbO2+2Pb(NO3)2+2H2O。铅丹的化学式是 ,此铅丹中铅的化合价是 。由此反应可推测PbO是(填“酸”或“碱”) 性氧化物。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在3NO2+H2O=2HNO3+NO中,氧化剂和还原剂的质量比为1:2 |
| B.SO2气体使品红溶液褪色,表现了SO2的氧化性 |
| C.浓盐酸和MnO2反应时,浓盐酸中的HCl全部被氧化 |
| D.当7.8 g Na2O2与H2O完全反应时,有0.2 mol电子发生了转移 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成1molCu,转移2mol电子 | B.Cu是氧化产物 |
| C.Cu2S既是氧化剂又是还原剂 | D.氧化剂只有Cu2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.该燃料绿色环保,在燃烧过程中不会造成任何环境污染 |
| B.该反应中N2O4是氧化剂,偏二甲肼是还原剂 |
| C.CO2是氧化产物,N2是还原产物 |
| D.每有0.6 mol N2生成,转移电子数目为2.4NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
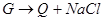 (2)
(2)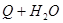 电解
电解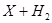
 (4)
(4)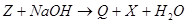
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com