
人类将在未来几十年内逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能与太阳能的转换形态),届时人们将适应“低碳经济”和“低碳生活”。下列说法不正确的是( )
A.煤、石油和天然气都属于碳素燃料
B.发展太阳能经济有助于减缓温室效应
C.太阳能电池可将太阳能直接转化为电能
D.目前研究菠菜蛋白质“发电”不属于太阳能文明
科目:高中化学 来源: 题型:
分析题目中的图表信息,根据信息完成填空。
Ⅰ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
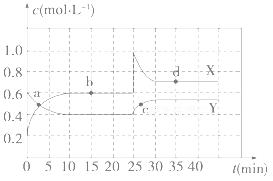
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):
_______________________________________________________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是________________。
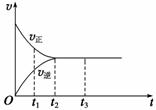
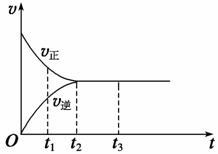 Ⅱ. (3)下图是可逆反应X2+3Y2
Ⅱ. (3)下图是可逆反应X2+3Y2  2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是 。
2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是 。
A.t1时,正反应速率大于逆反应速率;
B.t2时,反应达到限度;
C.t2~t3,反应不再发生;
D.t2~t3,各物质的浓度相等。
Ⅲ.以下是关于化学反应2SO2+O2 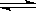 2SO3的两个素材:
2SO3的两个素材:
素材1:某温度和压强下2升容器中,不同时间点测得密闭体系中三种物质的物质的量。
|
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| SO2 | 1 | 0.7 | 0.5 | 0.35 | 0.2 | 0.1 | 0.1 | 0.1 |
| O2 | 0.5 | 0.35 | 0.25 | 0.18 | 0.1 | 0.05 | 0.05 | 0.05 |
| SO3 | 0 | 0.3 | 0.5 | 0.65 | 0.8 | 0.9 | 0.9 | 0.9 |
素材2:反应在不同条件下进行时SO2的转化率:
(SO2的转化率是反应的SO2占起始SO2的百分数,SO2的转化率越大,化学反应的限度越大)
|
| 0.1 MPa | 0.5 MPa | 1 MPa | 10 MPa |
| 400 ℃ | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 ℃ | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 ℃ | 73.7 | 85.8 | 90.0 | 96.4 |
根据以上的两个素材回答问题:
(4)根据素材1中计算20~30 s期间,用二氧化硫表示的化学反应平均速率为________。
(5)根据素材2中分析得到,提高该化学反应限度的途径有:
__________________________________________________________。
(6)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应条件是
________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
验证淀粉水解可生成葡萄糖,进行了下列实验,该实验中操作步骤的排列顺序正确的是
①取少量淀粉加水制成溶液 ②加热煮沸 ③加入Cu(OH)2悬浊液 ④加入几滴稀硫酸 ⑤再加热 ⑥加入NaOH溶液,调PH至碱性
A.④②⑥③⑤ B.①⑤②⑥④③ C.①②④⑤③⑥ D.①④②⑥③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是 ( )。
A.地球上99%的溴元素以溴单质形式存在于海洋中
B.在每升海水中含量低于1 mg的元素称为海水中的微量元素
C.海水是锂元素的一个重要来源
D.世界上生产的镁大部分来自海水
查看答案和解析>>
科目:高中化学 来源: 题型:
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用如图工艺流程生产单质碘。试回答:
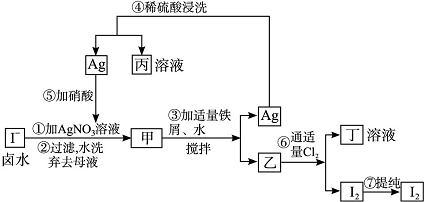
(1)乙、丁中溶质的化学式:乙________;丁________________________________________________________________________。
(2)第④步操作中用稀H2SO4浸洗的目的是________(填写字母编号)。a.除去未反应的NO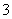
b.除去未反应的I-
c.除去未反应的Fe
d.除去碱性物质
(3)第⑦步操作可供提纯I2的两种方法是__________和________(不要求写具体步骤)。
(4)实验室检验I2的方法是
_____________________________________________________
_____________________ ___________________________________________________。
___________________________________________________。
(5)甲物质见光易变黑,其原因是(用化学方程式表示)________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用NaHCO3和KHCO3组成的混合物样品与某种浓度的盐酸反应进行实验,测得数据如下表:
| 实验编号 | ① | ② | ③ |
| 盐酸体积/mL | 50 | 50 | 50 |
| m(混合物)/g | 9.2 | 26.56 | 36.8 |
| V(CO2)(标准状况)/L | 2.24 | 4.48 | 4.48 |
分析表中数据,下列说法中不正确的是 ( )。
A.由①、②可知:①中的盐酸过量
B.由②、③可知:混合物的质量增加,而气体体积没有变化,说明盐酸已经反应完全
C.所用盐酸的物质的量浓度为0.4 mol·L-1
D.该混合物中NaHCO3的物质的量分数为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是四种常见有机物的比例模型示意图。下列说法正确的是( )
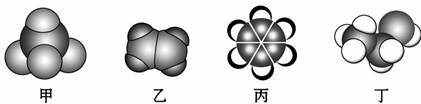
A.甲能使酸性高锰酸钾溶液褪色
B.乙可与溴水发生取代反应使溴水褪色
C.丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键
D.丁在稀硫酸作用下可与乙酸发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
空气吹出法是目前海水提溴的最主要方法之一。其工艺流程如图所示:

(1)步骤④利用了SO2的还原性,反应的离子方程式为
________________________________________________________________________。
(2)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差较大的特点进行分离。所用分离仪器的名称是________。
(3)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过空气吹出、SO2吸收、氯化后再蒸馏,这样操作的意义是_____________________________________。
(4) 根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
观察下列结构简式,回答下列问题:
 |
Ⅰ、乙酸的结构简式为
(1)a的名称是__________。
(2)c的名称是________________。

Ⅱ、
(1)有机物名称是__________________________。
(2)此有机物为烯烃加成的产物,则原来烯烃的结构可能有_______种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com