
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.6gSiO2晶体中含有的硅氧键数目为0.2NA
B.常温下pH=12的Na2CO3溶液中,由水电离出OH-的数目为0.01NA
C.常温常压下,10gD2O含有的质子数、电子数、中子数均为5NA
D.将含0.01molFeCl3的饱和溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
科目:高中化学 来源: 题型:
【题目】ClO2广泛用于水处理、纸浆漂白等。
(1)制备ClO2原料有NaClO2等,产生的ClO2(g)用蒸馏水吸收得到吸收液A。
①ClO2中氯元素的化合价为___。
②NaClO2与盐酸在微热条件下生成ClO2气体(及少量副产物Cl2),写出其反应生成ClO2、NaCl和水的化学方程式:___。
(2)碘量法测定ClO2吸收液A中ClO2和Cl2的浓度的主要实验步骤如下:
步骤1.向锥形瓶中加入50mL蒸馏水、25mL100g·L-1KI溶液(足量),再向其中加入5.00mLClO2吸收液(发生反应:2ClO2+2KI=2KClO2+I2,Cl2+2KI=2KCl+I2)。
步骤2.用0.1000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉溶液,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液6.00mL。
步骤3.向步骤2的溶液中加入5mL2mol·L-1硫酸溶液酸化,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O。
步骤4.重复步骤2操作,第二次滴定又消耗0.1000mol·L-1Na2S2O3溶液20.00mL。
根据上述数据,计算ClO2吸收液A中ClO2和Cl2的浓度___(单位g·L-1,写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中的∣△H∣能表示可燃物的燃烧热的是( )
A.H2(g)+![]() O2(g)=H2O(1)△H=-285.8kJ/mol-1
O2(g)=H2O(1)△H=-285.8kJ/mol-1
B.H2(g)+C12(g)=2HCl(g)△H=-184.6kJ/mol-1
C.2CO(g)+O2(g)=2CO2(g)△H= 一566kJ/mol-1
D.CH4(g)+2O2(g)=2H2O(g)+CO2(g)△H= 一802.3kJ/mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯(![]() )有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
)有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
A. ①②③④⑤ B. ①②⑤⑥ C. ①②④⑤⑥ D. 全部正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如下图,该物质不应有的化学性质是( )
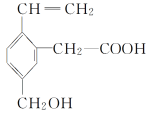
①可燃烧;②可与溴加成;③可使酸性KMnO4溶液褪色;④可与NaHCO3溶液反应;⑤可与NaOH溶液反应;⑥1mol该有机物与Na反应生成2molH2
A.①③B.②⑥C.④⑤D.⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. (CH3)3C-CH=CH2与氢气完全反应后,生成2,2,3-三甲基戊烷
B. 工业上由乙烯制乙醇、苯制环己烷均属于加成反应
C. C5H11Cl的同分异构体有3种
D.  分子中所有碳原子一定在同一平面上
分子中所有碳原子一定在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:

(1)铝灰中氧化铝与硫酸反应的化学方程式为 。
(2)图中“滤渣”的主要成分为 (填化学式)。
(3)加30%的H2O2溶液发生的离子反应方程式为 。
(4)煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)2·12H2O]![]() 2Al2O3+ 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
2Al2O3+ 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。

①集气瓶中收集到的气体是 (填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有 (填化学式)。
③KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是
A.![]() 与
与![]() 组成的混合物中,含有的电子数目为
组成的混合物中,含有的电子数目为![]()
B.![]() (标准状况)
(标准状况)![]() 与足量乙烷反应时,断裂的
与足量乙烷反应时,断裂的![]() 键数目为
键数目为![]()
C.![]() 浓度均为
浓度均为![]() 的
的![]() 、
、![]() 溶液中,
溶液中,![]() 数目前者比后者多
数目前者比后者多![]()
D.![]() [电离方程式:
[电离方程式:![]() ]消耗
]消耗![]() 数目最多为
数目最多为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化剂是化工技术的核心,绝大多数的化工生产需采用催化工艺。
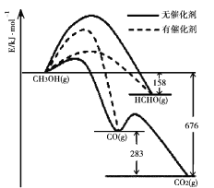
Ⅰ.(1)催化剂的选择性指在能发生多种反应的反应系统中,同一催化剂促进不同反应的程度的比较,实质上是反应系统中目的反应与副反应之间反应速度竞争的表现。如图所示为一定条件下![]() 与
与![]() 发生反应时,生成
发生反应时,生成![]() 、
、![]() 或
或![]() 的能量变化图[反应物
的能量变化图[反应物![]() 和生成物
和生成物![]() 略去]。在有催化剂作用下,
略去]。在有催化剂作用下,![]() 与
与![]() 反应主要生成____(选填“
反应主要生成____(选填“![]() 或
或![]() 或
或![]() ”)。
”)。
(2)2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家哈德·埃特尔,他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论。埃特尔研究的氮气和氢气分子在固体催化剂表面发生的部分变化过程如图所示:

①下列说法不正确的是_________。
A.升高温度可以提高一段时间内![]() 的生产效率
的生产效率
B.图示中的②→③以及后面几个过程均是放热过程
C.此图示中存在![]() 键断裂和
键断裂和![]() 键断裂,以及
键断裂,以及![]() 键的形成过程
键的形成过程
②合成氨工业中,原料气(![]() 、
、![]() 及少量
及少量![]() 、
、![]() 的混合气)在进入合成塔前常用
的混合气)在进入合成塔前常用![]() (醋酸二氨合亚铜,
(醋酸二氨合亚铜,![]() 代表醋酸根)溶液来吸收原料气中的
代表醋酸根)溶液来吸收原料气中的![]() ,其反应是:
,其反应是:![]() ,生产中必须除去原料气中
,生产中必须除去原料气中![]() 的原因是_________;
的原因是_________;![]() 溶液吸收原料气中的
溶液吸收原料气中的![]() 的生产适宜条件应是____________。
的生产适宜条件应是____________。
Ⅱ.氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一,存在较多蓝、绿藻类的酸性水体中存在如有图所示的氮循环,请回答相关问题。

(3)![]() 硝化过程的方程式是
硝化过程的方程式是![]() ,恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是____(填标号)。
,恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是____(填标号)。
A.溶液的![]() 不再改变
不再改变
B.![]() 的消耗速率和
的消耗速率和![]() 的生成速率相等
的生成速率相等
C.溶液中![]() 、
、![]() 、
、![]() 的总物质的量保持不变
的总物质的量保持不变
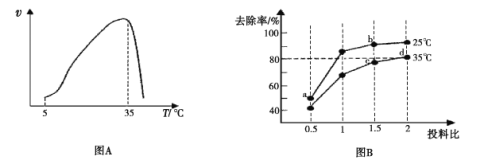
实验测得在其它条件一定时,![]() 硝化反应的速率随温度变化曲线如下图A所示,温度高于35℃时反应速率迅速下降的原因可能是__________________。
硝化反应的速率随温度变化曲线如下图A所示,温度高于35℃时反应速率迅速下降的原因可能是__________________。
(4)亚硝酸盐含量过高对人和动植物都会造成直接或间接的危害,因此要对亚硝酸盐含量过高的废水进行处理。处理亚硝酸盐的方法之一是用次氯酸钠将亚硝酸盐氧化为硝酸盐,反应方程式是![]() 。在25℃和35℃下,分别向
。在25℃和35℃下,分别向![]() 初始浓度为
初始浓度为![]() 的溶液中按不同的投料比
的溶液中按不同的投料比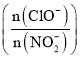 加入次氯酸钠固体(忽略溶液体积的变化),平衡时
加入次氯酸钠固体(忽略溶液体积的变化),平衡时![]() 的去除率和温度、投料比的关系如上图B所示,a、b、c、d四点
的去除率和温度、投料比的关系如上图B所示,a、b、c、d四点![]() 的转化率由小到大的顺序是______,35℃时该反应的平衡常数
的转化率由小到大的顺序是______,35℃时该反应的平衡常数![]() ______(保留三位有效数字)。
______(保留三位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com