
��ľ���к��� ���Ӳ�ľ������ȡ̼��أ������й�ʵ�飮
���Ӳ�ľ������ȡ̼��أ������й�ʵ�飮
(1)������ʵ�������a��������b�����ˣ�c���ܽ⣻d����ȴ�ᾧ��
��ȷ�IJ���˳����______________��
(2)���˺����Һ���������м��ȿɵõ����ξ��壬���ȹ�����Ҫ________________________��Ŀ����_____________________________����������____________________________ʱֹͣ���ȣ�
(3)����ɫ��Ӧ����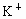 ʱ��ijѧ����������˿��պ
ʱ��ijѧ����������˿��պ ��ĩ��ȴ��պ���ϣ�������Ϊ_____________��ijѧ��պ�˼��η�ĩ�����ھƾ���������ʱ�����Ļ����ǻ�ɫ��������ɫ��������Ϊ__________________��
��ĩ��ȴ��պ���ϣ�������Ϊ_____________��ijѧ��պ�˼��η�ĩ�����ھƾ���������ʱ�����Ļ����ǻ�ɫ��������ɫ��������Ϊ__________________��
 һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
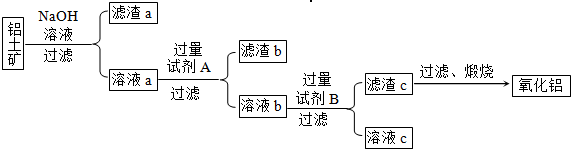
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
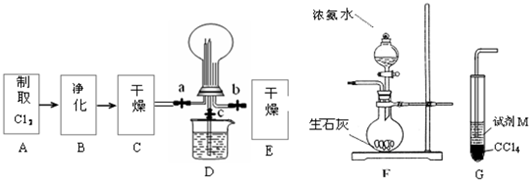
| ||
| ||

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ʵ�鲽�� | Ԥ����������� |
����1��ȡ����������Һע���Թ��У����뼸�ε�����Һ�� |
����Һ�� ��ɫ ��ɫ �������1������������1���������ٽ��в���2 |
����2�� ȡ����������Һע���Թ��� ȡ����������Һע���Թ��� ���뼸��1.0mol?L-1H2SO4��Һ�ͼ���3%H2O2��Һ ���뼸��1.0mol?L-1H2SO4��Һ�ͼ���3%H2O2��Һ �ٵ��뼸�ε�����Һ���� �ٵ��뼸�ε�����Һ���� |
����Һ����ɫ�������2��������Ӧ�����ӷ���ʽΪ 2I-+H2O2+2H+=I2+2H2O 2I-+H2O2+2H+=I2+2H2O ��������2���������ٽ��в���3 |
����3�� ȡ����������Һע���Թ��� ȡ����������Һע���Թ��� ���뼸��1.0mol?L-1NaHSO3��Һ ���뼸��1.0mol?L-1NaHSO3��Һ �ٵ��뼸�ε�����Һ���� �ٵ��뼸�ε�����Һ���� |
����Һ����ɫ�������3���� ����Һ����ɫ�������3���� ������3������ ������3������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������������ ���ͣ�058
��ľ���к��� ���Ӳ�ľ������ȡ̼��أ������й�ʵ�飮
���Ӳ�ľ������ȡ̼��أ������й�ʵ�飮
(1)������ʵ�������a��������b�����ˣ�c���ܽ⣻d����ȴ�ᾧ��
��ȷ�IJ���˳����______________��
(2)���˺����Һ���������м��ȿɵõ����ξ��壬���ȹ�����Ҫ________________________��Ŀ����_____________________________����������____________________________ʱֹͣ���ȣ�
(3)����ɫ��Ӧ����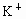 ʱ��ijѧ����������˿��պ
ʱ��ijѧ����������˿��պ ��ĩ��ȴ��պ���ϣ�������Ϊ_____________��ijѧ��պ�˼��η�ĩ�����ھƾ���������ʱ�����Ļ����ǻ�ɫ��������ɫ��������Ϊ__________________��
��ĩ��ȴ��պ���ϣ�������Ϊ_____________��ijѧ��պ�˼��η�ĩ�����ھƾ���������ʱ�����Ļ����ǻ�ɫ��������ɫ��������Ϊ__________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com