
ЁОЬтФПЁПЯТБэЪЧдЊЫижмЦкБэЕФвЛВПЗж,БэжаЫљСаЕФзжФИЗжБ№ДњБэФГвЛЛЏбЇдЊЫиЁЃ
A | ||||||||
B | C | |||||||
D | E | F | ||||||
ЛиД№ЯТСаЮЪЬтЃК
(1)дЊЫиBЕФдЊЫиЗћКХЮЊ______ЃЌЫќдкдЊЫижмЦкБэжаЕФЮЛжУЪЧ__________ЁЃ
(2)DЕФМђЕЅРызгЕФНсЙЙЪОвтЭМЮЊ_________ЃЌЫќЕФзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяжаКЌгаЕФЛЏбЇМќга_____________ЃЌDЕЅжЪгыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЮЊ____________________ЁЃ
(3)гУЕчзгЪНБэЪОEF2ЕФаЮГЩЙ§ГЬ_________________________________ЁЃ
(4)гЩA2ЁЂC2ЙЙГЩМюадШМСЯЕчГиЃЌдђИУЕчГиЕФИКМЋЗДгІЗНГЬЪНЮЊ_______________ЃЌИУЕчГиЙЄзїЙ§ГЬжаУПЭЈЙ§2molЕчзгЫљашвЊЕФC2ЬхЛ§ЮЊ___________(БъзМзДПі)ЁЃ
(5)CКЭDдкИпЮТЬѕМўЯТаЮГЩЛЏКЯЮяЕФЛЏбЇЪНЮЊ_________ЃЌгыЖўбѕЛЏЬМЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_________________________ЁЃ
ЁОД№АИЁП N ЕкЖўжмЦкЕкЂѕAзх  РызгМќЁЂ(МЋад)ЙВМлМќ 2Na+2H2O
РызгМќЁЂ(МЋад)ЙВМлМќ 2Na+2H2O![]() 2NaOH+ H2Ёќ
2NaOH+ H2Ёќ ![]() H2 ЈC 2eЃ+ 2OHЃ
H2 ЈC 2eЃ+ 2OHЃ![]() 2H2O 11.2L Na2O2 2Na2O2 +2CO2
2H2O 11.2L Na2O2 2Na2O2 +2CO2![]() 2Na2CO3+O2
2Na2CO3+O2
ЁОНтЮіЁПИљОндЊЫидкжмЦкБэжаЕФЮЛжУПЩжЊЃЌAЮЊHЃЛBЮЊNЃЛCЮЊOЃЛDЮЊNaЃЛEЮЊMgЃЛFЮЊClЃЛ
(1) BЮЊNЃЌдкдЊЫижмЦкБэжаЮЛгкЕкЖўжмЦкЕкЂѕAзхЃЌЙЪД№АИЮЊЃКNЃЛЕкЖўжмЦкЕкЂѕAзхЃЛ
(2) DЮЊNaЃЌФЦРызгЕФНсЙЙЪОвтЭМЮЊ ЃЌЧтбѕЛЏФЦЪєгкРызгЛЏКЯЮяЃЌЦфжаКЌгаЕФЛЏбЇМќгаРызгМќЁЂ(МЋад)ЙВМлМќЃЌФЦгыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЮЊ2Na+2H2O=2NaOH+ H2ЁќЃЌЙЪД№АИЮЊЃК
ЃЌЧтбѕЛЏФЦЪєгкРызгЛЏКЯЮяЃЌЦфжаКЌгаЕФЛЏбЇМќгаРызгМќЁЂ(МЋад)ЙВМлМќЃЌФЦгыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЮЊ2Na+2H2O=2NaOH+ H2ЁќЃЌЙЪД№АИЮЊЃК ЃЛРызгМќЁЂ(МЋад)ЙВМлМќЃЛ2Na+2H2O=2NaOH+ H2ЁќЃЛ
ЃЛРызгМќЁЂ(МЋад)ЙВМлМќЃЛ2Na+2H2O=2NaOH+ H2ЁќЃЛ
(3)гУЕчзгЪНБэЪОMgCl2ЕФаЮГЩЙ§ГЬЮЊ![]() ЃЌЙЪД№АИЮЊЃК
ЃЌЙЪД№АИЮЊЃК![]() ЃЛ
ЃЛ
(4)гЩH2ЁЂO2ЙЙГЩМюадШМСЯЕчГиЃЌЭЈШыЧтЦјЕФЮЊИКМЋЃЌИКМЋЗДгІЗНГЬЪНЮЊH2 ЈC 2eЃ+ 2OHЃ= 2H2OЃЌИУЕчГиЙЄзїЙ§ГЬжаУПЭЈЙ§2molЕчзгЫљашвЊЕФO2ЕФЮяжЪЕФСПЮЊ![]() =0.5molЃЌдкБъзМзДПіЯТЕФЬхЛ§ЮЊ0.5molЁС22.4L/mol=11.2LЃЌЙЪД№АИЮЊЃКH2 ЈC 2eЃ+ 2OHЃ= 2H2OЃЛ 11.2LЃЛ
=0.5molЃЌдкБъзМзДПіЯТЕФЬхЛ§ЮЊ0.5molЁС22.4L/mol=11.2LЃЌЙЪД№АИЮЊЃКH2 ЈC 2eЃ+ 2OHЃ= 2H2OЃЛ 11.2LЃЛ
(5)бѕЦјКЭФЦдкИпЮТЬѕМўЯТЗДгІЩњГЩЙ§бѕЛЏФЦЃЌЙ§бѕЛЏФЦгыЖўбѕЛЏЬМЗДгІЕФЛЏбЇЗНГЬЪНЮЊ2Na2O2 +2CO2= 2Na2CO3+O2ЃЌЙЪД№АИЮЊЃКNa2O2ЃЛ2Na2O2 +2CO2= 2Na2CO3+O2ЁЃ


 КЎМйДДаТаЭзджїбЇЯАЕкШ§бЇЦкКЎМйЯЮНгЯЕСаД№АИ
КЎМйДДаТаЭзджїбЇЯАЕкШ§бЇЦкКЎМйЯЮНгЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПNH3ЪЧвЛжжживЊЕФЛЏЙЄдСЯЃЌдкЩњВњЁЂЩњЛюжагУЭОЙуЗКЁЃ
ЃЈ1ЃЉвбжЊЃК
ЙВМлМќ | МќФм/ kJЁЄmol-1 |
HЈDH | 436 |
NЁдN | 946 |
NЈDH | 391 |
зЂЃКВ№ПЊЦјЬЌЮяжЪжа1 molФГжжЙВМлМќашвЊЮќЪеЕФФмСПЃЌОЭЪЧИУЙВМлМќЕФМќФмЁЃ
N2 (g)ЃЋ3 H2 (g)![]() 2 NH3 (g) H =____kJЁЄmol-1
2 NH3 (g) H =____kJЁЄmol-1
ЃЈ2ЃЉвЛЖЈЮТЖШЯТЃЌЯђКуШнЕФУмБеШнЦїжаГфШыN2КЭH2ЗЂЩњЗДгІЃКN2 ЃЋ3H2 ![]() 2NH3ЃЌВтЕУИїзщЗжХЈЖШЫцЪБМфБфЛЏШчЭМ1ЫљЪОЁЃ
2NH3ЃЌВтЕУИїзщЗжХЈЖШЫцЪБМфБфЛЏШчЭМ1ЫљЪОЁЃ
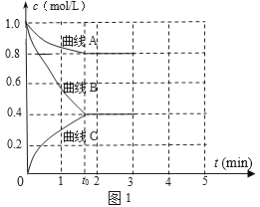
ЂйБэЪОc(N2)ЕФЧњЯпЪЧ__ЃЈЬюЁАЧњЯпAЁБЁЂЁАЧњЯпBЁБЛђЁАЧњЯпCЁБЃЉЁЃ
Ђк0ЁЋt0ЪБгУH2БэЪОЗДгІЫйТЪv(H2)____molЁЄL-1ЁЄmin-1ЁЃ
ЂлЯТСаФмЫЕУїИУЗДгІДяЕНЦНКтЕФЪЧ____ЁЃ
aЃЎЛьКЯЦјЬхЕФбЙЧПВЛдйБфЛЏ
bЃЎ2c(H2)= 3c(NH3)
cЃЎЛьКЯЦјЬхЕФжЪСПВЛдйБфЛЏ
dЃЎNH3ЕФЬхЛ§ЗжЪ§ВЛдйБфЛЏ
ЃЈ3ЃЉЧБЭЇжаЪЙгУЕФвКАБ-вКбѕШМСЯЕчГиЙЄзїдРэШчЭМ2ЫљЪОЃК
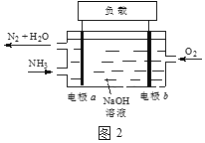
ЂйЕчМЋbУћГЦЪЧ____ЁЃ
ЂкЕчНтжЪШмвКжаOH-РызгЯђ____вЦЖЏЃЈЬюЁАЕчМЋaЁБЛђЁАЕчМЋbЁБЃЉЁЃ
ЂлЕчМЋaЕФЕчМЋЗДгІЪНЮЊ____ЁЃ
ЃЈ4ЃЉПЩЭЈЙ§NH3гыNaClOЗДгІРДжЦЕУЛ№М§ШМСЯыТЃЈN2H4ЃЉЁЃИУЗДгІЕФЛЏбЇЗДгІЗНГЬЪНЪЧ____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЖдЗжзгМАЦфаджЪЕФНтЪЭжаЃЌВЛе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
A. ЕтвзШмгкЫФТШЛЏЬМЃЌМзЭщФбШмгкЫЎЖМПЩгУЯрЫЦЯрШмдРэНтЪЭ
B. ШщЫс[CH3CH(OH)COOH]жаДцдквЛИіЪжадЬМдзг
C. вбжЊЫсадЃКH3PO4ЃОHClOЃЌЪЧвђЮЊH3PO4Зжзгжага1ИіЗЧєЧЛљбѕдзгЖјHClOЮЊ0
D. аэЖрЙ§ЖЩН№ЪєРызгЖдЖржжХфЬхОпгаКмЧПЕФНсКЯСІЃЌвђЖјЃЌжЛгаЙ§ЖЩН№ЪєВХФмаЮГЩХфКЯЮя
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПБНМзЫсФЦЃЈ![]() ЃЌЫѕаДЮЊNaAЃЉПЩгУзївћСЯЕФЗРИЏМСЃЌбаОПБэУїБНМзЫсЃЈHAЃЉЕФвжОњФмСІЯджјИпгкAЃЃЌвбжЊ25ЁцЪБЃЌHAЕФKa=6.25ЁС10Ѓ5ЃЌH2CO3ЕФKa1=4.7ЁС10Ѓ7ЃЌKa2=4.90ЁС10Ѓ11ЃЌдкЩњВњЬМЫсвћСЯЕФЙ§ГЬжаГ§СЫЬэМгNaAЭтЃЌЛЙашМгбЙГфШыCO2ЦјЬхЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЮТЖШЮЊ25ЁцЃЌВЛПМТЧвћСЯжаЦфЫћГЩЗжЃЉ
ЃЌЫѕаДЮЊNaAЃЉПЩгУзївћСЯЕФЗРИЏМСЃЌбаОПБэУїБНМзЫсЃЈHAЃЉЕФвжОњФмСІЯджјИпгкAЃЃЌвбжЊ25ЁцЪБЃЌHAЕФKa=6.25ЁС10Ѓ5ЃЌH2CO3ЕФKa1=4.7ЁС10Ѓ7ЃЌKa2=4.90ЁС10Ѓ11ЃЌдкЩњВњЬМЫсвћСЯЕФЙ§ГЬжаГ§СЫЬэМгNaAЭтЃЌЛЙашМгбЙГфШыCO2ЦјЬхЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЮТЖШЮЊ25ЁцЃЌВЛПМТЧвћСЯжаЦфЫћГЩЗжЃЉ
A. ЯрБШгкЮДГфCO2ЕФвћСЯЃЌЬМЫсвћСЯЕФвжОњФмСІНЯЕЭ
B. ЬсИпCO2ГфЦјбЙСІЃЌвћСЯжаc(AЃ)ВЛБф
C. ЬМЫсвћСЯжаИїжжСЃзгЕФХЈЖШЙиЯЕЮЊЃКc(H+)=c(HCO3Ѓ)+c(CO32Ѓ)+c(OHЃ)Ѓc(HA)
D. ЕБpHЮЊ5.0ЪБЃЌвћСЯжа![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
A.ФІЖћЪЧвЛИіЛљБОЮяРэСПЃЌБэЪОЮяжЪЫљКЌСЃзгЕФЖрЩй
B.1molЧтжаКЌга2molЧтдзгКЭ2molЕчзг
C.1molH2OЕФжЪСПЕШгкNAИіH2OжЪСПЕФзмКЭЃЈNAБэЪОАЂЗќМгЕТТоГЃЪ§ЃЉ
D.ФІЖћБэЪОЮяжЪЕФЪ§СПЕФЕЅЮЛ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏбЇгыЩњЛюУмЧаЯрЙиЁЃЯТСаЩњЛюжаГЃМћЮяжЪЕФЫзУћгыЛЏбЇЪНЯрЖдгІЕФЪЧЃЈ ЃЉ
A.ЫеДђЁЊЁЊNaHCO3
B.ЕЈЗЏЁЊЁЊZnSO4
C.ОЦОЋЁЊЁЊC2H5OH
D.ЩњЪЏЛвЁЊЁЊCa(OH)2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЮяжЪжаЃЌМШФмЕМЕчгжЪєгкЧПЕчНтжЪЕФвЛзщЮяжЪЪЧЃЈ ЃЉ
A.ШлШкMgCl2ЁЂШлШкNaOH
B.вКАБЁЂЪЏЛвЫЎ
C.ЪЏФЋЁЂЪГДз
D.ЯЁСђЫсЁЂесЬЧ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПДЮСзЫс(H3PO2)ЪЧвЛдЊжаЧПЫсЃЌОпгаНЯЧПЛЙдадЃЌЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ( )
A. ДЮСзЫсЕФЕчРыЗНГЬЪНЮЊЃКH3PO2=H++H2PO2-
B. NaH2PO2ЪЧДЮСзЫсЕФе§бЮЃЌЦфЫЎШмвКГЪжаад
C. АзСзгыЧтбѕЛЏФЦШмвКЗДгІПЩЕУДЮСзЫсбЮЃЌЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК
P4+9NaOH=3Na2PO2+PH3Ёќ+3H2O
D. РћгУ(H3PO2)НјааЛЏбЇЖЦвјЗДгІжаЃЌ1mol H3PO2зюЖрЛЙд4mol Ag+Рызг
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com