
| A. | 该反应为吸热反应 | |
| B. | 该反应中,SO2为还原剂 | |
| C. | 1 mol H2S中含有的共价键的数目为3 mol | |
| D. | 常温下,H2S的还原性强于S的还原性 |
分析 A.反应能自发进行,应满足△H-T•△S<0;
B.反应SO2中S元素的化合价降低;
C.1个H2S中含有2个共价键;
D.氧化还原反应中还原剂的还原性大于还原产物的还原性.
解答 解:A.反应能自发进行,应满足△H-T•△S<0,已知2H2S(g)+SO2(g)═3S(s)+2H2O(l)的熵变小于零,则△H<0,故该反应为放热反应,故A错误;
B.反应SO2中S元素的化合价降低,所以SO2为氧化剂,故B错误;
C.1个H2S中含有2个共价键,则1 mol H2S中含有的共价键的数目为2mol,故C错误;
D.氧化还原反应中还原剂的还原性大于还原产物的还原性,H2S为还原剂,S还原产物,所以H2S的还原性强于S的还原性,故D正确.
故选D.
点评 本题考查了反应自发性的判断、氧化还原反应、共价键的类型,根据元素化合价变化和共价键的分类来分析解答,注意反应能自发进行,应满足△H-T•△S<0,为易错点,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| A | B | C |
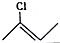 |  |  |
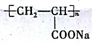 .
.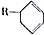 结构,D可能的结构有4种;写出
结构,D可能的结构有4种;写出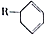 和Cl2发生1,4-加成反应的化学方程式:
和Cl2发生1,4-加成反应的化学方程式: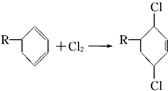 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在 pH 为 6.37 及 10.25 时,溶液中 c(H2CO3)=c(HCO3-)=c(CO32-) | |
| B. | 反应 HCO3-+H2O?H2CO3+OH-的平衡常数为 10-7.63 | |
| C. | 0.1 mol•L-1NaHC2O4溶液中 c(HC2O4-)+2c(C2O42-)+c(H2C2O4)=0.1 mol•L-1 | |
| D. | 往 Na2CO3溶液中加入少量草酸溶液,发生反应:CO32-+H2C2O4=HCO3-+HC2O4- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
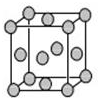 已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.
已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有一个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ•mol-1,I2=1817kJ•mol-1, I3=2745kJ•mol-1,I4=11575kJ•mol-1 |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
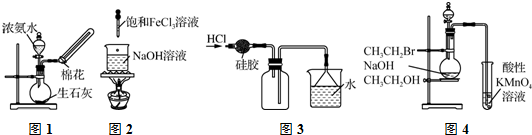
| A. | 利用图1所示装置制取少量NH3 | |
| B. | 利用图2所示装置制备Fe(OH)3胶体 | |
| C. | 利用图3所示装置收集HCl | |
| D. | 利用图4所示装置检验是否生成乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
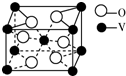 钒及其化合物非常丰富.钒可用于生产合金钢、航天用的钒钛合金及化工催化剂等.
钒及其化合物非常丰富.钒可用于生产合金钢、航天用的钒钛合金及化工催化剂等.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 晶胞是晶体结构中的基本结构单元 | |
| B. | 根据晶体的不同,晶胞可以是多种形状的几何体 | |
| C. | 晶胞一般都是平行六面体 | |
| D. | 晶胞都是正八面体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加少量盐酸 | B. | 加热 | ||
| C. | 加少量醋酸钠晶体 | D. | 加少量NaOH晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com