
【题目】常温常压下,在四支相同的试管中,分别装入等物质的量混合的两种气体。混合气体具体组成如下:
试管编号 | 1 | 2 | 3 | 4 |
混合气体组成 | Cl2、SO2 | NO2、O2 | NO、O2 | NH3、N2 |
将四支试管迅速同时倒立于水槽中,至液面稳定后,水面上升高度由大到小正确的是( )
A.1>2>3>4B.3>1>4>2
C.4>2>3>1D.1>3>2>4
【答案】D
【解析】
(1)3NO2+H2O=2HNO3+NO,2NO+O2=2NO2,将第一个方程式×2+第二个方程式可得出新的方程式:4NO2+O2+2H2O=4HNO3;
(2)2NO+O2=2NO2,3NO2+H2O=2HNO3+NO,将第一个方程式×3+第二个方程式×2可得出新的方程式:4NO+3O2+2H2O=4HNO3。
假设试管体积为2,则两种气体初始体积都为1,试管总高度为2,则:
试管1:Cl2+SO2+2H2O=2HCl+H2SO4,1体积氯气和1体积二氧化硫恰好完全反应,气体体积变为0,液体充满试管,所以水面上升的高度=1+1=2;
试管2:4NO2+O2+2H2O=4HNO3,当n(NO2):n(O2)=4:1时两者恰好完全反应,现在n(NO2):n(O2)=1:1,氧气过量,1体积二氧化氮消耗完,同时消耗氧气![]() 体积,所以水面上升了的高度=(1+
体积,所以水面上升了的高度=(1+![]() )=
)=![]() ;
;
试管3:4NO+3O2+2H2O=4HNO3,当n(NO):n(O2)=4:3时两者恰好完全反应,现在n(NO):n(O2)=1:1=3:3,氧气过量,1体积一氧化氮消耗完,同时消耗氧气![]() 体积,所以水面上升了的高度=(1+
体积,所以水面上升了的高度=(1+![]() )=
)=![]() ;
;
试管4:1体积氨气溶于水,1体积氮气剩余,所以水面上升了的高度=1;
综上所述:水面上升高度由大到小为:1>3>2>4。
答案选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某种苯的同系物0.1mol 在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,使浓硫酸增重9g,氢氧化钠溶液增重35.2g。实践中可根据核磁共振氢谱(PMR)上观察到氢原子给出的峰值情况,确定有机物的结构。此含有苯环的有机物,在PMR谱上峰给出的稳定强度仅有四种,它们分别为:①3∶1∶1②1∶1∶2∶6③3∶2④3∶2∶2∶2∶1,请分别推断出其对应的结构:①_______;②_________________;③___________;④___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂废水中含5.00×10-3mol·L-1的![]() ,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料
,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料![]() (
(![]() 的化合价依次为+3、+2),设计了如下实验流程:
的化合价依次为+3、+2),设计了如下实验流程:
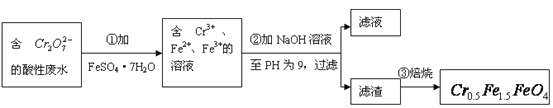
(1)第①步反应的离子方程式是_________________________________________________;
(2)第②步中用pH试纸测定溶液pH的操作是:
______________________________________________________________________________;
(3)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有______________________;
(4)欲使1L该废水中的![]() 完全转化为
完全转化为![]() 。理论上需要加入__________g FeSO4·7H2O。
。理论上需要加入__________g FeSO4·7H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。已知反应:
①CH4 (g) +2O2 (g) = CO2 (g) +2H2O(l) ΔH1 = a kJ mol-1
②CH4(g) + 2O2 (g) = CO2 (g) +2H2O(g) ΔH2 = bkJ mol-1
其他数据如下表所示,下列说法正确的是
化学键 | C=O | C—H | O—H | O=O |
键能/(kJ mol-1) | 798 | 413 | 463 | x |
A.ΔH1 < ΔH2
B.H2O(g) = H2O(1) ΔH=(a-b)kJ mol -1
C.当有4NA个O-H键生成时,反应放出的热量为a kJ
D.上文中x =![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R均为短周期元素(原子序数Y<X<R<Q<Z)。25℃时,其最高价氧化物的水化物溶液(浓度均为0.001mol/L)的pH和原子半径的关系如图所示。下列说法中正确的是( )
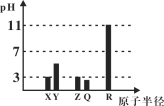
A.X和R的简单离子半径:X < R
B.Z、Q的气态氢化物的稳定性:Z > Q
C.Z的最高价氧化物对应水化物的化学式为HZO3
D.上述五种元素中有两种元素是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.按系统命名法,化合物![]() 的名称为2,4-二乙基-6-丙基辛烷
的名称为2,4-二乙基-6-丙基辛烷
B.若两种二肽互为同分异构体,则二者的水解产物一定不相同
C.醋酸和硬脂酸互为同系物,C2H6和C9H20也一定互为同系物
D.1mol某有机物的结构简式为 通过消去反应脱去1molHCl时,能得到5种不同产物(不考虑立体异构)
通过消去反应脱去1molHCl时,能得到5种不同产物(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭被人们誉为黑色的“金子”,它是人类使用的主要能源之一。为了提高煤的利用率,减少有害气体的排放,人们采取了各式各样的方法。
(1)煤的气化和液化可能提高煤的利用率。煤的气化技术的主要产物是___________。煤的液化技术又分为直接液化和间接氧化.将煤隔绝空气加强热得到焦炉气、煤焦油及焦炭等产品的技术称为___________。
(2)煤在燃烧前、后及燃烧过程中均可采取措施减少有害气体的排放.
①在燃烧前,可以采用微生物脱硫技术.原理如下:
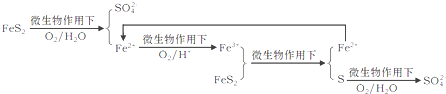
上述过程中Fe2+的作用为________________。写出Fe2+![]() Fe3+的离子方程式________________。
Fe3+的离子方程式________________。
②煤在燃烧时,进行脱硫处理,常采用________燃烧技术,在把煤和脱硫剂加入锅炉燃烧室,使煤与空气在流化过程中充分混合、燃烧,起到固硫作用.常用脱硫剂的主要化学成分为_______(填化学式)。
③煤在燃烧后,烟气净化常采用除尘技术和脱硫、脱硝技术.湿法脱硫、脱硝技术中将烟气通入_________设备,用石灰水淋洗。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生探究小组将一批废弃的电子线路板简单处理后,得到含71%Cu、20%Al、5%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜晶体的路线:

已知:Cu+4HNO3(浓)=Cu(NO3)2+2H2O+2NO2↑
回答下列问题:
(1)滤渣1的主要成分为___。
(2)第②步加入H2O2目的是将Fe2+氧化成Fe3+,其离子方程式为___;使用H2O2作为氧化剂的优点是___。
(3)用第③步所得CuSO4·5H2O晶体加热制备无水CuSO4的瓷质主要仪器___。
(4)由滤渣2制取Al2(SO4)3·18H2O,探究小组设计了三种方案:

上述三种方案中,可行方案是___,其中不可行方案的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有100mLHNO3溶液的烧杯中加入一定量的Cu、Al合金(还原产物为NO ),充分反应后向溶液中加入lmol/L的NaOH溶液,产生沉淀的质量与所加溶液的体积的关系如下图所示。则原HNO3溶液的物质的最浓度是

A. 0.4mol/L B. 0.45mol/L C. 0.525mol/L D. 0.625mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com