
ЁОЬтФПЁПФГбаОПаЁзщФтКЯГЩШОСЯXКЭвНвЉжаМфЬхYЁЃ

вбжЊЃК
![]()
CH3CH2Cl![]() CH3CH2CNCH3CH2COOH
CH3CH2CNCH3CH2COOH
ЃЈ1ЃЉЯТСаЫЕЗЈе§ШЗЕФЪЧ______
AЃЎЛЏКЯЮяAФмгыFeCl3ШмвКЗЂЩњЯдЩЋЗДгІBЃЎЛЏКЯЮяEОпгаШѕМюад
CЃЎЛЏКЯЮяXФмЗЂЩњМгГЩЁЂШЁДњЁЂЛЙдЗДгІ
DЃЎЛЏКЯЮяYЕФЗжзгЪНЮЊC20H23NO4
ЃЈ2ЃЉЛЏКЯЮяCЕФНсЙЙМђЪН______
ЃЈ3ЃЉаДГіD+EЁњXЕФЛЏбЇЗДгІЗНГЬЪН______
ЃЈ4ЃЉаДГіЭЌЪБЗћКЯЯТСаЬѕМўЕФBЕФЭЌЗжвьЙЙЬхЕФНсЙЙМђЪН______
1H-NMRЦзКЭIRЦзМьВтБэУїЃК
ЂйЗжзгжага4жжЛЏбЇЛЗОГВЛЭЌЕФЧтдзгЃЛ
ЂкЗжзгжаКЌгаБНЛЗЁЂМзбѕЛљЃЈ-OCH3ЃЉЃЌ-CH2Cl
ЃЈ5ЃЉЧыЩшМЦвдБНКЭввЯЉЮЊдСЯжЦБИ ЕФКЯГЩТЗЯпЃЈгУСїГЬЭМБэЪОЃЌЮоЛњЪдМСШЮбЁЃЉЁЃКЯГЩТЗЯпСїГЬЭМЪОР§ШчЯТЃКCH3CH2OHCH3CHOCH3COOH______________
ЕФКЯГЩТЗЯпЃЈгУСїГЬЭМБэЪОЃЌЮоЛњЪдМСШЮбЁЃЉЁЃКЯГЩТЗЯпСїГЬЭМЪОР§ШчЯТЃКCH3CH2OHCH3CHOCH3COOH______________
ЁОД№АИЁПBC 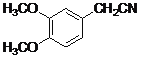

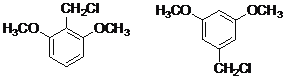
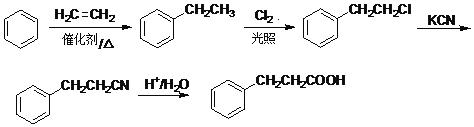
ЁОНтЮіЁП
ЃЈ1ЃЉAЃЎЛЏКЯЮяAЮЊ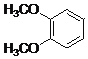 ЃЌУЛгаЗгєЧЛљЃЌВЛФмгыFeCl3ШмвКЗЂЩњЯдЩЋЗДгІЃЌЙЪAДэЮѓЃЛ
ЃЌУЛгаЗгєЧЛљЃЌВЛФмгыFeCl3ШмвКЗЂЩњЯдЩЋЗДгІЃЌЙЪAДэЮѓЃЛ
BЃЎЛЏКЯЮяEЮЊ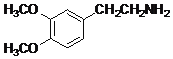 ЃЌКЌгаАБЛљЃЌОпгаШѕМюадЃЌЙЪBе§ШЗЃЛ
ЃЌКЌгаАБЛљЃЌОпгаШѕМюадЃЌЙЪBе§ШЗЃЛ
CЃЎЛЏКЯЮяXКЌгаБНЛЗЃЌФмгыЧтЦјЗЂЩњМгГЩЗДгІЃЌвВЪєгкЛЙдЗДгІЃЌКЌгаѕЃАЗМќЕШЃЌПЩвдЗЂЩњЫЎНтЗДгІЃЌЫЎНтЗДгІЪєгкШЁДњЗДгІЃЌЙЪCе§ШЗЃЛ
DЃЎЛЏКЯЮяYЕФЗжзгЪНЮЊC20H25NO5ЃЌЙЪDДэЮѓЃЛ
ЙЪбЁBCЃЛ
ЃЈ2ЃЉЛЏКЯЮяCЕФНсЙЙМђЪНЮЊЃК ЃЛ
ЃЛ
ЃЈ3ЃЉD+EЁњXЕФЛЏбЇЗДгІЗНГЬЪНЮЊ ЃЛ
ЃЛ
ЃЈ4ЃЉЭЌЪБЗћКЯЯТСаЬѕМўЕФBЃЈ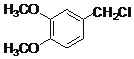 ЃЉЕФЭЌЗжвьЙЙЬхЃКЂйЗжзгжага4жжЛЏбЇЛЗОГВЛЭЌЕФЧтдзгЃЌЂкЗжзгжаКЌгаБНЛЗЁЂМзбѕЛљЃЈ-OCH3ЃЉЃЌ-CH2ClЃЌЗћКЯЬѕМўЕФЭЌЗжвьЙЙЬхгаЃК
ЃЉЕФЭЌЗжвьЙЙЬхЃКЂйЗжзгжага4жжЛЏбЇЛЗОГВЛЭЌЕФЧтдзгЃЌЂкЗжзгжаКЌгаБНЛЗЁЂМзбѕЛљЃЈ-OCH3ЃЉЃЌ-CH2ClЃЌЗћКЯЬѕМўЕФЭЌЗжвьЙЙЬхгаЃК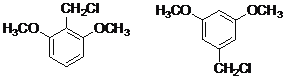 ЃЛ
ЃЛ
ЃЈ5ЃЉБНгыввЯЉЗЂЩњМгГЩЗДгІЩњГЩ![]() ЃЌШЛКѓдкЙтееЬѕМўЯТЗДгІЩњГЩ
ЃЌШЛКѓдкЙтееЬѕМўЯТЗДгІЩњГЩ![]() ЃЌдйгыKCNЗЂЩњШЁДњЗДгІЩњГЩ
ЃЌдйгыKCNЗЂЩњШЁДњЗДгІЩњГЩ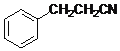 ЃЌзюКѓдкЫсадЬѕМўЯТЫЎНтЩњГЩ
ЃЌзюКѓдкЫсадЬѕМўЯТЫЎНтЩњГЩ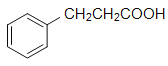 ЃЌКЯГЩТЗЯпСїГЬЭМЮЊЃК
ЃЌКЯГЩТЗЯпСїГЬЭМЮЊЃК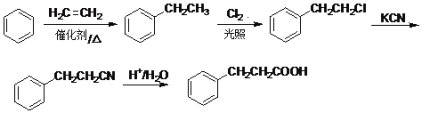 ЁЃ
ЁЃ


 УћаЃПЮЬУЯЕСаД№АИ
УћаЃПЮЬУЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПХфжЦвјАБШмвКВйзїШчЭМЫљЪОЃЌЯТСаЫЕЗЈДэЮѓЕФЪЧ( )
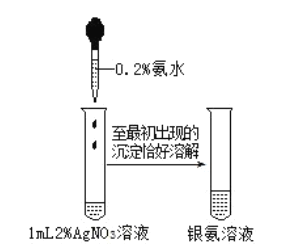
вбжЊЃК![]() ЃЌ
ЃЌ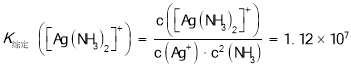
A.жЦЕУЕФвјАБШмвКПЩгУгкЛЙдадЬЧЕФМьбщ
B.![]() жаКЌга
жаКЌга![]() Иі
Иі![]() Мќ
Мќ
C.вјАБШмвКВЛФмГЄЦкДцЗХЃЌашвЊЯжгУЯжХф
D.![]() ЙЬЬхПЩШмгкАБЫЎЕУЕНвјАБШмвК
ЙЬЬхПЩШмгкАБЫЎЕУЕНвјАБШмвК
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
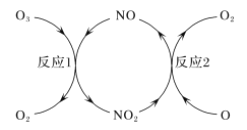
ЁОЬтФПЁПгааЇШЅГ§ДѓЦјжаЕФNOxЃЌБЃЛЄГєбѕВуЃЌЪЧЛЗОГБЃЛЄЕФживЊПЮЬтЁЃ
(1)дкУЛгаNOxДпЛЏЪБЃЌO3ЕФЗжНтПЩЗжЮЊвдЯТСНВНЗДгІНјааЃЛ
ЂйO3=O+O2 (Т§) ЂкO+O3=2O2 (Пь)
ЕквЛВНЕФЫйТЪЗНГЬЮЊv1=k1c(O3)ЃЌЕкЖўВНЕФЫйТЪЗНГЬЮЊv2=k2c(O3)ЁЄc(O)ЁЃЦфжаOЮЊЛюадбѕдзгЃЌЫќдкЕквЛВНТ§ЗДгІжаЩњГЩЃЌШЛКѓгжКмПьЕФдкЕкЖўВНЗДгІжаЯћКФЃЌвђДЫЃЌЮвУЧПЩвдШЯЮЊЛюадбѕдзгБфЛЏЕФЫйТЪЮЊСуЁЃЧыгУk1ЁЂk2зщГЩЕФДњЪ§ЪНБэЪОc(O)=____________ЁЃ
(2)NOзіДпЛЏМСПЩвдМгЫйГєбѕЗДгІЃЌЦфЗДгІЙ§ГЬШчЭМЫљЪОЃК
вбжЊЃКO3(g)+O(g)=2O2(g) ІЄH=Ѓ143 kJ/mol
ЗДгІ1ЃКO3(g)+NO(g)=NO2(g)+O2(g) ІЄH1=Ѓ200.2 kJ/molЁЃ
ЗДгІ2ЃКШШЛЏбЇЗНГЬЪНЮЊ____________________________ЁЃ
(3)вЛЖЈЬѕМўЯТЃЌНЋвЛЖЈХЈЖШNOx(NO2КЭNOЕФЛьКЯЦјЬх)ЭЈШыCa(OH)2аќзЧвКжаЃЌИФБф![]() ЃЌNOxЕФШЅГ§ТЪШчЭМЫљЪОЁЃ
ЃЌNOxЕФШЅГ§ТЪШчЭМЫљЪОЁЃ
вбжЊЃКNOгыCa(OH)2ВЛЗДгІЃЛ

NOxЕФШЅГ§ТЪ=1Ѓ![]() ЁС100%
ЁС100%
Ђй![]() дк0.3Ѓ0.5жЎМфЃЌNOЮќЪеЪБЗЂЩњЕФжївЊЗДгІЕФРызгЗНГЬЪНЮЊЃК___________ЁЃ
дк0.3Ѓ0.5жЎМфЃЌNOЮќЪеЪБЗЂЩњЕФжївЊЗДгІЕФРызгЗНГЬЪНЮЊЃК___________ЁЃ
ЂкЕБ![]() Дѓгк1.4ЪБЃЌNO2ШЅГ§ТЪЩ§ИпЃЌЕЋNOШЅГ§ТЪШДНЕЕЭЁЃЦфПЩФмЕФдвђЪЧ__________ЁЃ
Дѓгк1.4ЪБЃЌNO2ШЅГ§ТЪЩ§ИпЃЌЕЋNOШЅГ§ТЪШДНЕЕЭЁЃЦфПЩФмЕФдвђЪЧ__________ЁЃ
(4)ШєНЋCOКЭNOАДВЛЭЌБШР§ЭЖШывЛУмБеШнЦїжаЗЂЩњЗДгІЃК2CO(g)+2NO(g)=N2(g)+2CO2(g) ІЄH=Ѓ759.8 kJ/molЃЌЗДгІДяЕНЦНКтЪБЃЌN2ЕФЬхЛ§ЗжЪ§Ыц![]() ЕФБфЛЏЧњЯпШчЭМЁЃ
ЕФБфЛЏЧњЯпШчЭМЁЃ
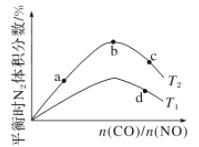
ЂйbЕуЪБЃЌЦНКтЬхЯЕжаCЁЂNдзгИіЪ§жЎБШНгНќ________ЁЃ
ЂкaЁЂbЁЂcШ§ЕуCOЕФзЊЛЏТЪДгаЁЕНДѓЕФЫГађЮЊ________ЃЛbЁЂcЁЂdШ§ЕуЕФЦНКтГЃЪ§ДгДѓЕНаЁЕФЫГађЮЊ__________(вдЩЯСНПеОљгУaЁЂbЁЂcЁЂdБэЪО)ЁЃ
ЂлШє![]() =0.8ЃЌЗДгІДяЦНКтЪБЃЌN2ЕФЬхЛ§ЗжЪ§ЮЊ20%ЃЌдђNOЕФзЊЛЏТЪЮЊ_____ЁЃ
=0.8ЃЌЗДгІДяЦНКтЪБЃЌN2ЕФЬхЛ§ЗжЪ§ЮЊ20%ЃЌдђNOЕФзЊЛЏТЪЮЊ_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПН№ЪєУЬдквБН№ЙЄвЕжагУРДжЦдьЬижжИжЃЌГЃзїЮЊЭбСђМСКЭШЅбѕМСЃЌЦфЛЏКЯЮяЙуЗКгІгУгкЕчГиЁЂЛњаЕжЦдьвЕЕШСьгђЁЃ
(1)вдШэУЬПѓ(жївЊЮЊMnO2)ЮЊдСЯЭЈЙ§ШШЛЙдЗЈЕУЕНН№ЪєУЬЩцМАЕФСНИіЗДгІЃК
Ђй3MnO2(s)=Mn3O4(s)+ O2(g) ЁїH1= akJmol-1
Ђк3Mn3O4(s)+ 8Al(s) =4Al2O3(s) + 9Mn(s) ЁїH2= bkJmol-1
вбжЊAlЕФШМЩеШШЮЊ ЁїH3=ckJmol-1ЃЌдђMnO2гыAlЗЂЩњТСШШЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ___________ЁЃ
(2)ПЦбаШЫдБНЋжЦЕУЕФУЬЗлЫщКѓМгШыЕНSnCl2ШмвКжаЪЙЦфНўГі(МйЖЈдгжЪВЛЗДгІЃЌШмвК ЬхЛ§ВЛБф)ЃЌЗЂЩњЗДгІMn(s)+ Sn2+(aq)![]() Mn2+(aq)+ Sn(s)(вбжЊКЌSn2+ЫЎШмвКЮЊУзЛЦЩЋ)
Mn2+(aq)+ Sn(s)(вбжЊКЌSn2+ЫЎШмвКЮЊУзЛЦЩЋ)
ЧыЛиД№ЯТСаЮЪЬтЃК
ЂйЮЊМгПьЗДгІЫйТЪПЩвдВЩШЁЕФДыЪЉга__________ЃЛВЛПМТЧЮТЖШвђЫиЃЌвЛЖЮЪБМфКѓMnЕФШмНтЫйТЪМгПьЃЌПЩФмЕФдвђЪЧ____________________ЁЃ
ЂкЯТСаФмЫЕУїЗДгІвбДяЦНКтЕФга____________________(ЬюБрКХ)ЁЃ
A.ШмвКЕФбеЩЋВЛЗЂЩњБфЛЏ B.ШмвКжаc(Mn2+)=c( Sn2+)
C.ЬхЯЕжаЙЬЬхЕФжЪСПВЛБф D.Mn2+гыSn2+ХЈЖШЕФБШжЕБЃГжВЛБф
ЂлЪвЮТЯТЃЌВтЕУШмвКжабєРызгХЈЖШc(R2+)ЫцЪБМфЕФБфЛЏЧщПіШчЯТЭМЫљЪОЃЌдђЩЯЪіЗДгІЕФЦНКтГЃЪ§K=________________ЃЌMn2+ЕФВњТЪЮЊ____________ЁЃ
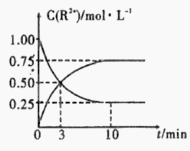
ЂмШєЦфЫћЬѕМўВЛБфЃЌ10minКѓЯђШнЦїжабИЫйМгШыеєСѓЫЎжСШмвКЬхЛ§БфЮЊдРДЕФ2БЖЃЌдђ дйДЮЦНКтЪБc(Mn2+) =____________(ВЛПМТЧРызгЫЎНтЕФгАЯь)ЁЃ
(3)MnO2вВПЩдкMnSO4-H2SO4-H2OЮЊЬхЯЕЕФЕчНтвКжаЕчНтЛёЕУЃЌЦфбєМЋЗДгІЪНЮЊ_____________________ЃЌбєМЋИННќШмвКЕФpH____________(бЁЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПSO2ХХЗХжСПеЦјжаЛсдьГЩДѓЦјЮлШОЃЌФГбаОПаЁзщРћгУШэУЬПѓЃЈжївЊГЩЗжЮЊMnO2ЃЌСэКЌЩйСПЬњЃЌТСЃЌЭЃЌФјЕШН№ЪєЛЏКЯЮяЃЉзїЭбСђМСЃЌЭЈЙ§ШчЯТМђЛЏСїГЬЃЌМШЭбГ§ШМУКЮВЦјжаЕФSO2ЃЌгжжЦЕУЕчГиВФСЯMnO2ЃЈЗДгІЬѕМўвбЪЁТдЃЉЁЃ
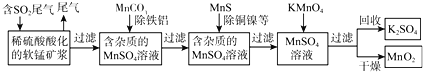
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉвбжЊЃК25ЁцЁЂ101kPaЪБЃЌ
Mn(s)+O2(g)=MnO2(s) ЁїH=-520kJ/mol
S(s)+O2(g)=SO2(g) ЁїH=-297kJ/mol
Mn(s)+S(s)+2O2(g)=MnSO4(s) ЁїH=-1065kJ/mol
ИљОнвдЩЯаХЯЂаДГігУMnO2ЭбСђЕФШШЛЏбЇЗНГЬЪНЪЧ______
ЃЈ2ЃЉЕкЖўВНМгШыMnCO3ЦфдвђЪЧ______
ЃЈ3ЃЉШєзюКѓвЛВНЫљМгKMnO4ЧЁКУЗДгІЭъШЋЃЌШчКЮжЄУїЙ§ТЫЫљЕУЕФMnO2ЙЬЬхвбЯДЕгИЩОЛЃК______
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩшNAЮЊАЂЗќМгЕТТоГЃЪ§жЕЁЃШчЭМБэЪОN2OдкPt2O+БэУцгыCOЗДгІзЊЛЏГЩЮоКІЦјЬхЕФЙ§ГЬЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ

A.N2OзЊЛЏГЩЮоКІЦјЬхЪБЕФДпЛЏМСЪЧPt2O2+
B.УП1mol Pt2O+зЊЛЏЮЊPt2O2+ЕУЕчзгЪ§ЮЊ3NA
C.НЋЩњГЩЕФCO2ЭЈШЫКЌДѓСПSiO32-ЁЂNa+ЁЂCl-ЕФШмвКжаЃЌЮоУїЯдЯжЯѓ
D.1g CO2 ЁЂN2OЕФЛьКЯЦјЬхжаКЌгаЕчзгЪ§ЮЊ0.5NA
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЪЧH2 КЭCl2 ЗДгІЩњГЩHClЕФФмСПБфЛЏЪОвтЭМЃЌгЩЭМПЩжЊЃЈЁЁЁЁЃЉ
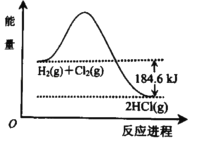
A. ЗДгІЮяЕФФмСПзмКЭаЁгкЩњГЩЮяЕФФмСП
B. ЩњГЩ1molHClЃЈgЃЉашЮќЪе92.3kJЕФФмСП
C. H2ЃЈgЃЉ+Cl2ЃЈgЃЉЃН2HClЃЈgЃЉЁїHЃНЉ184.6 kJmolЉ1
D. H2ЃЈgЃЉ+Cl2ЃЈgЃЉЃН2HClЃЈgЃЉЁїHЃНЉ184.6 kJ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮяжЪЕФСПЪЧИпжаЛЏбЇжаГЃгУЕФЮяРэСПЃЌЧыЭъГЩвдЯТгаЙиФкШнЁЃ
(1)ПЇЗШКЌгаПЇЗШвђ(ЛЏбЇЪНЮЊC8H10N4O2)ЃЌдђПЇЗШвђЕФФІЖћжЪСПЮЊ__________g/molЁЃ
(2)0.2 g H2ДѓдМКЌга________ИіHдзгЁЃ
(3)100 mLФГAl2(SO4)3ШмвКжаЃЌc(Al3ЃЋ)ЃН2.0 mol/LЃЌЦфжаc(SO42Ѓ)ЃН ________mol/LЁЃ
(4)8 ПЫO2КЭO3ЕФЛьКЯЦјЬхжабѕдзгЕФЮяжЪЕФСПЮЊ ________molЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГПЮЭтЛюЖЏаЁзщЮЊСЫбаОПЁАИЩдяЕФCO2ВЛФмгыNa2O2ЗДгІЁБКЭЁАCO2дкгаЫЎДцдкЪБВХФмгыNa2O2ЗДгІЁБЃЌЩшМЦСЫШчЯТЪЕбщзАжУЃК

(1)ШчЭМзАжУЃЌдкИЩдяЙмжазАШыNa2O2КѓЃЌДђПЊЛюШћМгШыЯЁСђЫсЃЌЩњГЩCO2ЁЃДђПЊK1ЃЌЙиБеK2ЃЌМгШШЭЫПЃЌФПЕФЪЧ_____ЃЌXЪЧ_____ЁЃЪЕбщЙлВьЕНЭЫПЮДБфЛЏЃЌдђЕУГіНсТл______ЁЃ
(2)ШєДђПЊK2ЃЌЙиБеK1ЃЌГіЯж________ЯжЯѓЃЌПЩжЄУїгаЫЎЪБCO2гыNa2O2ЗДгІВњЩњСЫO2ЁЃ
(3)ИљОнвдЩЯЕФЪЕбщНсТлЃЌаДГіЩњГЩCO2ЁЂO2ЗДгІЕФЛЏбЇЗНГЬЪНЃК_______________ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com