
����Ŀ����������������Դ�����ˮ�����Ⱦ�ǻ�����������Ҫ�о����⡣
(1) ��ѧ�ϲ���NH3����NxOy��������������Ⱦ��������Ϊ��ҵ������������Դ��
��֪��2NO(g)=N2(g)+O2(g) ��H=��177kJ/mol
4NH3(g)+3O2(g)===2N2(g)+6H2O(g) ��H=��1253.4kJ/mol
����NH3����NO���ɵ�������̬ˮ���Ȼ�ѧ����ʽΪ___________________��
(2)��֪��N2(g)+3H2(g) ![]() 2NH3(g) ��H<0����ͬ�¶��£������������зֱ�Ͷ����ͬ���ķ�Ӧ����з�Ӧ����ò�ͬѹǿ��ƽ��������NH3�����ʵ���������ͼ��ʾ��
2NH3(g) ��H<0����ͬ�¶��£������������зֱ�Ͷ����ͬ���ķ�Ӧ����з�Ӧ����ò�ͬѹǿ��ƽ��������NH3�����ʵ���������ͼ��ʾ��

��M���v��_________Q���v��(����>����<������=��)��
��T3�¶��£���1molN2��3molH2����2L���ܱ������У�ά��ѹǿΪ60MPa���䣬�ﵽN���ƽ��״̬����Ӧ��Ũ��ƽ�ⳣ��K=_____________ (����������ʾ)��M���ƽ�ⳣ����N���ƽ�ⳣ��_________(����������С�����������)��
(3)ˮ���й�������(��NH3��ʾ)�ᵼ��ˮ�帻Ӫ������
���ô������Ƴ�ȥ������ԭ����ͼ��ʾ��д���ܷ�Ӧ��ѧ����ʽ��_____________��


��ȡһ�����ĺ�������ˮ���ı����������Ƶ���������Ӧһ��ʱ�����Һ�а���ȥ���ʡ��ܵ�(��Һ�����п����Եĺ����������е�Ԫ�ص�����)ȥ�����Լ�ʣ��������Ƶĺ�����m(NaClO)��m(NH3)�ı仯�������ͼ��ʾ����Bʣ��NaClO�������ڵ�A��ԭ����____����m(NaClO)��m(NH3)>7.6ʱ��ˮ�����ܵ�ȥ���ʷ����½������ܵ�ԭ����__________��
(4)�缫����Ĥ��������ǵ绯ѧ�����﹤�յ���ϡ�ij����Ĥ�����õ������Ļ���ԭ�ӽ�NO3-��ԭΪN2������ԭ������ͼ��ʾ�����������ɱ�״����2.24 L���壬�����Ͽɳ�ȥNO3-�����ʵ���Ϊ_____mol��

���𰸡�4NH3(g)��6NO (g)=5N2(g)��6H2O(g)�� ��H��-1784.4kJ��mol��1 > 25/108 �� 2NH3��3NaClO=N2��3NaCl��3H2O ����NaClO��������Ӧ���ʼӿ죬��ͬʱ����NaClO���Ķ� �в���NH3��������NO2-��NO3- 0.08
��������
(1)NH3��NO���ɵ�������̬ˮ�Ļ�ѧ����ʽΪ4NH3(g)+6NO(g)�T5N2(g)+6H2O(g)��������֪�Ȼ�ѧ����ʽ��ϸ�˹���ɷ������
(2)��Q��M������ͬһ���������ϣ���M��ѹǿ�ߣ�����ѹǿ�Ի�ѧ��Ӧ����Ӱ���𣻢���������ʽ����N���������ʵ������ٸ������ʵ���֮�ȵ������֮�ȼ���ƽ��ʱ���������ת��Ϊ�����ʵ�Ũ�ȴ���ƽ�ⳣ������ʽ����K���÷�Ӧ�����Ƿ��ȷ�Ӧ���¶�Խ��ƽ�ⳣ��KԽС���ݴ˷������
(3)�ٸ���ͼʾ�жϷ���������ԭ��Ӧ�ķ�Ӧ������������ת�����غ��Ԫ���غ������д�������Ӵ������ƻ�ӿ췴Ӧ���ʣ�NaClOͶ�����Ὣ��������ΪNO3-�ȸ���̬�����ʣ�
(4)����������������ʧ�������ɵ��������������ɵ����������ת�Ƶĵ��ӵ����ʵ�������ϵ����غ���������Ͽɳ�ȥNO3-�����ʵ�����
(1)NH3��NO���ɵ�������̬ˮ�Ļ�ѧ����ʽΪ4NH3(g)+6NO(g)�T5N2(g)+6H2O(g)����2NO(g)=N2(g)+O2(g) ��H=��177kJ/mol����4NH3(g)+3O2(g)===2N2(g)+6H2O(g) ��H=��1253.4kJ/mol�����ݸ�˹���ɢ���3+�ڵõ�4NH3(g)+6NO(g)�T5N2(g)+6H2O(g)��H=(-177kJ/mol)��3+(-1253.4kJ/mol)-1784.4kJ/mol���ʴ�Ϊ��4NH3(g)+6NO(g)�T5N2(g)+6H2O(g)��H=-1784.4kJ/mol��
(2)��Q��M������ͬһ���������ϣ���M��ѹǿ�ߣ�����M�㷴Ӧ���ʴʴ�Ϊ������
�ڷ�Ӧ������ʽ��N2(g)+3H2(g)2NH3(g)
��ʼ��(mol) 1 3 0
�仯��(mol) x 3x 2x
ƽ����(mol) 1-x 3-3x 2x
ƽ��ʱ�����ĺ���Ϊ20%����![]() ��100%=20%��x=
��100%=20%��x=![]() mol��N2��H2��NH3�����ʵ����ֱ�Ϊ
mol��N2��H2��NH3�����ʵ����ֱ�Ϊ![]() mol��2mol��
mol��2mol��![]() mol�������ʵ���Ϊ(4-2��
mol�������ʵ���Ϊ(4-2��![]() )mol=
)mol=![]() mol����ѹʱ�������֮�ȵ������ʵ���֮�ȣ�����ƽ��ʱ�������Ϊ
mol����ѹʱ�������֮�ȵ������ʵ���֮�ȣ�����ƽ��ʱ�������Ϊ![]() L=
L=![]() L����c(N2)=c(NH3)=0.4mol/L��c(H2)=1.2mol/L��ƽ�ⳣ��K=
L����c(N2)=c(NH3)=0.4mol/L��c(H2)=1.2mol/L��ƽ�ⳣ��K=![]() =
=![]() =
=![]() ���÷�Ӧ������ȣ�����ƽ�������ƶ���ƽ�ⳣ��k��С������T3��T2ʱ��T3��ƽ�ⳣ��С��T2��ʱƽ�ⳣ������M��ƽ�ⳣ������N��ƽ�ⳣ�����ʴ�Ϊ��
���÷�Ӧ������ȣ�����ƽ�������ƶ���ƽ�ⳣ��k��С������T3��T2ʱ��T3��ƽ�ⳣ��С��T2��ʱƽ�ⳣ������M��ƽ�ⳣ������N��ƽ�ⳣ�����ʴ�Ϊ��![]() ����
����
(3)�ٸ���ͼʾ����ʼ̬����̬�жϷ�Ӧ����NH3������ΪN2����NaCl����ԭΪNaCl������1molN2ת��6mol���ӣ�����ת�Ƶĵ����غ㣬��Ҫ3molNaClO���ٽ��Ԫ���غ㣬��Ӧ�Ļ�ѧ����ʽΪ2NH3+3NaClO=N2+3H2O+3NaCl���ʴ�Ϊ��2NH3��3NaClO=N2��3NaCl��3H2O��
������NaClO��������Ӧ���ʼӿ죬��ͬʱ����NaClO���Ķ࣬ʹ��B��ʣ��NaClO��������A�㣻��m(NaClO)��m(NH3)��7.7ʱ��������NaClOͶ�����Ὣ��������ΪNO3-�ȸ���̬�����ʣ�δ�ܴ���Һ�г�ȥ��ʹ���ܵ���ȥ������m(NaClO)��m(NH3)���������������ʴ�Ϊ������NaClO��������Ӧ���ʼӿ죬��ͬʱ����NaClO���ĶࣻNaClOͶ�����Ὣ����NH3��������NO2-��NO3-��
(4)��������������Ӧ����Һ�е�����������ʧ�������ɵ���������״���£�2.24L���������ʵ���=![]() =0.1mol��ת�Ƶĵ���Ϊ0.1mol��4=0.4mol������ԭ�ӽ�NO3-��ԭΪN2�����ڹ�ϵNO3-��
=0.1mol��ת�Ƶĵ���Ϊ0.1mol��4=0.4mol������ԭ�ӽ�NO3-��ԭΪN2�����ڹ�ϵNO3-��![]() N2��5e-�������Ͽɳ�ȥNO3-�����ʵ���=
N2��5e-�������Ͽɳ�ȥNO3-�����ʵ���=![]() =0.08mol���ʴ�Ϊ��0.08��
=0.08mol���ʴ�Ϊ��0.08��


 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��������ý���ϣ���Ҫ�ɷ�ΪNi-Al�Ͻ𣬻�������Fe��Cu��Zn���л�� �Ʊ�NiO�����ս�����Դ������������ʾ��
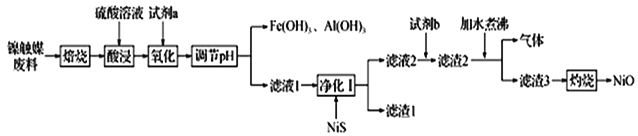
��֪������������1�ͱ�2��ʾ
��1�������ܵ���ʵ��ܶȻ�������25�棩
���� | Ksp | ���� | Ksp |
Fe(OH)3 | 4.0��10-38 | CuS | 6.3��10-34 |
Fe(OH)2 | 1.8��10-16 | ZnS | 1.6��10-24 |
Al(OH)3 | 1.0��10-33 | NiS | 3.2��10-18 |
Ni(OH)2 | 2.0��10-15 |
��2 ԭ�ϼ۸��
���� | �۸�/��Ԫ��-1�� |
ƯҺ����25.2%NaClO�� | 450 |
˫��ˮ����30%H2O2�� | 2400 |
�ռ��98%NaOH�� | 2100 |
�����99.5%Na2CO3�� | 600 |
��ش��������⣺
��1�������ա���Ŀ����________________________________��
��2�����Լ�a��������Ϊ__________________��ѡ����Լ���������______��
��3����������ʱ��Ӧ�����ӷ���ʽΪ__________________________________________��
��4����ʹ��Һ��Fe3+��A13+��Ũ�Ⱦ�С�ڵ���1.0��10-6 mol L-1���衰����pH������Ϊ_______________��
��5�����Լ�b��Ӧѡ��__________������ˮ��С�ʱ����Ӧ�Ļ�ѧ����ʽΪ_______________________________��
��6�����������һ��Ӧ�ù㷺�Ķ��ε�أ��ŵ�ʱ���õ�ص��ܷ�ӦΪNiOOH+MH=Ni(OH)2+M��������������2 mol����ʱ�������ϸ�����������__________g�����ʱ��������ӦʽΪ_______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.10 mol��L-1NaOH��Һ�ֱ�ζ�20.00 mLŨ�Ⱦ�Ϊ 0.10mol L-1��CH3COOH(Ka=1.75��10-5)��Һ��HCN (Ka=4.9��10-10)��Һ���õζ�������ͼ������˵����ȷ����

A. ����I�����ߢ�ֱ��������CH3COOH��HCN
B. ��ۺ͵����ʾ��Һ�У�c(CN-)=c(CH3COO-)
C. ��ٺ͵����ʾ��Һ�У�c��CH3COO-��-c��CN-��=c��HCN��-c��CH3COOH��
D. �ڵ�ں͢�֮�䣨�������˵������ڹ�ϵ�� c(Na+)>c(A-)>c(H+)>c(OH-) (A-������Һ�е�������ӣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش���������:
��1�������м������ʣ��뽫����������пո��ڣ�
A��CH2=CH-COOH�����ᣨC17H33COOH��
B��C60��ʯī
C��![]() ��
��![]()
D��35Cl��37Cl
E���Ҵ����Ҷ���
�ٻ�Ϊͬλ�ص���______________��
�ڻ�Ϊͬϵ�����_________________��
�ۻ�Ϊͬ�����������__________��
�ܻ�Ϊͬ���칹�����_____________��
��2���ݶ��ݣ�TNT���ṹ��ʽΪ____________________________��
��3��ij�л��ۺ�����ṹΪ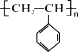 ���Իش��������⣺
���Իش��������⣺
���л���������___________________������Ϊ______��
��ʵ���øø߾������Է���������ƽ��ֵ��Ϊ52000����ø߾���ľۺ϶�nΪ________��
��4��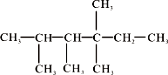
�����������__________________________��
�ڴ��л���Ϊϩ���ӳɵIJ����ԭ��ϩ���Ľṹ������_______�֡�
��5��ij���ʽṹ��ͼ��ʾ������ʽΪ_________________�������ʿ���������_____���������������Ӧ��
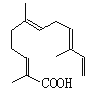
A������KMnO4��Һ B������
C����ˮ D��NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C���ֿ��������Σ����������Ӹ�����ͬ���������ӵ�Ħ��������������A��B��C��˳���������ʵ�����A��B��C����ˮ��������Һ��ֻ����Fe3����K����SO![]() ��NO
��NO![]() ��Cl���������ӣ�ͬʱ����һ�ְ�ɫ������
��Cl���������ӣ�ͬʱ����һ�ְ�ɫ������
��ش��������⣺
��1�������飬���������л���������ѡ���е�һ�����ӣ��������� ��
A��Na�� B��Mg2�� C��Cu2�� D��Ag��
��2���������εĻ�ѧʽ�ֱ��ǣ�A ��B ��C ��
��3������A��B��C�������ΰ�һ����������ˮ��������Һ��ֻ����Fe3����SO![]() ��NO
��NO![]() ��K���������������ʵ���֮������Ϊ1��2��3��4����A��B��C�������ε����ʵ���֮��Ϊ ��
��K���������������ʵ���֮������Ϊ1��2��3��4����A��B��C�������ε����ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ��һ���ܴ����������
A. ��84������Һ�У�SiO32-��CO32-��Na+��K+
B. ![]() ����Һ��NH4+��Ca2+��C1-��NO3-
����Һ��NH4+��Ca2+��C1-��NO3-
C. 0.1mol/LNaA1O2��Һ�У�HCO3-��NH4+��SO32-��Fe3+
D. pH=1����Һ�У�Na+��K+��Cl-��S2O32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Li/Li2O��ϵ������ѭ��ͼ��ͼ��ʾ������˵����ȷ����

A. ��H3<0 B. ��H3+��H4+��H5=��H6
C. ��H6>��H5 D. ��H1+��H2+��H3+��H4+��H5+��H6=0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�ܱ������м��� 0.3 mol A��0.1 mol C ��һ������ B �������壬 һ�������·������·�Ӧ�� 3A(g) ![]() B(g)��2C(g)�������ʵ�Ũ����ʱ��仯��ͼ��ʾ[t0��t1 �ε� c(B)�仯δ����]������˵������ȷ����( )
B(g)��2C(g)�������ʵ�Ũ����ʱ��仯��ͼ��ʾ[t0��t1 �ε� c(B)�仯δ����]������˵������ȷ����( )

A. �� t1��15 s������ A ��Ũ�ȱ仯��ʾ t0��t1�ε�ƽ����Ӧ����Ϊ 0.004 mol��L��1��s��1
B. t1ʱ�÷�Ӧ�ﵽƽ�⣬ A ��ת����Ϊ 60%
C. ���������ݻ�Ϊ2 L��B����ʼ�����ʵ���Ϊ 0.02 mol
D. t0��t1 �Σ� �˹����������������Ƚ�������Ϊ a kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ 3A(g)![]() B(g)��2C(g) ��H����50a kJ��mol��1
B(g)��2C(g) ��H����50a kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����ˮɹ�ο��Եõ����������γ��� NaCl �������������� MgCl2��CaCl2��Na2SO4��KCl �Լ���ɳ�������������Ǽ�����ͬѧ��ʵ�����д����ᴿ�IJ���������

�ṩ���Լ���Na2CO3 ��Һ��K2CO3��Һ��NaOH ��Һ��BaCl2 ��Һ��75%�Ҵ���
��1������ȥ��Һ I �е� MgCl2��CaCl2��Na2SO4�����ṩ���Լ���ѡ�� a ���������Լ������μ�˳������Ϊ____��
A. ������ NaOH ��Һ��Na2CO3 ��Һ��BaCl2 ��Һ
B. ������ NaOH ��Һ��K2CO3��BaCl2 ��Һ
C. ������ NaOH ��Һ��BaCl2 ��Һ��Na2CO3 ��Һ
D. ������ NaOH ��Һ��BaCl2 ��Һ��K2CO3 ��Һ
��2����μ������� BaCl2 ��Һ�ѹ���____��
��3������Һ�м������������_____������____�����������������������Թ�����
��4����ϴ�ӵ�ʱ��������ʹ�õ����ϴ�Ӽ���_____��
��5����ͬѧ��ʹ���ᴿ�õ��ľ������� 100mL 1mol/L �� NaCl ��Һ����Ҫ���� NaCl____g����ʹ�õIJ� �����������ձ����������ͽ�ͷ�ιܻ���_____��
��6����ͬѧ�۲���ͬѧ�IJ�������Ϊ�����Ƶ���ҺŨ��ƫ������ͬѧ�������Ĵ��������____��
A. ����ʱ�����Ӷ���
B. ϴ������ƿ��û�н��и���
C. δϴ���ձ��Ͳ����� 2 ����3 ��
D. �ڶ���ʱ��ˮ�����̶��������ý�ͷ�ι��������ಿ��
E. ��ˮ���̶��ߺ���ҡ�ȹ�����������Һ����ڿ̶���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com