
”¾ĢāÄæ”æO2ŗĶO3ŹĒŃõŌŖĖŲµÄĮ½ÖÖµ„ÖŹ£¬øł¾ŻĘä·Ö×ÓŹ½Ķź³ÉĻĀĮŠø÷Ģā£ŗ
£Ø1£©ÖŹĮæÖ®ŗĶĪŖ96æĖµÄO2ŗĶO3µÄĘųĢå»ģŗĻ£¬ĘäŃõŌ×ÓøöŹżĪŖ______________”£
£Ø2£©ĻÖŅŖÅäÖĘ1 mol”¤L1 Na2CO3ČÜŅŗ250 mL£¬Ēó£ŗ¢ŁŠčŅŖ¹ĢĢåNa2CO3_____________g£»¢ŚŠčŅŖŗ¬½į¾§Ė®µÄĢ¼ĖįÄĘ¾§Ģå£ØNa2CO3”¤10 H2O£© g£»¢ŪŠčŅŖĪļÖŹµÄĮæÅضČĪŖ4 mol”¤L1µÄNa2CO3ČÜŅŗ mL£»¢ÜŠčŅŖČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ12£„”¢ĆܶČĪŖ1£®12 g”¤cm-3µÄNa2CO3ČÜŅŗ mL”£
£Ø3£©ŌŚÅäÖĘÉĻŹöČÜŅŗµÄ¹ż³ĢÖŠ£¬æÉÄܵ¼ÖĀÅäÖĘČÜŅŗÅضČĘ«Š”µÄÓŠ£ŗ_________
A. ¹ĢĢåNa2CO3·ÅŌŚÓŅÅĢ£Ø1 gŅŌĻĀÓĆÓĪĀė£©£»
B. ČŻĮæĘæÓĆĢ¼ĖįÄĘČÜŅŗĻČČóĻ“£»
C. ×ŖŅĘČÜŅŗŹ±Ī“Ļ“µÓÉÕ±£»
D. ¶ØČŻŹ±£¬ČÜŅŗĪ“ĄäČ“£»
E. ¶ØČŻŹ±ŹÓĻßŃöŹÓ£»
F. Ņ”ŌČŹ±£¬·¢ĻÖŅŗĆęµĶÓŚČŻĮæĘææĢ¶ČĻߣ¬µ«Ī“²¹¼ÓĖ®£»
G. ČŻĮæĘæĪ“øÉŌļ”£
”¾“š°ø”æ£Ø1£©6NA£Ø2£©26.5£»71.5£»62.5£»197.2£Ø3£©ACE
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©O2ŗĶO3¾łŹĒŃõŌŖĖŲŠĪ³ÉµÄ²»Ķ¬µ„ÖŹ£¬ŌņÖŹĮæÖ®ŗĶĪŖ96æĖµÄO2ŗĶO3µÄĘųĢå»ģŗĻ£¬ĘäŃõŌ×ÓøöŹżĪŖ![]() ”£
ӣ
£Ø2£©ÅäÖĘĢ¼ĖįÄĘČÜŅŗ£¬ŠčŅŖĢ¼ĖįÄĘ¹ĢĢåµÄÖŹĮæĪŖ1 mol”¤L£1”Į0.25L”Į106g/mol£½26.5g£¬ŠčŅŖŗ¬½į¾§Ė®µÄĢ¼ĖįÄĘ¾§ĢåµÄÖŹĮæĪŖ 1 mol”¤L£1”Į 0.25L”Į286g/mol£½71.5g £¬ŠčŅŖĢ¼ĖįÄʵÄČÜŅŗµÄĢå»żĪŖ1 mol”¤L£1”Į 0.25L”Ā4 mol”¤L£1£½62.5 mL£¬ŠčŅŖČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ12%”¢ĆܶČĪŖ1.12g”¤cm£3µÄNa2CO3ČÜŅŗµÄĢå»żĪŖ1 mol”¤L£1”Į0.25L”Į106 g/mol”Ā£Ø12%”Į1.12g”¤cm£3£©£½197.2mL”£
£Ø3£©A. ¹ĢĢåNa2CO3·ÅŌŚÓŅÅĢ£Ø1 gŅŌĻĀÓĆÓĪĀė£©£¬Ōņµ¼ÖĀ³ĘĮæµÄĢ¼ĖįÄĘÖŹĮæ¼õÉŁ£¬ÅضČĘ«Š”£¬AÕżČ·£»B. ČŻĮæĘæÓĆĢ¼ĖįÄĘČÜŅŗĻČČóĻ“£¬µ¼ÖĀČÜÖŹµÄĪļÖŹµÄĮæŌö¼Ó£¬ÅضČĘ«“ó£¬B“ķĪó£»C. ×ŖŅĘČÜŅŗŹ±Ī“Ļ“µÓÉÕ±£¬µ¼ÖĀČÜÖŹµÄĪļÖŹµÄĮæ¼õŠ”£¬ÅضČĘ«Š”£¬CÕżČ·£»D. ¶ØČŻŹ±£¬ČÜŅŗĪ“ĄäČ“£¬ŌņČÜŅŗµÄĢå»ż¼õÉŁ£¬ÅضČĘ«“ó£¬D“ķĪó£»E. ¶ØČŻŹ±ŹÓĻßŃöŹÓ£¬ČÜŅŗĢå»żŌö¼Ó£¬ÅضČĘ«Š”£¬EÕżČ·£»F. Ņ”ŌČŹ±£¬·¢ĻÖŅŗĆęµĶÓŚČŻĮæĘææĢ¶ČĻߣ¬µ«Ī“²¹¼ÓĖ®£¬ÅØ¶Č²»±ä£¬F“ķĪó£»G. ČŻĮæĘæĪ“øÉŌļ£¬ÅØ¶Č²»±ä£¬G“ķĪ󣬓š°øŃ”ACE”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń.ŅŃÖŖHClOŹĒ±ČH2CO3»¹ČõµÄĖį£¬HClOµÄµēĄėĘ½ŗā³£ŹżĪŖ2.95”Į10-5£¬H2CO3µÄµēĄėĘ½ŗā³£ŹżĪŖK1£½4.3”Į10£7ŗĶK2£½5.6”Į10£11ĀČĖ®ÖŠ“ęŌŚĻĀĮŠĘ½ŗā£ŗCl2£«H2O![]() HCl£«HClO£¬HClO
HCl£«HClO£¬HClO![]() H£«£«ClO££¬“ļĘ½ŗāŗó
H£«£«ClO££¬“ļĘ½ŗāŗó
(1)ŅŖŹ¹HClOÅضČŌö¼Ó£¬æɼÓČėĻĀĮŠĪļÖŹ________(Ģī“śŗÅ)”£
A£®SO2 B£®NaHCO3 C£®HCl D£®NaOH
(2)ÓÉ“ĖĖµĆ÷ŌŚŹµŃéŹŅæÉÓĆÅű„ŗĶŹ³ŃĪĖ®ŹÕ¼ÆCl2µÄĄķÓÉŹĒ________________”£
¢ņ.Al(OH)3µÄµēĄė·½³ĢŹ½æɱķŹ¾ĪŖ£ŗH2O£«AlO2££«H£«![]() Al(OH)3
Al(OH)3![]() Al3£«£«3OH£”£
Al3£«£«3OH£”£
ŹŌøł¾ŻĘ½ŗāŅʶÆŌĄķ£¬½āŹĶĻĀĮŠÓŠ¹ŲĪŹĢā”£
(1)ĻņAl(OH)3³ĮµķÖŠ¼ÓČėŃĪĖį£¬³ĮµķČܽā£¬ĘäŌŅņŹĒ_________________£¬ÓŠ¹ŲĄė×Ó·½³ĢŹ½ĪŖ__________________”£
(2)ĻņAl(OH)3³ĮµķÖŠ¼ÓČėæĮŠŌÄĘČÜŅŗ£¬³ĮµķČܽā£¬ĘäŌŅņŹĒ________________£¬ÓŠ¹ŲĄė×Ó·½³ĢŹ½ĪŖ__________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚŗ£Ė®×ŹŌ“×ŪŗĻĄūÓƵÄĖµ·ØÖŠ£¬²»ÕżČ·µÄŹĒ£Ø £©
A£®“Óŗ£Ė®ÖŠø»¼ÆĆ¾ŌŖĖŲæÉÓĆCa(OH)2³Įµķ·Ø
B£®ŗ£Ė®µ»ÆµÄ·½·ØÖ÷ŅŖÓŠÕōĮó·Ø”¢Ąė×Ó½»»»·Ø”¢µēÉųĪö·Ø
C£®“Óŗ£Ė®ÖŠĢįČ”äåµ„ÖŹµÄ¹ż³ĢÖŠÓĆĀČĘų×ö»¹Ō¼Į
D£®“Óŗ£Ė®ÖŠ»ńµĆ“ÖŃĪæÉÓĆÕō·¢½į¾§·Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ

£Ø1£©Š“³öĻĀĮŠŅĒĘ÷µÄĆū³Ę£ŗ¢Ł____________£¬¢Ś____________£¬¢Ü____________”£
£Ø2£©ŅĒĘ÷¢Ł”«¢ÜÖŠ£¬Ź¹ÓĆŹ±±ŲŠė¼ģ²éŹĒ·ńĀ©Ė®µÄŹĒ________________£ØĢīŠņŗÅ£©”£
£Ø3£©ČōĄūÓĆ×°ÖĆ¢ń·ÖĄė¾Ę¾«ŗĶĖ®µÄ»ģŗĻĪļ£¬»¹Č±ÉŁµÄŅĒĘ÷____________£¬½«ŅĒĘ÷²¹³äĶźÕūŗó½ųŠŠµÄŹµŃé²Ł×÷µÄĆū³ĘĪŖ____________£»¢ŚµÄ½ųĖ®æŚŹĒ____________£ØĢī”°f”±»ņ”°g”±£©”£
£Ø4£©ĻÖŠčÅäÖĘ250mL”¢0.2 mol”¤L£1NaClČÜŅŗ£¬×°ÖĆ¢ņŹĒijĶ¬Ń§×ŖŅĘČÜŅŗµÄŹ¾ŅāĶ¼£¬Öø³öĶ¼ÖŠµÄ“ķĪó²Ł×÷£ŗ______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ”°ĀĢÉ«»Æѧ”±µÄŗĖŠÄŹĒŌŚ»Æѧ·“Ó¦¹ż³ĢÖŠ»ņ»Æ¹¤Éś²śÖŠ£¬¾”Įæ¼õÉŁŹ¹ÓĆ»ņ³¹µ×Ļū³żÓŠŗ¦ĪļÖŹ£¬ĻĀĮŠ×ö·ØÖŠ£¬·ūŗĻ”°ĀĢÉ«»Æѧ”±ĄķÄīµÄŹĒ ( )
A£®Éś²śŗĶŹ¹ÓĆ¾ē¶¾Å©Ņ© B£®»Æ¹¤³§²śÉśµÄ·ĻĘųĻņøßæÕÅÅ·Å
C£®ĄūÓĆĒāĘų×÷øßÄÜČ¼ĮĻ D£®ŌģÖ½³§ÓƶžŃõ»ÆĮņ½ųŠŠÖ½½¬ĘÆ°×
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉś»īÖŠ“¦“¦ÓŠ»Æѧ£¬ĻĀĮŠ±ķŹö²»ÕżČ·µÄŹĒ( )
A£®ŃĻ½ūĀŅĘś·Ļµē³Ų£¬·ĄÖ¹ÖŲ½šŹōĪŪČ¾ĶĮČĄŗĶĖ®Ō“
B£®Ę¤·ōÕ“ÓŠÓĶÖ¬Ź±£¬Į¢¼“ÓĆĒāŃõ»ÆÄĘĻ”ČÜŅŗ²ĮĻ“
C£®¹čĖįÄʵÄĖ®ČÜŅŗĖ׳ĘĖ®²£Į§£¬ŹĒÖʱø¹č½ŗŗĶľ²Ä·Ą»š¼ĮµÄŌĮĻ
D£®ÓĆŗ¬³ČÉ«ĖįŠŌÖŲøõĖį¼ŲµÄŅĒĘ÷¼ģŃé¾Ę¼Ż£¬ĄūÓĆĮĖŅŅ“¼µÄ»Ó·¢ŠŌŗĶ»¹ŌŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNA±ķŹ¾°¢·üŁ¤µĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ŌŚ±ź×¼×“æöĻĀ£¬22.4LCCl4ÖŠŗ¬5 NA øöŌ×Ó
B£®0.1molĢśÓė×ćĮæµÄŃĪĖįĶźČ«·“Ó¦£¬ĢśŹ§Č„µÄµē×ÓŹżĪŖ0.1 NA
C£®1.6gÓÉŃõĘųŗĶ³ōŃõ×é³ÉµÄ»ģŗĻĪļÖŠŗ¬ÓŠŃõŌ×ӵďżÄæĪŖ0.1 NA
D£®½«100mL0.1mol/LµÄFeCl3ČÜŅŗµĪČė·ŠĖ®ÖŠæÉÖʵĆFe(OH£©3½ŗĮ£ŹżÄæĪŖ0.01 NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£ØI£©¼ģŃéijČÜŅŗÖŠŹĒ·ńŗ¬SO42-µÄÕżČ·²Ł×÷Ė³ŠņŹĒ£ŗȔɣĮæĪ“ÖŖČÜŅŗ£¬¼ÓČė____________________£¬Čō³öĻÖ ĻÖĻó£¬ŌŁ¼ÓČė_____________£¬Čō³öĻÖ ĻÖĻó£¬Ö¤Ć÷ŌČÜŅŗŗ¬ÓŠSO42-£»BaSO4ŗĶNaClµÄŠü×ĒŅŗŌŚ·ÖĄė¹ż³ĢÖŠÉę¼°µ½¹żĀĖ”¢Ļ“µÓ³Įµķ²Ł×÷£¬Ö¤Ć÷ĀĖÖ½ÉĻµÄBaSO4³ĮµķŅŃ¾Ļ“¾»µÄ·½·ØŹĒ_______________”£
£Ø¢ņ£©ĻÖÓŠA”¢BĮ½ÖÖÓŠ»śĪļµÄŅŗĢå»ģŗĻĪļ£¬Čē¹ūA”¢B»„ČÜ£¬ĒŅĻą»„²»·¢Éś»Æѧ·“Ó¦”£ŌŚ³£Ń¹ĻĀ£¬AµÄ·ŠµćĪŖ35”ę£¬BµÄ·ŠµćĪŖ200”ę”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©·ÖĄėÉĻŹöA”¢BµÄ»ģŗĻĪļ£¬³£ÓƵķ½·ØŹĒ £¬ŠčŅŖµÄ²£Į§ŅĒĘ÷ÓŠ¾Ę¾«µĘ”¢ĪĀ¶Č¼Ę”¢Å£½Ē¹Ü”¢ÕōĮóÉÕĘ棬»¹ÓŠ ŗĶ £ØĆææÕ1·Ö£©”£
£Ø2£©Ó¦ÓĆÉĻŹö·ÖĄė²Ł×÷£¬Ź×ĻȵƵ½µÄĪļÖŹŹĒ ”£
£Ø3£©µćČ¼¾Ę¾«µĘĒ°µÄ×ī½üŅ»²½²Ł×÷ŹĒ ”£
£Ø¢ó£©ĻĀĶ¼ŹĒĮņĖįŹŌ¼ĮĘæ±źĒ©ÉĻµÄÄŚČŻ£ŗ
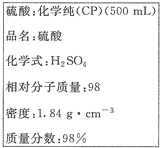
£Ø1£©øĆĮņĖįµÄĪļÖŹµÄĮæÅØ¶ČŹĒ mol”¤L-1”£
£Ø2£©Ä³»ÆѧŠĖȤŠ”×é½ųŠŠĮņĖįŠŌÖŹµÄŹµŃéĢ½¾æŹ±£¬ŠčŅŖ240 mL 4.6 mol”¤L-1µÄĻ”ĮņĖį£¬ŌņŠčŅŖČ” mLµÄøĆĮņĖį”£½«ÉĻŹöĮņĖį½ųŠŠĻ”ŹĶµÄŹµŃé²Ł×÷ĪŖ ”£
£Ø3£©ÓĆÉĻŹöĮņĖįÅäÖĘ240 mL 4.6 mol”¤L-1µÄĻ”ĮņĖį£¬ŹµŃéŅĒĘ÷ÓŠ£ŗ
¢Ł50 mLĮæĶ² ¢Ś100 mLĮæĶ² ¢ŪĶŠÅĢĢģĘ½ ¢Ü²£Į§°ō
¢Ż250 mLČŻĮæĘæ ¢Ž½ŗĶ·µĪ¹Ü ¢ßÉÕ± ¢ą×¶ŠĪĘæ
ŹµŃ鏱Ź¹ÓĆŃ”ÓĆŅĒĘ÷µÄĻČŗóĖ³ŠņĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲÉśĪļĢåÄŚ»ÆѧŌŖĖŲµÄŠšŹö“ķĪóµÄŹĒ
A. »īĻø°ūÖŠŗ¬Įæ×ī¶ąµÄĪŽ»śĪļÓėŗ¬Įæ×ī¶ąµÄÓŠ»śĪļÖŠ¾łŗ¬H”¢O
B. µ°°×ÖŹÖŠµÄNÖ÷ŅŖ“ęŌŚÓŚėļüÖŠ
C. Ļø°ūÄŚĪ¢ĮæŌŖĖŲ×÷ÓĆÄܱ»ĘäĖüŌŖĖŲĢę“ś
D. ÉśĪļĢåÄŚµÄ»ÆѧŌŖĖŲ¾łÄÜŌŚĪŽ»ś»·¾³ÖŠÕŅµ½
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com