
 液并使它们接近,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性。则
液并使它们接近,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性。则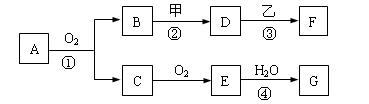
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源:不详 题型:填空题



























| 阳离子 | Na+ Mg2+ Al3+ Ag+ Ba2+ |
| 阴离子 | OH- Cl- SO42- SO32- CO32- |

 为了鉴定其中的离子,现进行如下实验,试根据实验现象和要求填空。
为了鉴定其中的离子,现进行如下实验,试根据实验现象和要求填空。
 (1)取少许该白色固体加水溶解,最后得到无色溶液;用pH试纸检测,溶液的pH为13。则X中一定不存在的离子是_____________。
(1)取少许该白色固体加水溶解,最后得到无色溶液;用pH试纸检测,溶液的pH为13。则X中一定不存在的离子是_____________。
 (2)向溶液中滴加盐酸溶液,刚开始无沉淀,后有沉淀生成,继续滴加沉淀消失,并有无色无味气体逸出。则由(1)和(2)可得出的结论是:X中一定存在的离子有____________;又可确定X中一定不存在的离子有________________。
(2)向溶液中滴加盐酸溶液,刚开始无沉淀,后有沉淀生成,继续滴加沉淀消失,并有无色无味气体逸出。则由(1)和(2)可得出的结论是:X中一定存在的离子有____________;又可确定X中一定不存在的离子有________________。
 (3)若组成X的物质有三种,则可能是(用化学式表示,写出一组即可) ________________。
(3)若组成X的物质有三种,则可能是(用化学式表示,写出一组即可) ________________。
 (4)尚待检验的离子及检验方法是:
(4)尚待检验的离子及检验方法是:| 尚待检验的离子 | 检验方法 |
            | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.164号元素是金属元素 |
| B.164号元素位于ⅣA族 |
| C.164号元素对应的最高价氧化物的水化物其碱性比114号的强 |
| D.164号元素存在稳定的气态氢化物,且还原性比SiH4弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
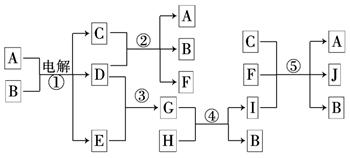
 ____.
____. __________________.
__________________. _.
_.查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na、Mg、Al原子最外层电子数依次增多,所以还原性逐渐增强 |
| B.P、S、Cl元素最高正化合价依次增大,所以最高价氧化物水化物的酸性增强 |
| C.N、O、F原子半径逐渐减小,最外层电子数逐渐增多,所以得电子能力依次增强 |
| D.Li、Na、K的电子层数依次增多,金属性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 A)时,A为: ;
A)时,A为: ;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com