
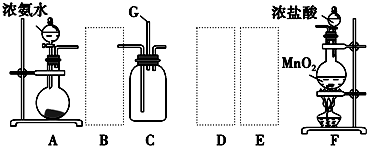
| Ⅰ | Ⅱ | Ⅲ | |
| 备选装置 |  | 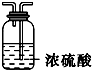 | 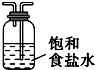 |
分析 (1)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水,注意稀盐酸和二氧化锰不反应;
(2)利用物质溶解时放出的热量促进氨水的挥发来制取氨气,且该物质和氨气不反应;
(3)根据杂质的性质选择除杂装置;
(4)氨气、氯气都能够污染空气,氨气易溶于水,氯气能够与氢氧化钠溶液反应,所以可以用氢氧化钠溶液进行尾气处理.
解答 解:(1)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水,离子反应为MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O,
故答案为:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O;
(2)利用物质溶解时放出的热量促进氨水的挥发来制取氨气,且该物质和氨气不反应,氨气是碱性气体,所以溶解的物质必须是碱性物质,A.碱石灰、B.生石灰、E.烧碱都是碱性物质,且溶解于水时放出热量,C、二氧化硅不溶于水,D.五氧化二磷虽然溶于水时放热,但是酸性物质.
故选A、B、E,
故答案为:ABE;
(3)氨气中混有水蒸气,氨气是碱性气体,要除去水蒸气只能用碱性物质,故B选Ⅰ;制取的氯气中混有氯化氢气体和水蒸气,氯化氢极易溶于水,氯气也能溶于水,所以不能用水除去氯化氢气体;氯气和 水反应生成盐酸和次氯酸,食盐水中含有氯离子,能抑制氯气的溶解,所以要想除去氯气中的氯化氢E应选Ⅲ;水蒸气常用浓硫酸除去,故D选Ⅱ.
故答案为:Ⅰ;Ⅱ;Ⅲ;
(4)氨气、氯气都能够污染空气,氨气易溶于水,氯气能够与氢氧化钠溶液反应,所以可以用氢氧化钠溶液进行尾气处理,反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:氢氧化钠溶液吸收;Cl2+2NaOH=NaCl+NaClO+H2O.
点评 本提考查了氨气、氯气的制备和二者性质的检验,熟悉制备原理、各仪器的作用是解题关键,注意氨根离子检验方法,为高频考点,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 溶质的质量分数ω=$\frac{A}{(A+V)}×100%$ | |
| B. | 溶质的物质的量浓度c=$\frac{1000ρA}{(MA+MV)}mol•{L}^{-1}$ | |
| C. | 1mL该溶液中n(Cl-)=$\frac{nρAV}{M(A+V)}mol$ | |
| D. | 该温度下此盐的溶解度S=$\frac{100A}{V}g$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-、Na+、NO3-、OH- | B. | HCO3-、Cl-、Na+、K+ | ||
| C. | Ba2+、Cl-、SO42-、K+ | D. | NH4+、K+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键 分子间作用力 非极性键 | B. | 氢键 氢键 极性键 | ||
| C. | 氢键 极性键 分子间作用力 | D. | 分子间作用力 氢键 非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3 | B. | BaCl2 | C. | NaOH | D. | Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
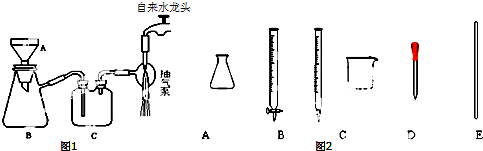
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用高纯硅可以制成光电池,将光能直接转化为电能 | |
| B. | CO、CO2均易于血红蛋白结合而中毒 | |
| C. | SiO2可用于制造光导纤维和半导体 | |
| D. | SiO2和H2O反应可直接制备H2SiO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com