

·ÖĪö ÓŠ»śĪļAÖ»ÓÉĢ¼”¢ĒāĮ½ÖÖŌŖĖŲ×é³ÉĒŅÄÜŹ¹äåĖ®ĶŹÉ«£¬Ęä²śĮææÉŅŌÓĆĄ“ŗāĮæŅ»øö¹ś¼ŅŹÆÓĶ»Æ¹¤·¢Õ¹Ė®Ę½£¬ŌņA½į¹¹¼ņŹ½ĪŖCH2=CH2£¬AŗĶäå·¢Éś¼Ó³É·“Ӧɜ³ÉFĪŖCH2BrCH2Br£¬AŗĶĖ®·¢Éś¼Ó³É·“Ӧɜ³ÉBĪŖCH3CH2OH£¬BÄÜ·¢ÉśŅ»ĻµĮŠŃõ»Æ·“Ӧɜ³ÉŅŅĖį£¬ŌņCĪŖCH3CHO£»
F·¢ÉśĖ®½ā·“Ӧɜ³ÉG£¬DŗĶG·¢Éśõ„»Æ·“Ӧɜ³ÉE£¬øł¾ŻE·Ö×ÓŹ½ÖŖ£¬E½į¹¹¼ņŹ½ĪŖCH3COOCH2CH2OOCCH3£¬½įŗĻĢāÄæ·ÖĪö½ā“š£®
½ā“š ½ā£ŗÓŠ»śĪļAÖ»ÓÉĢ¼”¢ĒāĮ½ÖÖŌŖĖŲ×é³ÉĒŅÄÜŹ¹äåĖ®ĶŹÉ«£¬Ęä²śĮææÉŅŌÓĆĄ“ŗāĮæŅ»øö¹ś¼ŅŹÆÓĶ»Æ¹¤·¢Õ¹Ė®Ę½£¬ŌņA½į¹¹¼ņŹ½ĪŖCH2=CH2£¬AŗĶäå·¢Éś¼Ó³É·“Ӧɜ³ÉFĪŖCH2BrCH2Br£¬AŗĶĖ®·¢Éś¼Ó³É·“Ӧɜ³ÉBĪŖCH3CH2OH£¬BÄÜ·¢ÉśŅ»ĻµĮŠŃõ»Æ·“Ӧɜ³ÉŅŅĖį£¬ŌņCĪŖCH3CHO£»
F·¢ÉśĖ®½ā·“Ӧɜ³ÉG£¬DŗĶG·¢Éśõ„»Æ·“Ӧɜ³ÉE£¬øł¾ŻE·Ö×ÓŹ½ÖŖ£¬E½į¹¹¼ņŹ½ĪŖCH3COOCH2CH2OOCCH3£¬
£Ø1£©AÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü”¢±ūĶéÖŠ²»ŗ¬Ģ¼Ģ¼Ė«¼ü£¬Ģ¼Ģ¼Ė«¼üÄÜŹ¹äåĖ®ĶŹÉ«£¬¶ųĶéĢž²»ÄÜŹ¹äåĖ®ĶŹÉ«£¬ĖłŅŌĘä¼ģŃé·½·ØĪŖ½«ĘųĢå·Ö±šĶØČėäåĖ®ÖŠ£¬ÄÜŹ¹äåĖ®ĶŹÉ«µÄĘųĢåŹĒŅŅĻ©£Ø»ņĘäĖūŗĻĄķ“š°ø£©£¬
¹Ź“š°øĪŖ£ŗ½«ĘųĢå·Ö±šĶØČėäåĖ®ÖŠ£¬ÄÜŹ¹äåĖ®ĶŹÉ«µÄĘųĢåŹĒŅŅĻ©£Ø»ņĘäĖūŗĻĄķ“š°ø£©£»
£Ø2£©ĶعżŅŌÉĻ·ÖĪöÖŖ£¬DÖŠ¹ŁÄÜĶÅĆū³ĘŹĒōČ»ł£¬CµÄ½į¹¹¼ņŹ½ĪŖCH3CHO£¬
¹Ź“š°øĪŖ£ŗōČ»ł£»CH3CHO£»
£Ø3£©DŗĶG·¢Éśõ„»Æ·“Ӧɜ³ÉE£¬·“Ó¦·½³ĢŹ½ĪŖHOCH2CH2OH+2CH3COOH$?_{”÷}^{ÅØĮņĖį}$CH3COOCH2CH2OOCCH3+2H2O£¬
¹Ź“š°øĪŖ£ŗHOCH2CH2OH+2CH3COOH$?_{”÷}^{ÅØĮņĖį}$CH3COOCH2CH2OOCCH3+2H2O£»
£Ø4£©DŹĒōČĖį”¢GŹĒ“¼”¢EŹĒõ„£¬æÉŅŌÓƱ„ŗĶĢ¼ĖįÄĘČÜŅŗ³żČ„õ„ÖŠµÄōČĖįŗĶ“¼£¬DÄÜŗĶĢ¼ĖįÄĘ·“Ӧɜ³ÉæÉČÜŠŌµÄŅŅĖįÄĘ£¬GÄÜČÜÓŚ±„ŗĶĢ¼ĖįÄĘČÜŅŗ£¬E²»ČÜÓŚ±„ŗĶĢ¼ĖįÄĘČÜŅŗ£¬Č»ŗó²ÉÓĆ·ÖŅŗµÄ·½·ØĢį“棬
¹Ź“š°øĪŖ£ŗ±„ŗĶĢ¼ĖįÄĘČÜŅŗ£»·ÖŅŗ£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļĶʶĻ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜ·ÖĪöĶʶĻ¼°ÖŖŹ¶×ŪŗĻŌĖÓĆÄÜĮ¦£¬Ć÷Č·¹ŁÄÜĶż°ĘäŠŌÖŹ¹ŲĻµ”¢ĪļÖŹÖ®¼äµÄ×Ŗ»ÆŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢Ņā£Ø1£©ÖŠ²Ł×÷²½ÖčµÄŹéŠ“ŅŖĢåĻÖ²Ł×÷²½Öč”¢ĻÖĻóŗĶ½įĀŪ£¬ŗܶąŃ§ÉśĶłĶł²»Š“½įĀŪ¶ųµ¼ÖĀ¶Ŗ·Ö£¬ĢāÄæÄŃ¶Č²»“ó£®


 ½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ± pH=7 Ź±£¬Čō V1=V2£¬ŌņŅ»¶ØŹĒ c2£¾c1 | |
| B£® | ŌŚČĪŗĪĒéæöĻĀ¶¼Āś×ć c£ØNa+ £©+c£ØH+ £©=c£ØCH3COO- £©+c£ØOH- £© | |
| C£® | Čō pH£¾7£¬ŌņŅ»¶ØŹĒ c1V1£¾c2V2 | |
| D£® | Čō V1=V2£¬c1=c2£¬Ōņ c£ØCH3COO-£©+c£ØCH3COOH£©=c£ØNa+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉŅŌÓƶ”“ļ¶ūĻÖĻóĒų·ÖČÜŅŗŗĶ½ŗĢå | |
| B£® | ¹čŹĒĮ¼ŗƵİėµ¼Ģå²ÄĮĻ£¬“æ¾»¶žŃõ»Æ¹čŹĒ¹āµ¼ÖĘĘ·µÄ»ł±¾ŌĮĻ | |
| C£® | SO2 Ź¹øßĆĢĖį¼ŲĶŹÉ«ŹĒĄūÓĆ SO2 µÄĘư׊Ō | |
| D£® | ¶ØČŻŹ±ø©ŹÓæĢ¶ČĻߣ¬»įµ¼ÖĀÅضČĘ«øß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
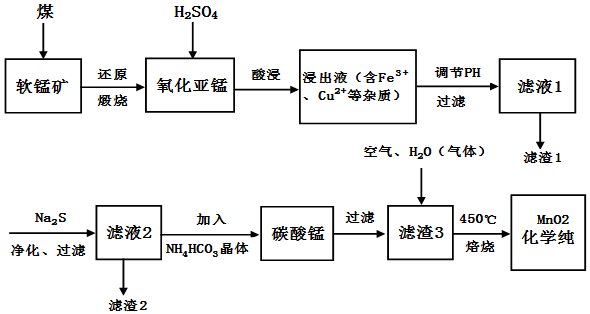
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CaO | B£® | Ca£ØOH£©2 | C£® | SiO2 | D£® | Al2O3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõ»ÆøĘ | B£® | ĻõĖį¼Ų | C£® | øßĆĢĖį¼Ų | D£® | ĻõĖįÄĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
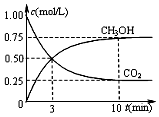 Č¼Ćŗ¼¼ŹõµÄøĽų£¬ÓŠÖśÓŚŗĻĄķæŲÖĘĪĀŹŅŠ§Ó¦”¢»·¾³ĪŪČ¾£¬²¢ÄܽųŠŠ×ŹŌ“»ÆĄūÓĆ£¬»¹æÉÖŲŠĀ»ńµĆČ¼ĮĻ»ņÖŲŅŖ¹¤Ņµ²śĘ·£®¹¤ŅµÉĻŅŌĆŗŗĶĖ®ĪŖŌĮĻĶعżŅ»ĻµĮŠ×Ŗ»Æ±äĪŖĒå½ąÄÜŌ“ĒāĘųŗĶ¹¤ŅµŌĮĻ¼×“¼£®
Č¼Ćŗ¼¼ŹõµÄøĽų£¬ÓŠÖśÓŚŗĻĄķæŲÖĘĪĀŹŅŠ§Ó¦”¢»·¾³ĪŪČ¾£¬²¢ÄܽųŠŠ×ŹŌ“»ÆĄūÓĆ£¬»¹æÉÖŲŠĀ»ńµĆČ¼ĮĻ»ņÖŲŅŖ¹¤Ņµ²śĘ·£®¹¤ŅµÉĻŅŌĆŗŗĶĖ®ĪŖŌĮĻĶعżŅ»ĻµĮŠ×Ŗ»Æ±äĪŖĒå½ąÄÜŌ“ĒāĘųŗĶ¹¤ŅµŌĮĻ¼×“¼£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
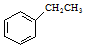 $”ś_{”÷}^{Fe_{2}O_{3}}$
$”ś_{”÷}^{Fe_{2}O_{3}}$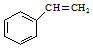 +H2£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
+H2£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ŅŅ±½±½»·ÉĻµÄŅ»ĀČČ”“śĪļÓŠČżÖÖ | |
| B£® | 1mol±½ŅŅĻ©·Ö±šÓė×ćĮæµÄäåĖ®»ņĒāĘų·“Ó¦×ī¶ąĻūŗÄBr2»ņH24mol | |
| C£® | ŅŅ±½·Ö×ÓÖŠ¹²Ę½ĆęµÄĢ¼Ō×Ó×ī¶ąÖ»ÓŠ7øö | |
| D£® | øĆ·“Ó¦ĪŖ»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 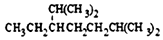 2£¬6-¶ž¼×»ł-5-ŅŅ»łøżĶé | B£® | 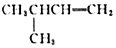 3-¼×»ł-1-¶”Ļ© | ||
| C£® | 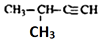 2-¼×»ł-3-¶”Ļ© | D£® | 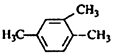 1£¬3£¬4-Čż¼×±½ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com