
| A. | v (C)=3 mol/(L•min) | B. | v (D)=0.5 mol/(L•s) | ||
| C. | v (B)=0.6 mol/(L•s) | D. | v (A)=12 mol/(L•min) |
分析 反应速率的单位相同,用各物质表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快.
解答 解:当反应速率的单位相同,用各物质表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快.
A、v(C)/2=1.5mol/(L•min),
B、υ(D)/2=0.25 mol/(L•s)=15mol/(L•min),
C、v(B)/3=0.2mol/(L•s)=12mol/(L•min),
D、v(A)/1=12mol/(L•min),
所以反应速率v(D)>v(A)=v(B)>v(C).
故选:B.
点评 比较反应速率常用的两种方法:(1)归一法:将同一反应中的不同物质的反应速率转化成同一物质的反应速率,再较小比较.(2)比值法:用各物质的量表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快.
比较反应速率时注意(1)反应速率的单位要相同(2)单位时间内反应物或生成物的物质的量变化大,反应速率不一定快,反应速率是用单位时间内浓度的变化量来表示的.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 理论解释 |
| A | H2S的沸点比H2O的高 | H2S的范德华力大于H2O的范德华力 |
| B | 第一电离能Mg>Al | Mg的3P轨道处于全空状态,能量低,越稳定 |
| C | 熔点Na<Al | 同为金属晶体,Al原子半径小,外围电子多,晶格能大 |
| D | 键的极性:H-O>N-H | 非金属性差异越大,键的极性越小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
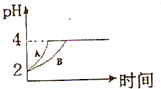 现有室温下浓度均为1×10-3mol/L的几种溶液:①盐酸、②醋酸、③氨水、④NaOH溶液,回答下列问题:
现有室温下浓度均为1×10-3mol/L的几种溶液:①盐酸、②醋酸、③氨水、④NaOH溶液,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、乙烷、丙烷在光照下分别与氯气反应,生成的一氯代物都只有一种 | |
| B. | 等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8 | |
| C. | 苯与溴水混合,反复振荡后溴水层褪色,这是由于发生了取代反应 | |
| D. | 邻二甲苯只有一种结构,证明苯环中不存在碳碳单键和碳碳双键交替的结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
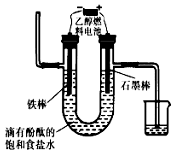 (1)在298K时,1molCH4在氧气中完全燃烧生成二氧化碳和液态水,放出热量890.0kJ.写出该反应的热化学方程式CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.0kJ/mol.现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18克液态水,并放出515kJ热量,则CH4和CO的物质的量分别为0.5mol、0.25mol.
(1)在298K时,1molCH4在氧气中完全燃烧生成二氧化碳和液态水,放出热量890.0kJ.写出该反应的热化学方程式CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.0kJ/mol.现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18克液态水,并放出515kJ热量,则CH4和CO的物质的量分别为0.5mol、0.25mol.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④①②③ | B. | ④③①② | C. | ④①③② | D. | ③②①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
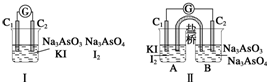
| A. | 甲组操作时,微安表指针不发生偏转 | |
| B. | 甲组操作时,溶液颜色不变 | |
| C. | 乙组操作时,C2作正极 | |
| D. | 乙组操作时,C1上发生的电极反应式为I2+2e-═2I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
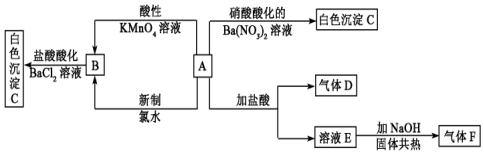
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com