
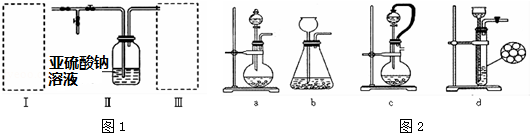
分析 (1)装置Ⅰ中产生的气体为SO2,亚硫酸钠与硫酸反应生成硫酸钠、二氧化硫与水;根据分液漏斗和长颈漏斗的特点结合气压原理来回答;
(2)固体和液体的分离采用过滤法;
(3)二氧化硫属于酸性氧化物,有毒,要处理尾气,容易和氢氧化钠反应生成盐和水;
(4)Na2S2O5与稀硫酸反应生成SO2,反应中S元素的化合价未发生变化,同时生成硫酸钠与水;
(5)检验产品中含有碳酸钠杂质,需加酸反应检验二氧化碳生成,即用的澄清石灰水,但加酸会生成二氧化硫,二氧化硫也能使澄清石灰水变浑浊,故应先除去,用酸性高锰酸钾溶液,并用品红(或酸性高锰酸钾)检验是否除净,或直接用酸性高锰酸钾溶液根据颜色不褪色确定二氧化硫除净;
(6)由消耗碘的量,结合SO2+I2+2H2O═H2SO4+2HI计算二氧化硫的质量,进而计算浓度.
解答 解:(1)装置Ⅰ中亚硫酸钠与硫酸反应生成硫酸钠、二氧化硫与水,反应方程式为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,如果想控制反应速度,用分液漏斗比长颈漏斗好得多,a装置可以,保证气压畅通,液体顺利留下,如图2中还可选用的发生装置是c,
故答案为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;ac;
(2)装置Ⅱ中有Na2S2O5晶体析出,固体和液体的分离采用过滤法,所以要获得已析出的晶体可采取的分离方法是过滤,
故答案为:过滤;
(3)二氧化硫有毒,要处理尾气,属于酸性氧化物,更容易和强碱氢氧化钠反应,饱和食盐水和二氧化硫不反应,浓硫酸不吸收二氧化硫,饱和NaHCO溶液和二氧化硫反应生成二氧化碳,不及氢氧化钠吸收效果好,所以最佳试剂应该选择b,
故答案为:b;
(4)Na2S2O5与稀硫酸反应生成SO2,反应中S元素的化合价未发生变化,同时生成硫酸钠与水,反应离子方程式为:S2O52-+2H+=2SO2↑+H2O,
故答案为:S2O52-+2H+=2SO2↑+H2O;
(5)检验产品中含有碳酸钠杂质,需加酸反应检验二氧化碳生成,即用的澄清石灰水,但加酸会生成二氧化硫,二氧化硫也能使澄清石灰水变浑浊,故应先除去,用酸性高锰酸钾溶液,并用品红(或酸性高锰酸钾)检验是否除净,或直接用酸性高锰酸钾溶液根据颜色不褪色确定二氧化硫除净,检验产品中含有碳酸钠杂质所需试剂是①③⑥或①②③⑥,
故答案为:①③⑥或①②③⑥;
(6)令20mL葡萄酒中二氧化硫的质量为mg,则:
SO2+2H2O+I2═H2SO4+2HI
64g 1mol
mg 0.025L×0.01mol/L
所以,64g:mg=1mol:0.025L×0.0105mol/L,
解得m=0.0168g
故该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为n=$\frac{0.0168g}{0.02L}$=0.84 g/L,
故答案为:0.84.
点评 本题考查物质的制备实验、实验方案设计,为高频考点,侧重于学生的分析能力、实验能力的考查,难度中等,明确实验原理是解本题关键,根据物质的性质分析解答,注意元素化合物知识的积累和灵活运用.


科目:高中化学 来源: 题型:实验题
 如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.
如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 | |
| C. | 化学反应吸收或放出热量的多少与参加反应的物质的多少无关 | |
| D. | C(石墨,s)═C(金刚石,s)△H>0,所以石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 温度 | 0℃ | 10℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
| 溶解度(g) | 125 | 132 | 143 | 213 | 278 | 295 | 312 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
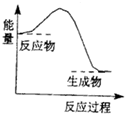
| A. | 生石灰溶于水 | |
| B. | 高温条件下铝与氧化铁的反应 | |
| C. | 高温条件下碳粉与二氧化碳的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4C1固体的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑥⑦ | B. | ②⑤⑦ | C. | ①②⑤⑥⑦ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸盐与盐酸之间的反应 | B. | 一切碳酸盐与一切酸之间的反应 | ||
| C. | 可溶性碳酸盐与强酸之间的反应 | D. | 可溶性碳酸盐与一切酸之间的反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com