
| 选项 | 现象或事实 | 解释 |
| A | 用浸有酸性高锰酸钾溶液的硅藻土作水果保鲜剂 | 酸性高锰酸钾溶液能氧化水果释放的乙烯 |
| B | 高温能杀死流感病毒 | 病毒的蛋白质受热变性 |
| C | 用过氧化钠作呼吸面具中的供氧剂 | 过氧化钠是强氧化剂,能氧化二氧化碳 |
| D | 用Al(OH)3用作塑料的阻燃剂 | A(OH)3分解会吸收热量且产物不能燃烧 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙烯具有催熟作用,能够被高锰酸钾氧化;
B.依据蛋白质的变性的性质解答;
C.过氧化钠与二氧化碳反应产生氧气;
D.Al(OH)3受热分解生成H2O并吸收大量的热量,使周围环境温度降低.
解答 解:A.乙烯具有催熟作用,能够被高锰酸钾氧化,所以用浸有酸性高锰酸钾溶液的硅藻土作水果保鲜剂,故A正确;
B.高温能够使蛋白质变性,故B正确;
C.过氧化钠与二氧化碳反应为歧化反应,过氧化钠既是氧化剂又是还原剂,过氧化钠做供氧剂是因为过氧化钠与水、二氧化碳反应都生成氧气,故C错误;
D.Al(OH)3受热分解生成H2O并吸收大量的热量,使周围环境温度降低,且生成的氧化铝熔点较高,附着在可燃物表面,从而阻止可燃物燃烧,故D正确;
故选C.
点评 本题考查较为综合,涉及物质的性质、用途等知识,为高考常见题型和高频考点,侧重化学与生活的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1L2mol•L-1K2S溶液中S2-和HS-的总数为2NA | |
| B. | 电解精炼铜时,若阴极得电子数为2NA,则阳极质量减少64g | |
| C. | 1mol聚苯乙烯分子有碳碳双键的数目为NA | |
| D. | 1molMg在空气中燃烧生成MgO(含少量Mg3N2)失去电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
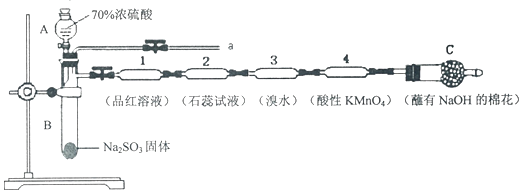
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
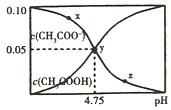 常温下,向1L 0.10mol/L CH3COONa溶液中,不断通入HCl气体(忽略溶液体积变化),得到c(CH3COO-)和c(CH3COOH)与pH的变化关系如图,则下列说法不正确的是( )
常温下,向1L 0.10mol/L CH3COONa溶液中,不断通入HCl气体(忽略溶液体积变化),得到c(CH3COO-)和c(CH3COOH)与pH的变化关系如图,则下列说法不正确的是( )| A. | 溶液的pH比较:x>y>z | |
| B. | 在y点再通入0.05molHCl气体,溶液中离子浓度大小比较:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| C. | 在溶液中加入一滴强酸或强碱,溶液pH变化最小的是y点 | |
| D. | 该温度下,CH3COONa的Kb=10-4.75 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基丁烷也称异丁烷 | |
| B. | 乙醇、糖类和蛋白质都是人体必需的营养物质 | |
| C. |  能发生加成反应和取代反应 能发生加成反应和取代反应 | |
| D. | 合成纤维与光导纤维都属于有机高分子材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,将1mol N2和3mol H2混合发生反应,转移的电子总数为6NA | |
| B. | 30g SiO2中含有的硅氧键数为NA | |
| C. | 向FeI2溶液中通入适量Cl2,当有2mol Fe2+被氧化时,消耗Cl2的分子数为NA | |
| D. | 取50 mL 14.0 mol•L-1 浓硝酸与足量的铜片反应,生成气体分子的数目可能为0.25NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的结构简式为C2H6O | |
| B. | C3H6Cl2有5种同分异构体 | |
| C. | 由苯乙烯生成聚苯乙烯塑料属于加聚反应 | |
| D. | 乙酸溶于水可以电离,属于离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种溶液pH的大小顺序是③>②>① | |
| B. | 若向3种溶液都通入足量二氧化碳,pH变化最大的是② | |
| C. | 若分别加入25mL0.1mol•L-1盐酸后,pH最小的是③ | |
| D. | 若3种溶液的pH均为9,则物质的量浓度的大小顺序是②>①>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
| 反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿空气中 | 一段时间后固体由红色变为绿色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com