
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源:2015-2016学年河北省唐山市高一下期末理科化学试卷(解析版) 题型:选择题
我国计划实现全球卫星通讯需发射77颗卫星,这与铱(Ir)元素的原子核外电子数恰好相等,因此称为“铱星计划”。已知铱的一种同位素是 ,则其核内的中子数是
,则其核内的中子数是
A. 77 B. 114 C. 191 D. 268
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省汕头市高一下期末化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.水分子的比例模型:
B.F-的结构示意图:
C.CO2的结构式:O-C-O
D.中子数为8的碳原子:
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省佛山市高二下期末化学试卷(解析版) 题型:选择题
下列能与文字表述对应且正确的反应方程式是
A.甲烷和氯气在光照条件下反应: 2CH4+Cl2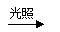 2CH3 Cl +H2
2CH3 Cl +H2
B.实验室用电石制乙炔: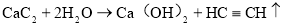
C.用NaOH溶液中和苯酚溶液的酸性:H++OH-===H2O
D.向苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2 C6H5OH+ CO32-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省佛山市高二下期末化学试卷(解析版) 题型:选择题
无机物氰酸铵(NH4OCN)受热可转化为有机物尿素[CO(NH2)2],这一反应的发现使人类踏上了有机合成的征程。下列关于这两种物质的说法中正确的是
A.都属于铵盐
B.都属于离子化合物
C.互为同素异形体
D.互为同分异构体
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期末化学试卷(解析版) 题型:推断题
现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,其中A在常温下能与水发生剧烈反应,B是目前使用最多的金属。物质之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
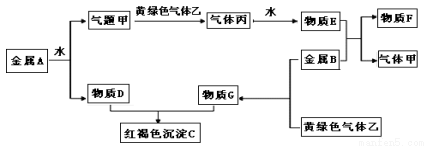
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙 ; F ;
(2)写出下列反应的离子方程式:
①金属A和水反应的离子方程式 。
②D和G的水溶液反应的离子方程式 。
(3)将G浓溶液逐滴加入到沸水中会产生一种红褐色的液体。你认为该液体中的分散质粒子直径在 之间,验证的简单方法是: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期末化学试卷(解析版) 题型:选择题
下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用酒精中
A.②③①④ B.③②①④ C.③①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省五市十校教研教改共同体高二下期末化学试卷(解析版) 题型:实验题
苯甲酸广泛用于医药、食品、染料、化工等领域。以下是实验室制备苯甲酸的一种方法。
反应原理:
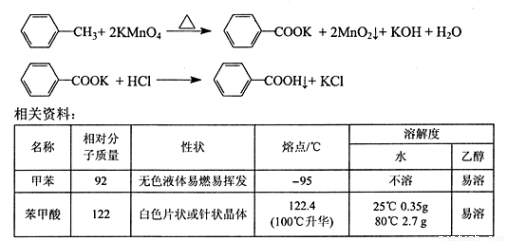
实验步骤:
①下图组装反应装置(冷凝水、夹持及加热装置未画出),并在三颈烧瓶中依次加入120mL水、稍过量高锰酸钾和3.0mL甲苯(密度为0.866g/ mL)。

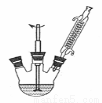
②将三颈烧瓶中的混合液体搅拌、加热至沸腾,直到甲苯完全反应。
③趁热过滤反应混合物。若滤液呈紫色,则需加入适量的亚硫酸氢钠溶液至紫色褪去后再过滤,用热水洗涤滤渣,洗涤液合并至滤液中。
④用冰水冷却滤液,然后用浓盐酸酸化,过滤,用少量冷水洗涤滤渣,得到苯甲酸粗产品,经重结晶得到精制的苯甲酸。
回答下列问题:
(1)仪器a名称为 。
(2)判断甲苯己完全反应的现象是 、回流液不再出现油珠。
(3)实验步骤④中,用少量冷水而不用热水洗涤滤渣的目的是 ;苯甲酸粗产品除了可用重结晶法精制外,还可用 法。
(4)精制的苯甲酸纯度测定:称取1.220g样品,用稀乙醇溶解并配成100 mL溶液,分别取25.00mL溶液,用0.1000 mo1·L-1NaOH标准溶液滴定,三次滴定消耗NaOH溶液的体积分别为V1=22.48mL.V2=22.52 mL.V3= 23.80mL。
①配制溶液时用稀乙醇而不用蒸馏水作溶剂的原因是 。
②若用酚酞作指示剂,确定滴定终点的现象是 。
③产品的纯度为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:填空题
(1)将1.0 mol CH4和2.0molH2O(g)通入容积固定为10 L的反应容器中,在一定条件下发生反应:CH4(g)+H2O(g)  CO (g)+3H2(g) ,测得在一定的压强下CH4的转化率与温度的关系如图1。
CO (g)+3H2(g) ,测得在一定的压强下CH4的转化率与温度的关系如图1。
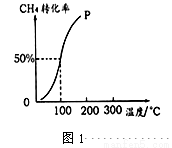
①该反应的ΔH 0(填“>”“<”或“=”)
②假设100 ℃时达到平衡所需的时间为3 min,则用H2表示该反应的平均反应速率为 mol/(L·min)。
③100℃时该反应的平衡常数的数值为 。
④可用来判断该反应达到平衡状态的标志有 (填字母)。
A.CO的含量保持不变
B.CH4浓度与CO浓度相等
C.ν正(CH4)=3ν逆(H2)
D.混合气体的密度保持不变
E.混合气体的总物质的量保持不变
F.混合气体的压强度保持不变
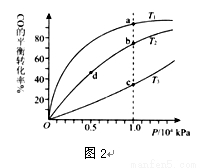
(2)生成甲醇的反应:CO(g)+2H2(g) CH3OH(g) △H =—129.0 kJ/mol,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示。下列说法正确的是 (填字母)。
CH3OH(g) △H =—129.0 kJ/mol,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示。下列说法正确的是 (填字母)。
A.温度:T1>T2 > T3
B.正反应速率:ν(a)>ν(c); ν(b)>ν(d)
C.平衡常数: K(a)>K(c) ; K(b)=K(d)
D.平均摩尔质量:M(a) >M(c); M(b)>M(d)
(3)工业上利用甲醇制备氢气的常用方法之一为:甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)  CO(g)+2H2(g),此反应能自发进行的原因是 。
CO(g)+2H2(g),此反应能自发进行的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com