
【题目】下列有关烷烃性质的叙述不正确的是( )
A. 常温下烷烃与酸、碱、强氧化剂不反应
B. 烷烃都具有还原性,能被氧气氧化
C. 烷烃都能燃烧生成二氧化碳和水
D. 烷烃能使酸性高锰酸钾溶液褪色
科目:高中化学 来源: 题型:
【题目】常见物质之间的转化如下图所示:

其中B常被用于制造光导纤维,其对应的单质的结构与金刚石的结构是相似的。
(1)试推测:A______,F___________(写化学式)
(2)试写出反应④的离子方租式:__________。
(3)写出反应①的化学方程式____________。
(4)在反应①中,碳的作用是______,当生成1molA时,转移电子的数目为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质性质递变中,不能用元素周期律解释的是( )
A.溶解度:MgCO3>Mg(OH)2
B.金属性:Mg<K
C.还原性:H2S<SiH4
D.稳定性:HF>PH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A.开启啤酒瓶后,瓶中立刻泛起大量泡沫
B.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
C.向氯水中加CaCO3后,溶液漂白性增强
D.在含有[Fe(SCN)]2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.在FeCl3和KSCN溶液中存在如下平衡: Fe3+(黄色)+3SCN-(无色)![]() Fe(SCN)3(红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和FeCl3溶液,溶液颜色变_________(填“深”或“浅”,下同),平衡向___________(填“正”或“逆”,下同)方向移动;向另一支试管中滴加 0.01mol/LNaOH 溶液,溶液颜色变__________,平衡向___________方向移动。
Fe(SCN)3(红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和FeCl3溶液,溶液颜色变_________(填“深”或“浅”,下同),平衡向___________(填“正”或“逆”,下同)方向移动;向另一支试管中滴加 0.01mol/LNaOH 溶液,溶液颜色变__________,平衡向___________方向移动。
Ⅱ.在两支容积均为30cm3针筒中分别抽入10cm3NO2 气体,将针筒前端封闭(存在2NO2(红棕色)N2O4(无色)平衡体系)将第二支针筒活塞迅速推至5cm3 处,此时气体的颜色变深,一段时间后气体颜色又变浅了,但仍比第一支针筒气体的颜色深.
①推进针筒后颜色变深,一段时间后又变浅的原因是______________;
②第二支针筒最终比第一支针筒气体颜色深的原因是_____________;
Ⅲ. 现有 a.HCl b.H2SO4 c.CH3COOH
①若三种溶液的物质的量浓度相同,其 C(H+)从大到小依次为____________;(用字母序号表示,下同)
②若三种溶液的的 C(H+)相同,取等体积上述三种溶液,分别用等浓度的NaOH 溶液完全中和,所需 NaOH 溶液体积大小关系为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017上海模拟】升高温度,下列数据不一定增大的是( )
A.化学反应速率v B.弱电解质的电离度α
C.化学平衡常数K D.水的离子积常数Kw
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡 常数 | 温度/℃ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1) 据反应①与②可推导出K1、K2与K3之间的关系,则K3=________(用K1、K2表示)。500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v正__________v逆(填“>”、“=”或“<”)。
(2) 对于反应③,在相同温度和容积不变时,能说明该反应已达平衡状态的是
A.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1
B.容器内压强保持不变
C.H2的消耗速率与CH3OH的消耗速率之比为3∶1
D.容器内的密度保持不变
Ⅱ.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)ΔH<0
2CO2(g)+N2(g)ΔH<0
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 1.00×10-3 | 4.50×10- 4 | 2.50×10- 4 | 1.50×10- 4 | 1.00×10- 4 | 1.00×10- 4 |
c(CO)(mol/L) | 3.60×10- 3 | 3.05×10- 3 | 2.85×10- 3 | 2.75×10- 3 | 2.70×10- 3 | 2.70×10- 3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)前2s内的平均反应速率υ(N2)= ,CO的平衡转化率为____________。(结果均保留两位有效数字)
(2)写出该反应的平衡常数K的表达式________________。
(3)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。某同学设计了三组实验,实验条件已经填在下面实验设计表中。
实验 编号 | T(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | 124 |
①以上三组实验的实验目的是_______________________。
②请在给出的坐标图中,画出上表中的第三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图。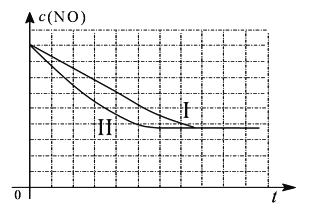
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种新型的固体氧化物型燃料电池,装置如图所示,在两极上分别通入甲烷和空气,电解质是掺杂了 Y2O3的ZrO3固体。在高温熔融状态下能传导O2-。下列说法正确的是
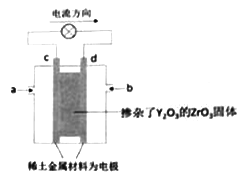
A. a处通入的甲烷
B. 工作时,在熔融电解质中,O2-离子移向d电极
C. c电极为正极,发生氧化反应
D. d电极的电极反应式:O2+4e-=2O2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com