
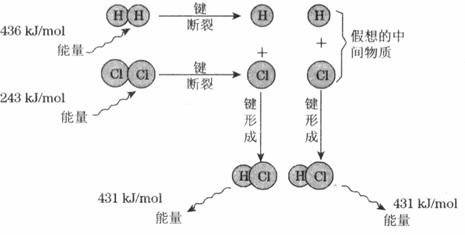
�ٻ�ѧ��������Ҫ____________(��ͷš������ա�)������
��ͼ�й��ͷŵ�����____________kJ��tool��
�۸÷�Ӧ�ķ�Ӧ���������___________(����ڡ������ڡ���С�ڡ�)��Ӧ��������������Ը÷�Ӧ��__________��Ӧ��
����ͼʾ���ݼ����䷴Ӧ�ȣ�д���÷�Ӧ���Ȼ�ѧ����ʽ
___________________________________________________________________��
(2)��֪һ����ѧ����ʽ�������⼸����ѧ����ʽ�Ӽ����õ�����û�ѧ��Ӧ�������仯��Ϊ�⼸����ѧ��Ӧ�����仯�Ĵ����͡�
���У�298 Kʱ
C(s��ʯī)+O2(g)====CO2(g)����H1=-393.5 kJ��mol
CO(g)+��O2(g)====CO2(g)����H3=-283.0 kJ��mol
д��ʯī�������з�Ӧ����һ����̼���Ȼ�ѧ����ʽ
_________________________________________________________________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 C��g��+D��s����Ӱ�죬�ں�����������һ���ݻ�Ϊ10L���ܱ������г���1mol A��1mol B����Ӧ��ƽ��ʱ��������и����ʵ�Ũ��ΪIȻ��ÿ�θı�һ�ַ�Ӧ��������������ʵ�飬���´ﵽƽ��ʱ�����и��ɷֵ�Ũ�ȣ�����D�����ʵ���������ֱ�Ϊ����
C��g��+D��s����Ӱ�죬�ں�����������һ���ݻ�Ϊ10L���ܱ������г���1mol A��1mol B����Ӧ��ƽ��ʱ��������и����ʵ�Ũ��ΪIȻ��ÿ�θı�һ�ַ�Ӧ��������������ʵ�飬���´ﵽƽ��ʱ�����и��ɷֵ�Ũ�ȣ�����D�����ʵ���������ֱ�Ϊ����| A | B | C | D | |
| �� | 0.05mol?L-1 | a mol?L-1 | 0.05mol?L-1 | b mol |
| �� | 0.078mol?L-1 | 0.078mol?L-1 | 0.122mol?L-1 | m mol |
| �� | 0.06mol?L-1 | 0.06mol?L-1 | 0.04mol?L-1 | n mol |
| �� | 0.07mol?L-1 | 0.07mol?L-1 | 0.098mol?L-1 | p mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������2010��2011ѧ���һ������ĩ���Ի�ѧ����(�˽̰�)(�˽̰�) �˽̰� ���ͣ�022
�����ڵ���������Ԫ��A��B��C��D��Eԭ���������α�С��A�ĵ����ڳ�����Ϊ��̬��B��D����ͬһ���壬CΪ��Ȼ�纬�����Ľ���Ԫ�أ�D������������Ϊ������2����EΪ���ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�
(1)A��B��Ԫ�����Ʒֱ�Ϊ________��________��
(2)D��E�����γɶ��ֻ��������һ�ֻ��������Է�������Ϊ28��д����ṹ��ʽ________��
(3)��Ȼ����BԪ�ض������������ʽ���ڣ���д����ҵ����ȡB���ʵĻ�ѧ����ʽ________��
(4)д��ʵ������ȡA����Ļ�ѧ����ʽ________��
(5)a��C���ʺ��������Ļ�����Ϊ���ȷݣ�������һ���м�������NaoH��Һ�������������(�������ͬ)���ΪmL����һ���ڸ�����ǡ����ȫ��Ӧ����������ȴ���������HCl��Һ����������������ΪnL����m��n��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ��ѧ��Ӧ��aA+bB====C,����Ӱ�컯ѧ��Ӧ���ʵ����ؿɵ�v(C)=K��c(A)��m����c��B����n������K�����¶��йصij�����Ϊ���K��m��n��ֵ����298 Kʱ����A��B��Һ����ͬŨ�Ȼ�ϣ��õ��±��е�ʵ�����ݣ�
| ��� |
|
|
|
| 1 | 1.0 | 1.0 | 1.2��10-2 |
| 2 | 2.0 | 1.0 | 2.4��10-2 |
| 3 | 4.0 | 1.0 | 4.9��10-2 |
| 4 | 1.0 | 1.0 | 1.2��10-2 |
| 5 | 1.0 | 2.0 | 4.8��10-2 |
| 6 | 1.0 | 4.0 | 1.9��10-2 |
��1���ɱ����������m��n��K��ֵ��K�ĵ�λ��
��2����a=m,b=n����c(A)=c��B��=2.0 mol��L-1ʱ������B��ʾ�ij�ʼ��Ӧ���ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)�������Li+��I-�Ľ��ư뾶���㻹�������μ��裿
(2)����Li+��I-�Ľ��ư뾶��
(3)������һ�ַ������Li+�İ뾶Ϊ6.0��10-11 ��6.8��10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)�������Li+��I-�Ľ��ư뾶���㻹�������μ��裿
(2)����Li+��I-�Ľ��ư뾶��
(3)������һ�ַ������Li+�İ뾶Ϊ6.0��10-11��6.8��10-11 m������֤��ļ����Ƿ���ȷ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com