
| 1 |
| 2 |
| 1 |
| 2 |
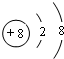 ,故答案为:
,故答案为: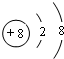 .
.


科目:高中化学 来源: 题型:
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
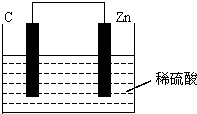 将锌片和碳棒浸入稀硫酸中组成原电池,两电极间连接一个电流计.
将锌片和碳棒浸入稀硫酸中组成原电池,两电极间连接一个电流计.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、②④⑥ |
| C、①③⑥ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg(OH)2+2HCl=MgCl2+2H2O | ||||
| B、Mg2++2OH-=Mg(OH)2↓ | ||||
C、Mg(OH)2
| ||||
D、MgCl2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑤⑥ | B、①②③④ |
| C、①②④ | D、只有② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com