

 B
B D
D .写出D→E的反应的化学方程式
.写出D→E的反应的化学方程式 +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O.
+H2O. 分析 酸性HCl>-COOH>H2CO3>C6H5OH>HCO3-; 中加入碳酸氢钠溶液,因酸性C6H5OH>HCO3-,酚羟基与碳酸氢根离子不反应,但-COOH>H2CO3,羧酸与碳酸氢根离子反应,所以A为
中加入碳酸氢钠溶液,因酸性C6H5OH>HCO3-,酚羟基与碳酸氢根离子不反应,但-COOH>H2CO3,羧酸与碳酸氢根离子反应,所以A为 ,
,
酚羟基具有酸性,能和氢氧化钠反应,生成酚钠盐,所以B为 ,通入二氧化碳,碳酸性比苯酚的酸性强,二氧化碳和酚钠反应生成酚,所以C为
,通入二氧化碳,碳酸性比苯酚的酸性强,二氧化碳和酚钠反应生成酚,所以C为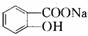 ,酸性HCl>-COOH,加入盐酸,羧酸盐变成羧酸,所以D为
,酸性HCl>-COOH,加入盐酸,羧酸盐变成羧酸,所以D为 ,羧酸和醇发生酯化反应,所以N为
,羧酸和醇发生酯化反应,所以N为 ,以此解答该题.
,以此解答该题.
解答 解:酸性HCl>-COOH>H2CO3>C6H5OH>HCO3-; 中加入碳酸氢钠溶液,因酸性C6H5OH>HCO3-,酚羟基与碳酸氢根离子不反应,但-COOH>H2CO3,羧酸与碳酸氢根离子反应,所以A为
中加入碳酸氢钠溶液,因酸性C6H5OH>HCO3-,酚羟基与碳酸氢根离子不反应,但-COOH>H2CO3,羧酸与碳酸氢根离子反应,所以A为 ,
,
酚羟基具有酸性,能和氢氧化钠反应,生成酚钠盐,所以B为 ,通入二氧化碳,碳酸性比苯酚的酸性强,二氧化碳和酚钠反应生成酚,所以C为
,通入二氧化碳,碳酸性比苯酚的酸性强,二氧化碳和酚钠反应生成酚,所以C为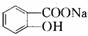 ,酸性HCl>-COOH,加入盐酸,羧酸盐变成羧酸,所以D为
,酸性HCl>-COOH,加入盐酸,羧酸盐变成羧酸,所以D为 ,羧酸和醇发生酯化反应,所以N为
,羧酸和醇发生酯化反应,所以N为 ,反应的方程式为
,反应的方程式为 +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为: ;
; ;
; ;
; +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.
点评 本题考查有机物的推断,涉及酚、醇、羧酸、酯等的性质与转化等,根据羧酸、酚羟基的性质利用题干信息顺推法进行判断,注意对常见官能团的理解掌握,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 LCCl4含有的分子数为NA个 | |
| B. | 500mL 1moL/L的盐酸溶液中含有的HCl分子数为0.5 NA个 | |
| C. | 将1L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA个 | |
| D. | 23gNa与O2反应生成Na2O和Na2O2的混合物,转移的电子数为 NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)3COH的名称:2,2二甲基乙醇 | B. | 甲烷的球棍模型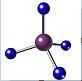 | ||
| C. | 乙醛的结构式:CH3CHO | D. | 四氯化碳分子的电子式: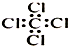 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量均为mg的H2SO4和H3PO4中含有的电子数均为50mNA/98 | |
| B. | 标准状况下,1升辛烷完全燃烧后,所生成气态产物的分子数为8NA/22.4个 | |
| C. | 在1L0.5mol•L-1的Na2CO3溶液中,离子总数一定大于1.5NA个 | |
| D. | 1mol H2O2与MnO2充分作用下转移的电子总数为NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2通入酸性的高锰酸钾溶液中紫红色褪去 | |
| B. | SO2通入Ba(OH)2溶液中中产生白色沉淀 | |
| C. | 久置的Na2SO3溶液中加入酸化的BaCl2溶液产生白色沉淀 | |
| D. | SO2通入氯水中无现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含40.0gNaOH的稀溶液与足量稀醋酸完全中和,放出的热量小于57.3kJ | |
| B. | 2C(s)+2O2(g)═2CO2(g)△H=akJ•mol-1:2C(s)+O2(g)═2CO(g)△H=bkJ•mol-1,则a>b | |
| C. | 氢气的燃烧热为285.5 kJ•mol-1,则水分解的热化学方程式为:2H2O(l)═2H2(g)+O2(g);△H=+285.5 kJ•mol-1 | |
| D. | 已知正丁烷(g)→异丁烷(g)△H<0,则正丁烷比异丁烷稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com