
| A. | 该反应是放热反应,降低温度将缩短反应达到平衡的时间 | |
| B. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 | |
| C. | 单位时间内消耗NO和N2的物质的量比为6:5时,反应达到平衡 | |
| D. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
分析 A.反应为放热反应为放热反应,降低温度反应速率减小反应达到平衡时间增长;
B.催化剂改变反应速率不改变化学平衡;
C.反应速率之比等于化学方程式计量数之比为正反应速率之比,正逆反应速率相同反应达到平衡状态;
D.反应为放热反应,升温平衡逆向进行,平衡常数减小.
解答 解:A.反应为放热反应为放热反应,降低温度反应速率减小反应达到平衡时间增长,降低温度将反应增长达到平衡的时间,故A错误;
B.催化剂改变反应速率不改变化学平衡,废气中氮氧化物的转化率不变,故B错误;
C.反应速率之比等于化学方程式计量数之比为正反应速率之比,正逆反应速率相同反应达到平衡状态,单位时间内消耗NO和N2的物质的量比为6:5时,说明正逆反应速率相同,反应达到平衡状态,故C正确;
D.4NH3(g)+6NO(g)$\frac{\underline{催化剂}}{△}$5N2(g)+6H2O(g)+Q,反应为放热反应,升温平衡逆向进行,平衡常数减小,故D错误;
故选C.
点评 本题考查了化学平衡、化学反应速率的影响因素、平衡常数和平衡状态的分析判断,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 饱和Na2CO3溶液中BaSO4沉淀转化为BaCO3沉淀 | |
| B. | 升高温度,化学平衡发生移动是因为平衡常数改变 | |
| C. | 持续加热,水中MgCO3逐渐转化为更难溶的Mg(OH)2 | |
| D. | 改变一个影响因素使化学平衡发生移动,则平衡常数K值一定变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要求处理垃圾,但是又极力反对建造垃圾焚烧处理厂行为 | |
| B. | 夏天盖着被子吹空调 | |
| C. | 尽量购买本地的、当季的食物,减少食物的加工过程 | |
| D. | 开着5.6L排量的汽车直播声讨北京的雾霾天气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
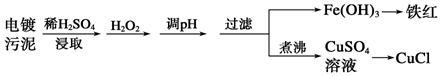
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com