
分析 (1)试管中的液体体积不超过其容积的$\frac{1}{3}$;
(2)用胶头滴管向试管滴液体时,滴管竖直悬空;
(3)不能用水湿润pH试纸,否则稀释了待测溶液,使溶液的酸碱性减弱;
(4)托盘天平的最小刻度为0.1g;
(5)滴定管精确到0.01;
(6)浓硝酸具有强氧化性,见光易分解;
(7)根据C(待测)═$\frac{C(标准)×V(标准)}{V(待测)}$分析误差.
解答 解:(1)加热时,试管中的液体体积不超过其容积的$\frac{1}{3}$,故正确;
(2)用胶头滴管向试管滴液体时,滴管要竖直悬空,滴管尖端不能接触试管内壁,故错误;
(3)用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能用水湿润pH试纸,否则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确,故错误;
(4)托盘天平的最小刻度为0.1g,所以可用托盘天平称量11.7g氯化钠固体,故正确;
(5)滴定管精确到0.01,可量取盐酸32.30mL,故正确;
(6)浓硝酸具有强氧化性,能腐蚀橡胶,不能用橡胶塞,且浓硝酸见光易分解,所以浓硝酸应保存在带玻璃塞的棕色细口试剂瓶中,故错误;
(7)若将锥形瓶用待测液润洗,然后再加入待测液,待测液的物质的量偏大,根据C(待测)═$\frac{C(标准)×V(标准)}{V(待测)}$可知消耗的V(标准)偏多,结果C(待测)偏大,故错误;
故答案为:(1)(4)(5).
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 漂白粉、盐酸、碘酒和液氯都属于混合物 | |
| B. | 向煮沸的1 mol/L NaOH溶液中滴加FeCl3饱和溶液,可制备Fe(OH)3胶体 | |
| C. | 熔融氯化钠,盐酸和铜都能导电,所以都属于电解质 | |
| D. | 一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
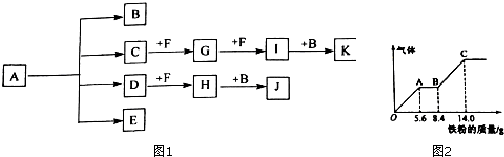
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
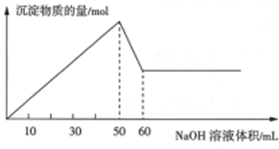
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
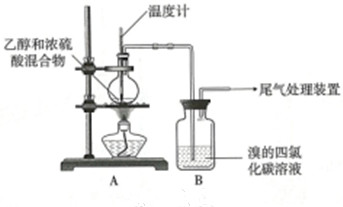
| 操作 | 现象 |
| 点燃酒精灯, 加热至170℃ | a.A中烧瓶内液体渐渐变黑 b.B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕 | c.A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiC | B. | SiO2 | C. | Si | D. | Si3N4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3比NaHCO3易溶于水 | B. | Na2CO3比NaHCO3稳定 | ||
| C. | Na2CO3和NaHCO3都能与盐酸反应 | D. | Na2CO3俗名:小苏打 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com