
| A. |  量取109.3mL稀盐酸 | B. |  称量25g烧碱固体 | ||
| C. |  碳酸氢钠受热分解 | D. | 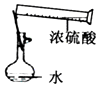 配制一定物质的量浓度的稀硫酸 |
分析 A.量筒规格应大于液体的体积;
B.NaOH潮解,具有腐蚀性,且物体在左盘中;
C.碳酸氢钠分解生成二氧化碳,二氧化碳与石灰水反应生成白色沉淀;
D.不能在容量瓶中稀释浓硫酸.
解答 解:A.量筒规格应大于液体的体积,图中量筒不合理,故A错误;
B.图中NaOH应在左盘小烧杯中称量,故B错误;
C.碳酸氢钠分解生成二氧化碳,二氧化碳与石灰水反应生成白色沉淀,图中装置可说明碳酸氢钠分解,故C正确;
D.不能在容量瓶中稀释浓硫酸,应在烧杯中稀释、冷却后,转移到容量瓶中定容,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握溶液的配制、实验基本操作、物质的性质实验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CO2+H2O═H2CO3 | B. | 2KClO3═2KCl+3O2↑ | ||
| C. | S+O2═SO2 | D. | 2O3═3O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1mol•L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | pH=3的NH4Cl溶液中水的电离程度等于pH=11的氨水溶液中水的电离程度 | |
| C. | 已知Ka(HF)=7.2×10-4,Ka(HCN)=6.2×10-10,等体积等浓度的NaF、NaCN溶液中,前者离子总数小于后者 | |
| D. | 将a mol•L-1 CH3COOH溶液与b mol•L-1 NaOH溶液等体积混合,测得溶液pH为7,则a与b的关系:a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制取乙酸乙酯时,往大试管中依次加入浓硫酸、无水乙醇、冰醋酸 | |
| B. | 检验C2H5Cl中含Cl元素时,将C2H5Cl和NaOH溶液混合加热后,加硫酸酸化,再滴入硝酸银溶液 | |
| C. | 银氨溶液的配制:向洁净的试管里加入1mL2%的稀氨水,边振荡边滴加2%的AgNO3 溶液 | |
| D. | 实验室制得的粗溴苯通常呈黄色,是因为溶解了少量的Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过盐析作用析出的蛋白质固体不溶于水 | |
| B. | 淀粉、纤维素和葡萄糖均可发生水解 | |
| C. | 油脂在酸性条件下的水解反应叫做皂化反应 | |
| D. | 紫外线可使蛋白质变性,可利用紫外线进行消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 可逆反应 FeCl3(aq)+3KSCN(aq)═Fe(SCN)3(aq)+3KCl(aq) 建立平衡后,在其它条件不变时,加入KC1固体,观察体系颜色的变化. | 验证浓度对化学平衡 的影响 |
| B | 相同温度下,将等质量的大理石块、大理石粉末分别加入等体积、等浓度的盐酸和硫酸中,观察气泡产生的快慢. | 验证固体接触面积对 化学反应速率的影响 |
| C | 相同温度下,两支试管中装有等体积、等浓度的H2O2溶液,向其中分别加入少量FeCl3固体和少量MnO2固体. | 验证不同催化剂对 H2O2分解速率的影响 |
| D | 将S02气体通入溴水中,观察溶液颜色的变化 | 证明S02具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | L电子层的电子数为奇数的所有元素都是非金属元素 | |
| B. | 短周期元素X、Y的原子序数相差2,则X、Y不可能处于同一主族 | |
| C. | 从左至右第8、9、10三列元素中没有非金属元素 | |
| D. | 若M+和R2+的核外电子层结构相同,则可推出原子序数:R>M |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com