
 用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法正确的是( )
用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法正确的是( )| A. | 阴极的电极反应式为:Cl-+2OH--2e -=ClO-+H2 O | |
| B. | 阳极的电极反应式为:2CN-+12OH--10e-=N2↑+2CO 32-+6H2O | |
| C. | 电解时使用锂钒氧化物二次电池(V2O5+xLi$?_{充电}^{放电}$LixV2O5)做电源,电池充电时a 电极的电极反应式为:LixV2O5_xe-=V2O5+xLi+ | |
| D. | 除去CN-的反应:2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O |
分析 A.阴极上水失电子生成氢气和氢氧根离子;
B.阳极上氯离子失电子生成氯气,氯气和氢氧根离子反应生成次氯酸根离子和水;
C.电池充电时a电极为阳极,LixV2O5失去电子发生氧化反应;
D.阳极产生的ClO-将CN-氧化为两种无污染的气体,该反应在碱性条件下进行,所以应该有氢氧根离子生成.
解答 解:A.电解质溶液呈碱性,则阴极上水失电子生成氢气和氢氧根离子,电极反应式为2H2O+2e-═H2↑+2OH-,故A错误;
B.阳极上氯离子失电子生成氯气,氯气和氢氧根离子反应生成次氯酸根离子和水,所以阳极反应式为Cl-+2OH--2e-═ClO-+H2O,故B错误;
C.电池充电时a电极为阳极,LixV2O5失去电子发生氧化反应,电极反应式为:LixV2O5_xe-=V2O5+xLi+,故C正确;
D.阳极产生的ClO-将CN-氧化为两种无污染的气体,两种气体为二氧化碳和氮气,该反应在碱性条件下进行,所以应该有氢氧根离子生成,反应方程式为2CN-+5ClO-+H2O═N2↑+2CO2↑+5Cl-+2OH-,故D错误;
故选C.
点评 本题涉及电解原理,明确各个电极上发生的反应及电解原理是解本题关键,注意D中碱性条件下不能有氢离子参加反应或生成.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
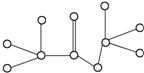
| A. | 分子式为C3H8O2 | |
| B. | 该物质属于酯类 | |
| C. | 该物质可由乙酸与乙醇反应制得 | |
| D. | 该物质含有双键,能跟氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常见的周期表中,共有七个周期,三个短周期、四个长周期 | |
| B. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行 | |
| C. | 短周期元素,是指一、二、三周期,分别有2、8、8种元素 | |
| D. | ⅠA中的金属元素,称为碱金属元素,ⅦA元素又称为卤族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2和SO32-的中心原子均为sp3杂化 | |
| B. | ClO3-的空间构型为三角锥形 | |
| C. | 分子晶体的堆积均采取分子密堆积 | |
| D. | CS2为V形的极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将碳酸钙加入到盐酸中:CO32-+2H+=CO2↑+H2O | |
| B. | 金属钾与水反应:K+H2O=K++OH-+H2↑ | |
| C. | 向稀硝酸中加入少量铜屑:Cu+4H++NO3-=Cu2++2H2O+NO↑ | |
| D. | 向偏铝酸钠溶液中通过量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com