
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ£Ø £©
A. Óɲ»Ķ¬ÖÖŌŖĖŲ×é³ÉµÄ¶ąŌ×Ó·Ö×ÓÖŠÖ»“ęŌŚ¼«ŠŌ¼ü
B. NaOHČÜÓŚĖ®¼ČĘĘ»µĮĖĄė×Ó¼üŅ²ĘĘ»µĮĖ¹²¼Ū¼ü
C. ĮņĖįĒāÄĘŹÜČČČŪČŚŹ±Ö»ĘĘ»µĮĖĄė×Ó¼ü
D. HFÓėHBrĻą±Č£¬HBrµÄ·Šµćøüøß
”¾“š°ø”æC
”¾½āĪö”æA. Óɲ»Ķ¬ÖÖŌŖĖŲ×é³ÉµÄ¶ąŌ×Ó·Ö×ÓÖŠ²»Ņ»¶ØÖ»“ęŌŚ¼«ŠŌ¼ü£¬ĄżČēŅŅ“¼·Ö×ÓÖŠ»¹ÓŠĢ¼Ō×ÓÓėĢ¼Ō×ÓÖ®¼äµÄ·Ē¼«ŠŌ¼ü£¬A“ķĪó£»B. NaOHČÜÓŚĖ®µēĄė³öÄĘĄė×ÓÓėĒāŃõøłĄė×Ó£¬Ö»ĘĘ»µĮĖĄė×Ó¼ü£¬Ć»ÓŠĘĘ»µ¹²¼Ū¼ü£¬B“ķĪó£»C. ĮņĖįĒāÄĘŹÜČČČŪČŚŹ±µēĄė³öÄĘĄė×ÓÓėĮņĖįĒāøłĄė×Ó£¬Ö»ĘĘ»µĮĖĄė×Ó¼ü£¬CÕżČ·£»D. HF·Ö×Ó¼ä“ęŌŚĒā¼ü£¬HFÓėHBrĻą±Č£¬HFµÄ·Šµćøüøߣ¬D“ķĪ󣬓š°øŃ”C”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌųÓŠÖĘŅ©³§Ī„·“¹ę¶Ø£¬¹ŗČė¹¤ŅµÓĆ”°¶žøŹ“¼”±“śĢęŅ½ÓƱū¶ž“¼(C2H8O2)×÷øØĮĻ£¬ÓĆÓŚ”°ĮĮ¾ś¼×ĖŲ×¢ÉäŅŗ”±µÄÉś²ś£¬µ¼ÖĀ¶ąĆū»¼ÕßÉö¹¦ÄÜĖ„ŠŖ¶ųĖĄĶö”£¶žøŹ“¼ÓÖ³ĘŅŅ¶ž“¼ĆŃ£¬·Ö×ÓŹ½ĪŖC4H10O3(HO-CH2-CH2-O-CH2-CH2-OH)£¬¶žøŹ“¼ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ÓĆĶ¾Ź®·Ö¹ć·ŗ”£¶žøŹ“¼Ņ»°ćµÄŗĻ³ÉĀ·ĻßĪŖ£ŗ

Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĻĀĮŠ¹ŲÓŚ”°±ū¶ž“¼ŗĶ”°¶žøŹ“¼”±¼°”°ŅŅ¶ž“¼”±µÄÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ____________
A.±ū¶ž“¼ŹĒŅŅ¶ž“¼µÄĶ¬ĻµĪļ
B.ĖüĆĒ¾ßÓŠĻąĶ¬ÖÖĄąŗĶŹżÄæµÄ¹ŁÄÜĶÅ£¬ŠŌÖŹÉĻĶźČ«ĻąĶ¬
C.”°±ū¶ž“¼”±ŗĶ”°¶žøŹ“¼”±ŌŚ²”ČĖĢåÄŚ¶¼Äܱ»Ńõ»ÆĪŖ²ŻĖį
D.·ÖĄė”°±ū¶ž“¼”±ŗĶ”°¶žøŹ“¼”±æɲÉÓĆ·ÖŅŗµÄ·½·Ø
£Ø2£©¹ż³ĢIŹĒŹÆÓĶ¼Ó¹¤ÖŠ³£ÓĆ²½Öč£¬ĘäĆū³ĘĪŖ_______”£
£Ø3£©“ÓĪļÖŹBµ½ĪļÖŹCµÄ¹ż³ĢČē¹ūĢõ¼žæŲÖĘ²»ŗĆ»įÉś³ÉĪļÖŹE£¬EæÉÓĆÓŚ½šŹōµÄĒŠøī£¬Š“³öŹµŃéŹŅÖʱøEµÄ»Æѧ·½³ĢŹ½___________£¬ŌņĪŖĮĖÄܵƵ½¶žøŹ“¼D£¬ĪļÖŹBµ½ĪļÖŹCµÄ·“Ó¦Ģõ¼žŹĒ_________£¬øĆ·“Ó¦ŹōÓŚ________(Ģī·“Ó¦ĄąŠĶ)”£Š“³öBæÉÄÜÉś³ÉEµÄ»Æѧ·½³ĢŹ½______”£
£Ø4£©·“Ó¦¢óµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ____________”£
£Ø5£©AµÄŅ»ÖÖĶ¬ĻµĪļ½į¹¹¼ņŹ½ĪŖ ĒėÓĆĻµĶ³ĆüĆū·Ø¶ŌĘäĆüĆū_______________”£
ĒėÓĆĻµĶ³ĆüĆū·Ø¶ŌĘäĆüĆū_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æW”¢X”¢Y”¢ZŹĒĖÄÖÖ³£¼ūµÄ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×Ó°ė¾¶ĖęŌ×ÓŠņŹż±ä»ÆČēĶ¼ĖłŹ¾”£ŅŃÖŖWµÄŅ»ÖÖŗĖĖŲµÄÖŹĮæŹżĪŖ18£¬ÖŠ×ÓŹżĪŖ10£»XŗĶNeŌ×ÓµÄŗĖĶāµē×ÓŹżĻą²īl£»YµÄµ„ÖŹŹĒŅ»ÖÖ³£¼ūµÄ°ėµ¼Ģå²ÄĮĻ£»ZµÄ·Ē½šŹōŠŌŌŚĶ¬ÖÜĘŚŌŖĖŲÖŠ×īĒ攣ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
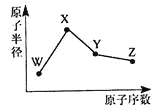
A. ¶ŌÓ¦¼ņµ„Ąė×Ó°ė¾¶£ŗW>X
B. ¶ŌÓ¦ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗY<Z
C. »ÆŗĻĪļXZW¼Čŗ¬Ąė×Ó¼ü£¬ÓÖŗ¬¹²¼Ū¼ü
D. ZµÄĒā»ÆĪļŗĶXµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄČÜŅŗ¾łÄÜÓėYµÄŃõ»ÆĪļ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ĪļÖŹµÄĮæŹĒøßÖŠ»Æѧ֊³£ÓƵÄĪļĄķĮ棬ĒėĶź³ÉÓŠ¹ŲĘäÄŚČŻµÄĢīæÕ£ŗ
¢Ł15.6 gNa2Xŗ¬ÓŠ0.4molNa+£¬Na2XµÄĦ¶ūÖŹĮæĪŖ_____________£¬ŗ¬X 3.2gµÄNa2X µÄĪļÖŹµÄĮæĪŖ_____________”£
¢ŚĮņĖį¼ŲŗĶĮņĖįĀĮµÄ»ģŗĻČÜŅŗ£¬ŅŃÖŖĘäÖŠAl3+µÄÅضČĪŖ0.4 mol/L£¬ĮņĖįøłĄė×ÓÅØ¶Č ĪŖ0.75 mol/L£¬ŌņK+µÄĪļÖŹµÄĮæÅضČĪŖ__________”£
£Ø2£©ÓŠŅŌĻĀ¼øÖÖĪļÖŹ£ŗ¢Ł“æH2SO4£¬¢ŚĻõĖį¼ŲČÜŅŗ£¬¢ŪĶ£¬¢Ü¶žŃõ»ÆĢ¼£¬¢Ż¾Ę¾«£¬¢ŽĢ¼ĖįĒāÄĘ¹ĢĢ壬¢ßÕįĢĒ£¬¢ąNaCl¾§Ģ壬¢į°±Ė®£¬¢āČŪČŚKCl”£
ŅŌÉĻÄܵ¼µēµÄŹĒ________________________£ØĢīŠņŗÅ£¬ĻĀĶ¬£©£»
ŅŌÉĻŹōÓŚµē½āÖŹµÄŹĒ_________________£»ŹōÓŚ·Ēµē½āÖŹµÄŹĒ______________”£
Š“³öŹōÓŚĖįŹ½ŃĪµÄĪļÖŹČÜÓŚĖ®ŗóµÄµēĄė·½³ĢŹ½_____________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬ŌŚŅ»¶ØĢõ¼žĻĀ¼ČÄÜ·¢ÉśĖ®½ā·“Ó¦£¬ÓÖÄÜ·¢ÉśŅų¾µ·“Ó¦µÄŹĒ
A.ÕįĢĒB.ĘĻĢŃĢĒC.ŅŅĖįŅŅõ„D.ĀóŃæĢĒ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
A. ŗ¬ÓŠ¹²¼Ū¼üµÄ»ÆŗĻĪļŅ»¶ØŹĒ¹²¼Ū»ÆŗĻĪļ B. ŌŚ¹²¼Ū»ÆŗĻĪļÖŠŅ»¶Øŗ¬ÓŠ¹²¼Ū¼ü
C. ŗ¬ÓŠĄė×Ó¼üµÄ»ÆŗĻĪļŅ»¶ØŹĒĄė×Ó»ÆŗĻĪļ D. Ė«Ō×Óµ„ÖŹ·Ö×ÓÖŠµÄ¹²¼Ū¼üŅ»¶ØŹĒ·Ē¼«ŠŌ¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹµÄČÜŅŗÄܵ¼µē£¬µ«²»ŹōÓŚµē½āÖŹµÄŹĒ£Ø £©
A. Ba(OH)2 B. ÕįĢĒ C. Cl2 D. HCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖŌŖĖŲµÄŌ×ÓŠņŹż£¬æÉŅŌĶĘÖŖŌ×ӵĢŁÖŠ×ÓŹż ¢ŚŗĖµēŗÉŹż ¢ŪŗĖĶāµē×ÓŹż ¢ÜŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ£¬ĘäÖŠÕżČ·µÄŹĒ( )
A. ¢Ł¢Ū B. ¢Ś¢Ū C. ¢Ł¢Ś¢Ū D. ¢Ś¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. ½šŹōÓė·Ē½šŹōŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļŅ»¶ØŹĒĄė×Ó»ÆŗĻĪļ
B. øɱłĘų»Æ¹ż³ĢÖŠÖ»ŠčæĖ·ž·Ö×Ó¼ä×÷ÓĆĮ¦
C. HFµÄČČĪČ¶ØŠŌŗÜŗĆ£¬ŹĒŅņĪŖHF·Ö×Ó¼ä“ęŌŚĒā¼ü
D. ³£ĪĀ³£Ń¹ĻĀ£¬ĘųĢ¬µ„ÖŹ·Ö×ÓÖŠ£¬ĆæøöŌ×ÓµÄ×īĶā²ć¶¼¾ßÓŠ8µē×ÓĪČ¶Ø½į¹¹
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com