

| A.放电时,负极质量增加 |
| B.充电时,应将外接直流电源的正极与蓄电池的铅电极相接 |
C.放电时,正极反应为: |
| D.铅蓄电池做电源电解Na2SO4溶液时,当有lmolO2产生时,消耗4molH2SO4 |
 2H2↑+O2↑当有lmolO2产生时,转移电子4NA,由于在整个回路中电子转移数目相等,所以在内电路也转移电子4NA。由电池的反应式可知:每消耗2摩尔H2SO4,转移电子2NA,所以共消耗4molH2SO4。正确。
2H2↑+O2↑当有lmolO2产生时,转移电子4NA,由于在整个回路中电子转移数目相等,所以在内电路也转移电子4NA。由电池的反应式可知:每消耗2摩尔H2SO4,转移电子2NA,所以共消耗4molH2SO4。正确。

 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源:不详 题型:单选题
| A.轮船水线以下的船壳上镶嵌有一定量的锌块 |
| B.镀锌的铁制品比镀锡的铁制品耐用 |
| C.埋在潮湿疏松土壤里的铁管比干燥致密不透气的土壤里的铁管更易被腐蚀 |
| D.在空气中,金属镁、铝的表面可形成一层氧化膜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用电解法精炼粗铜时粗铜作阳极 |
| B.在镀件上镀铜时纯铜作阴极 |
| C.在海轮的外壳上装上铜块可以减缓船体的腐蚀 |
| D.铜的金属活动性比铁弱,因此可用铜罐代替铁罐储运浓硝酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.负极发生的反应为:Fe-2e-===Fe2+ |
| B.正极发生的反应为:2H2O+O2+2e-=4OH- |
| C.钢和铁都是铁合金,所以它们的组成基本相同 |
| D.插在水中的钢柱在水下部分比在空气与水交界处更容易腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe - 2e—=Fe2+ | B.O2+4e-+2H2O=4OH- |
| C.4OH- - 4e-=O2↑+2H2O | D.4Fe(OH)2+O2+2H2O =4Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
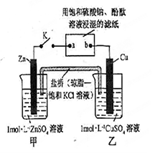
A.电子沿Zn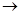 a a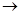 b b Cu路径流动 Cu路径流动 |
| B.片刻后可观察到滤纸b点变红色 |
| C.片刻后甲池中c(SO42-)增大 |
D. 电极上发生还原反应 电极上发生还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
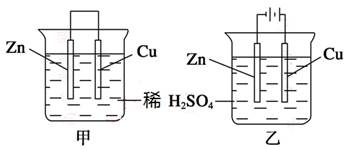
| A.甲、乙装置中的锌片都作负极 |
| B.甲、乙装置中的溶液内的H+在铜片被还原 |
| C.甲、乙装置中锌片上发生的反应都是还原反应 |
| D.甲装置中铜片有气泡生成,乙装置中的铜片质量减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.当右槽溶液颜色由绿色变为紫色时,电池中能量转化形式为化学能转化为电能 |
| B.充电过程中,a极的反应式为VO2+—e—+H2O=VO2++2H+ |
| C.储能电池a、b两极间的电解质溶液中通过电子的定向移动形成闭合回路 |
| D.放电时,当转移的电子数为6.02×1023时,从右槽迁移进入左槽的H+的物质的量为2mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com