
【题目】A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子化合物;B与Z的最外层电子数之比2:3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。请回答下列问题。
(1)Z的原子结构示意图为 ;化合物BA4的电子式为 。
(2)化合物Y2X2中含有的化学键类型有 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)化合物A2X和A2Z中,沸点较高的是 (填化学式),其主要原因是 。
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为 。
【答案】(1)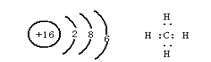
(2)A、C(3)H2O;水分子间存在氢键
(4)4H2O2+H2S=H2SO4+4H2O或H2O+H2S=S↓+2H2O
【解析】试题分析:A、B、C、X、Y和Z是原子序数依次递增的短周期元素,X与Z同主族,结合原子序数可知,X处于第二周期,Z处于第三周期,A与Y同主族,而Y的原子序数大于X,则Y只能处于第三周期,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红,Y2X2为Na2O2,X为O元素,Y为Na,可推知Z为S元素;A与B和A与X均可形成10个电子的化合物,则A为H元素;B与Z的最外层电子数之比为2:3,则B元素的最外层电子数为4,而B、C均处于第二周期,故B为碳元素,C的原子序数介于碳、氧之间,则C为N元素。
(1)Z为S元素,原子结构示意图为 ;A与B所形成的化合物CH4的电子式为
;A与B所形成的化合物CH4的电子式为 ;
;
(2)化合物Na2O2属于离子化合物,含有的化学键是:离子键、非极性共价键,答案选AC;
(3)H2O分子之间存在氢键,H2S分子之间不能形成氢键,沸点较高的是H2O;
(4)H与O和H与S均能形成18个电子的化合物,此两种化合物反应可以生成S单质和一种10电子化合物,应是H2O2与H2S反应生成S与H2O,反应的化学方程式为4H2O2+H2S=H2SO4+4H2O或H2O+H2S=S↓+2H2O。


科目:高中化学 来源: 题型:
【题目】在空气中直接蒸发下列盐的溶液:①Fe2(SO4)3②Na2CO3③KCl④CuCl2⑤NaHCO3可以得到相应盐的晶体(可以含有结晶水)的是( )
A.①③⑤
B.①②③
C.②④
D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积的两容器内,一个盛CH4,另一个盛NH3,若容器内温度、压强相同,则两容器内所盛气体比较,结论不正确的是
A.氢原子个数比为4∶3B.原子个数比为5∶4
C.分子个数比为1∶1D.密度比为17∶16
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣889.6kJ/mol.
(1)反应物能量总和_____(填“大于”、“小于”或“等于”)生成物能量总和.
(2)若1mol甲烷完全燃烧生成二氧化碳和水蒸气,则放出的热量_____889.6kJ.(填“>”、“<”或“=”)
(3)已知氢气燃烧生成液态水的热化学方程式是:2H2(g)+O2(g)=2H2O(l)△H=﹣572kJ/mol,则相同质量的甲烷和氢气,完全燃烧生成液态水,放热较多的是_____.
(4)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.
①已知甲烷燃料电池的总反应式为CH4+2O2+2KOH═K2CO3+3H2O,通入甲烷的这个电极是_____(填“正极”或“负极”),其另外一电极上的电极反应式为:__________________.
②通常情况下,甲烷燃料电池的能量利用率_____(填“大于”、“小于”或“等于”)甲烷燃烧的能量利用率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中可以大量共存的是
A.Na+、Fe3+、SO42-、SCN-B.K+ 、OH-、AlO2-、Cl-
C.H+ 、Na+、Fe2+、MnO4-D.Na+、H+、HCO3-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示.下列说法不正确的是( )
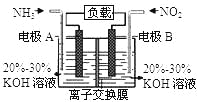
A. 电流从右侧电极经过负载后流向左侧电极
B. 为使电池持续放电,离子交换膜需选用阴离子交换膜
C. 电极A极反应式为:2NH3-6e-=N2+6H+
D. 当有4.48L NO2(标准状况) 被处理时,转移电子为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3和纯净的O2在一定条件下发生反应:4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g),现向一容积不变的2L密闭容器中充入4mol NH3和3mol O2,4min后,测得生成的H2O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确的是
2N2(g)+6H2O(g),现向一容积不变的2L密闭容器中充入4mol NH3和3mol O2,4min后,测得生成的H2O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确的是
A. v(O2)=0.225 mol·L-1min-1
B. v(H2O)=0.375 mol·L-1min-1
C. v(N2)=0.125 mol·L-1min-1
D. v(NH3)=0.250 mol·L-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED系列产品是一类新型节能产品。图甲是NaBH4/H2O2燃料电池,图乙是LED发光二极管的装置示意图。下列叙述错误的是

A.电池A极区的电极反应式为:H2O2+2e-=2OH-
B.电池放电过程中,Na+从负极区向正极区移动
C.每有1mol NaBH4参加反应转移电子数为4NA
D.要使LED发光二极管正常发光,图乙中的导线a应与图甲中的B极相连
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com