
【题目】NaCl溶液的电解产物可用于生产盐酸、漂白粉、氢氧化钠等产品。下列说法错误的是
A. HCl的电子式:![]()
B. NaOH中既含离子键又含共价键
C. 电解NaCl溶液时,阴极区pH增大的原因:2H2O +2e-=2OH-+H2↑
D. 漂白粉露置在空气中:Ca(ClO)2+CO2+H2O=CaCO3+2HClO
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F都是链状有机物,它们的转化关系如图所示。A是一种氯代烃,只含有一种官能团,D中含有两种官能团,D分子中不含甲基,且与碳原子相连的氢原子取代所得的一氯代物只有1种。请回答下列问题:

(1)D的分子式 ___________________。
(2)写出D的结构简式____________________,A的结构简式_________________。
(3)写出B生成C的化学方程式 _________________________________。
(4)写出C与新制氢氧化铜悬浊液反应的化学方程式_____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想以N2和H2为反应物,以溶有X的稀盐酸为电解质溶液,制造出新型燃料电池,装置如图所示。下列说法正确的是
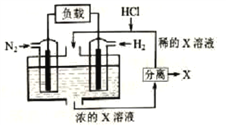
A. 放电时H+向左移动,生成的物质X是NH4Cl
B. 通入H2的一极为正极
C. 通入N2的电极反应为:N2+6H+-6e-=2NH3
D. 放电过程右边区域溶液pH逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,发生如下反应:CO(g)+2H2(g)![]() CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1mol CO和2 molH2,向乙中加入2 molCO和4molH2, 测得不同温度下CO的平衡转化率如图2所示。下列说法正确的是
CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1mol CO和2 molH2,向乙中加入2 molCO和4molH2, 测得不同温度下CO的平衡转化率如图2所示。下列说法正确的是

A. 该反应的ΔH> 0; P1> P2 B. 反应速率B点高于D点
C. A、C两点的平衡常数相同 D. M、L两点中,CH3OH的体积分数相同,且p(M)= 2p(L)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的“氧化物”样品,用5mol/L盐酸0.14L恰好完全反应,所得溶液还能吸收标准状况下2.24L氯气,使其中Fe2+全部转化为Fe3+.该样品可能的化学式是( )
A. Fe5O6 B. Fe3O4 C. Fe6O7 D. Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1molL-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图 所示。下列判断正确的是
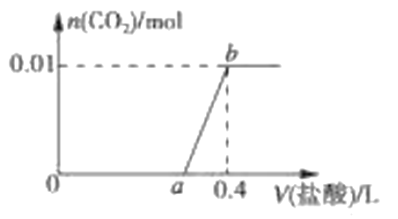
A. 在0a范围内,只发生NaOH和HCl的反应
B. ab段发生反应的离子方程式为:CO32-+2H+=CO2↑+H2O
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芦笋中的天冬酰胺(结构如下图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。

(1)天冬酰胺所含元素中,________(填元素名称)元素基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有________种。
(3)H2S和H2Se的参数对比见下表。
化学式 | 键长/nm | 键角 | 沸点/℃ |
H2S | 1.34 | 92.3° | -60.75 |
H2Se | 1.47 | 91.0° | -41.50 |
①H2Se分子中含有的共价键类型为_____________(填“σ”或“π”)。
②H2S的键角大于H2Se的原因可能为______________________________。
③H2Se的酸性比H2S________(填“强”或“弱”)。
(4)已知钼(Mo)位于第五周期ⅥB族,钼、铬、锰的部分电离能如下表所示:
编号 | I5/kJ·mol-1 | I6/kJ·mol-1 | I7/kJ·mol-1 | I8/kJ·mol-1 |
A | 6990 | 9220 | 11500 | 18770 |
B | 6702 | 8745 | 15455 | 17820 |
C | 5257 | 6641 | 12125 | 13860 |
A是____________(填元素符号),B的价电子排布式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带中含有丰富的碘元素,碘元素以I-的形式存在。实验室从海带中提取碘的流程如图所示:

(1)指出提碘的过程中有关的实验操作名称:①________,③________,④________。
(2)操作③、④可以分解为如下几步:
A.旋开活塞,用烧杯盛接溶液
B.从分液漏斗上口倒出上层溶液
C.打开分液漏斗上口玻璃塞或使塞上的凹槽对准漏斗上口的小孔
D.静置,分层 E.把盛有溶液的分液漏斗放在铁架台的铁圈上
F.把 50 mL 碘水和 15 mL 苯加入分液漏斗中,盖好玻璃塞
G.检查分液漏斗是否漏液 H.倒转分液漏斗,振荡
(ⅰ)正确的操作顺序是:G→________→________E→D→________→________→B。
(ⅱ)能选用苯作萃取剂的原因是_____________________________________。
(ⅲ)上述(C)这样操作的目的是________________________________________。
(3)流程图中,将操作④后的________层液体(填“上”或“下”)用上图仪器进行操作⑤,写出仪器的名称:X_______、Y___________。请指出上图装置中存在的一处错误:_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com