
”¾ĢāÄæ”æĻĀĮŠ“ėŹ©ÄÜĆ÷ĻŌŌö“óŌ·“Ó¦µÄ»Æѧ·“Ó¦ĖŁĀŹµÄŹĒ
A. C£Øs£©+ CO2 ![]() 2CO·“Ó¦ÖŠ£¬Ōö“óCµÄĮæ
2CO·“Ó¦ÖŠ£¬Ōö“óCµÄĮæ
B. ½«Ļ”H2SO4øÄĪŖ98%µÄÅØH2SO4ÓėZn·“Ó¦ÖĘČ”H2
C. ŌŚH2SO4ÓėNaOHĮ½ČÜŅŗ·“Ó¦Ź±£¬Ōö“óŃ¹Ēæ
D. ŗćĪĀŗćČŻĢõ¼žĻĀ£¬ŌŚ¹¤ŅµŗĻ³É°±·“Ó¦ÖŠ£¬Ōö¼ÓµŖĘųµÄĮæ
”¾“š°ø”æD
”¾½āĪö”æAĻī£¬C³Ź¹ĢĢ¬£¬Ōö“óCµÄĮæ²»ÄÜŌö“ó·“Ó¦ĖŁĀŹ£»BĻī£¬ZnÓėÅØH2SO4·“Ó¦·Å³öSO2£»CĻī£¬H2SO4ÓėNaOHĮ½ČÜŅŗµÄ·“Ó¦ÖŠ£¬·“Ó¦Īļ֊ƻӊĘųĢ壬Ōö“óŃ¹Ēæ²»ÄÜŌö“ó·“Ó¦ĖŁĀŹ£»DĻī£¬Ōö“ó·“Ó¦ĪļÅØ¶Č£¬Ōö“ó»Æѧ·“Ó¦ĖŁĀŹ”£
AĻī£¬C³Ź¹ĢĢ¬£¬Ōö“óCµÄĮæ²»ÄÜŌö“ó·“Ó¦ĖŁĀŹ£¬AĻī“ķĪó£»BĻī£¬ÅØH2SO4¾ßÓŠĒæŃõ»ÆŠŌ£¬ZnÓėÅØH2SO4·“Ó¦·Å³öSO2£¬²»»į·Å³öH2£¬BĻī“ķĪó£»CĻī£¬H2SO4ÓėNaOHĮ½ČÜŅŗµÄ·“Ó¦ÖŠ£¬·“Ó¦Īļ֊ƻӊĘųĢ壬Ōö“óŃ¹Ēæ²»ÄÜŌö“ó·“Ó¦ĖŁĀŹ£¬CĻī“ķĪó£»DĻī£¬Ōö“ó·“Ó¦ĪļN2µÄÅØ¶Č£¬Ōö“ó»Æѧ·“Ó¦ĖŁĀŹ£¬DĻīÕżČ·£»“š°øŃ”D”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøßĪĀĻĀ£¬Ä³·“Ó¦Ę½ŗā³£ŹżK= ![]() £®ŗćČŻĢõ¼žĻĀ“ļµ½Ę½ŗāŹ±£¬ĪĀ¶ČÉżøßH2ÅØ¶Č¼õŠ”£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
£®ŗćČŻĢõ¼žĻĀ“ļµ½Ę½ŗāŹ±£¬ĪĀ¶ČÉżøßH2ÅØ¶Č¼õŠ”£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
A.øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCO+H2O ![]() CO2+H2
CO2+H2
B.øĆ·“Ó¦µÄģŹ±äĪŖÕżÖµ
C.ŗćĪĀŗćČŻĻĀ£¬Ōö“óŃ¹Ē棬H2ÅضČŅ»¶Ø¼õŠ”
D.ÉżøßĪĀ¶Č£¬Ę½ŗāÓŅŅĘ£¬Äę·“Ó¦ĖŁĀŹ¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĖ£ØU£©ŹĒŅ»ÖÖĻ”ÓŠ½šŹō£¬ÖĘŌģĒāµÆµÄÖŲŅŖŌĮĻ”£ĢįČ”ÓĖÉę¼°µÄ·“Ó¦ĪŖ£ŗUF4+ 2Mg![]() U + 2MgF2”£ŌŚøĆ·“Ó¦ÖŠ£¬×÷ĪŖ»¹Ō¼ĮµÄĪļÖŹŹĒ______£¬±»»¹ŌµÄĪļÖŹŹĒ______£»Čō·“Ó¦ÖŠĻūŗÄ1 mol Mg£¬ŌņÉś³ÉU______mol”£
U + 2MgF2”£ŌŚøĆ·“Ó¦ÖŠ£¬×÷ĪŖ»¹Ō¼ĮµÄĪļÖŹŹĒ______£¬±»»¹ŌµÄĪļÖŹŹĒ______£»Čō·“Ó¦ÖŠĻūŗÄ1 mol Mg£¬ŌņÉś³ÉU______mol”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. 18 g D2OĖłŗ¬µÄµē×ÓŹżĪŖ10NA
B. 1 mol H2O2ÖŠŗ¬ÓŠ¼«ŠŌ¼üµÄŹżÄæĪŖ3NA
C. ±ź×¼×“æöĻĀ£¬22.4 LĖÄĀČ»ÆĢ¼Ėłŗ¬·Ö×ÓŹżĪŖNA
D. 32g O2ŗĶO3µÄ»ģŗĻĪļÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ2NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµē½āÖŹČÜŅŗÓėČĖĄąÉś»īĻ¢Ļ¢Ļą¹Ų£¬Ēė»Ų“šĻĀĮŠĪŹĢā
£Ø1£©Ä³ĪĀ¶ČĻĀ£¬Kw=1”Į10©12£Ø molL©1£©2 £¬ Čō±£³ÖĪĀ¶Č²»±ä£¬ĻņĖ®ÖŠµĪČėĻ”ĮņĖįĒ”ŗĆŹ¹ČÜŅŗÖŠc£ØH+£©/c£ØOH©£©=1”Į1010 £¬ Ōņ“ĖŹ±Ė®µēĄė³öµÄc£ØH+£©=molL©1 £®
£Ø2£©³£ĪĀĻĀČōČÜŅŗÓÉpH=3µÄHAČÜŅŗV1 mLÓėpH=11µÄNaOHČÜŅŗV2 mL»ģŗĻ¶ųµĆ£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £®
A.Čō»ģŗĻŗóČÜŅŗ³ŹÖŠŠŌ£¬Ōņc£ØH+£©+c£ØOH©£©=2”Į10©7mol/L
B.ČōV1=V2 £¬ »ģŗĻŗóČÜŅŗµÄpHŅ»¶ØµČÓŚ7
C.Čō»ģŗĻŗóČÜŅŗ³ŹĖįŠŌ£¬ŌņV1Ņ»¶Ø“óÓŚV2
D.Čō»ģŗĻŗóČÜŅŗ³Ź¼īŠŌ£¬ŌņV1Ņ»¶ØŠ”ÓŚV2
£Ø3£©ĻĀĮŠĒśĻßÖŠ£¬æÉŅŌĆčŹöŅŅĖį£Ø¼×£¬Ka=1.8”Į10©5 mol/L£©ŗĶŅ»ĀČŅŅĖį£ØŅŅ£¬Ka=1.4”Į10©3 mol/L£©ŌŚĖ®ÖŠµÄµēĄė¶ČÓėÅØ¶Č¹ŲĻµµÄŹĒ £® 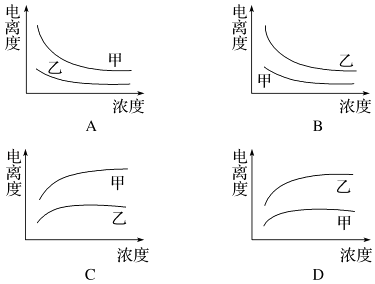
£Ø4£©ŌŚĻĀĮŠŹµŃéÖŠ£¬ÄÜÖ¤Ć÷“×ĖįĖįŠŌ±ČŃĪĖįĖįŠŌČõµÄŹĒ £®
A.½«µČĢå»ż”¢pH=4µÄŃĪĖįŗĶ“×ĖįĻ”ŹĶ³ÉpH=5µÄČÜŅŗ£¬²āĮæĖłŠč¼ÓČėĖ®ĮæµÄ¶ąÉŁ
B.ĻņµČĢå»ż”¢µČpHµÄŃĪĖįŗĶ“×ĖįÖŠ·Ö±š¼ÓČėĶ¬ĮæµÄĻąÓ¦ÄĘŃĪ¹ĢĢ壬²āČÜŅŗµÄpHÓŠĪŽ±ä»Æ
C.ĻņµČĢå»ż”¢µČÅØ¶ČµÄŃĪĖįŗĶ“×Ėį·Ö±š¼ÓČė×ćĮæŠæ·Ū£¬²āĮæ²śÉśĒāĘųµÄĢå»ż
D.ÓƵČĢå»ż”¢µČÅØ¶ČµÄŃĪĖįŗĶ“×Ėį×öµ¼µēŠŌŹµŃ飬øł¾ŻµĘÅŻµÄĆ÷ĮĮ³Ģ¶Č£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĆęĢįµ½µÄĪŹĢāÖŠ£¬ÓėŃĪµÄĖ®½āÓŠ¹ŲµÄŹĒ£Ø £©
¢ŁĆ÷·ÆŗĶFeCl3æÉ×÷¾»Ė®¼Į
¢ŚĪŖ±£“ęFeCl3ČÜŅŗ£¬ŅŖŌŚČÜŅŗÖŠ¼ÓÉŁĮæŃĪĖį
¢ŪŹµŃéŹŅÅäÖĘAlCl3ČÜŅŗŹ±£¬Ó¦ĻČ°ŃĖüČܽāŌŚŃĪĖįÖŠ£¬¶ųŗó¼ÓĖ®Ļ”ŹĶ
¢ÜNH4ClČÜŅŗæÉ×÷ŗø½ÓÖŠµÄ³żŠā¼Į
¢ŻŹµŃéŹŅŹ¢·ÅNa2SiO3ČÜŅŗµÄŹŌ¼ĮĘæÓ¦ÓĆĻšĘ¤Čū£¬¶ų²»ÄÜÓĆ²£Į§Čū
¢ŽÓĆNaHCO3ÓėAl2£ØSO4£©3Į½ÖÖČÜŅŗæÉ×÷ÅŻÄĆš»š¼Į
¢ßŌŚNH4Cl»ņAlCl3ČÜŅŗÖŠ¼ÓČė½šŹōĆ¾»įÉś³ÉĒāĘų
¢ą²ŻÄ¾»ŅÓėļ§Ģ¬µŖ·Ź²»ÄÜ»ģŗĻŹ©ÓĆ
¢į¼ÓČČÕōøÉAlCl3ČÜŅŗµĆµ½Al£ØOH£©3¹ĢĢ壮
A. ¢Ł¢Ü¢ß B. ¢Ś¢Ż¢ą C. ¢Ū¢Ž¢į D. Č«²æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČĖĆĒÓ¦ÓĆŌµē³ŲŌĄķÖĘ×÷ĮĖ¶ąÖÖµē³Ų£¬ŅŌĀś×ć²»Ķ¬µÄŠčŅŖ”£ŅŌĻĀĆ抔ĢāÖŠµÄµē³Ų¹ć·ŗŹ¹ÓĆÓŚČÕ³£Éś»ī”¢Éś²śŗĶæĘѧ¼¼ŹõµČ·½Ćę£¬Ēėøł¾ŻĢāÖŠĢį¹©µÄŠÅĻ¢£¬ĢīŠ“æÕøń”£
£Ø1£©Ē¦Šīµē³ŲŌŚ·ÅµēŹ±·¢ÉśµÄµē³Ų·“Ó¦Ź½ĪŖ£ŗPb£«PbO2£«2H2SO4===2PbSO4£«2H2O”£øŗ¼«µē¼«·“Ó¦Ź½ĪŖ___________________________________________”£
£Ø2£©FeCl3ČÜŅŗ³£ÓĆÓŚøÆŹ“Ó”Ė¢µēĀ·Ķ°å£¬·¢Éś2FeCl3£«Cu===2FeCl2£«CuCl2£¬Čō½«“Ė·“Ó¦Éč¼Ę³ÉŌµē³Ų£¬Ōņøŗ¼«ĖłÓƵē¼«²ÄĮĻĪŖ________£¬µ±ĻßĀ·ÖŠ×ŖŅĘ0.2 molµē×ÓŹ±£¬Ōņ±»øÆŹ“ĶµÄÖŹĮæĪŖ________g”£
£Ø3£©Č¼ĮĻµē³ŲŹĒŅ»ÖÖøߊ§”¢»·¾³ÓŃŗĆµÄ¹©µē×°ÖĆ£¬ŅŌ¼×“¼×öČ¼ĮĻµÄµē³Ų£¬ČēĻĀĶ¼ĖłŹ¾£¬

¢Łøŗ¼«·“Ó¦ĪļŹĒ______________£¬H+“Ó________¼«µ½________¼«£ØĢīa»ņb£©”£
¢ŚÕż¼«·“Ó¦Ź½ĪŖ_________________£¬øŗ¼«·“Ó¦Ź½ĪŖ___________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄė×ÓRO3n-ÖŠ¹²ÓŠxøöŗĖĶāµē×Ó£¬RŌ×ÓµÄÖŹĮæŹżĪŖA£¬ŌņRŌ×ÓŗĖÄŚŗ¬ÖŠ×ӵďżÄæ£Ø £©
A.A+n+48+xB.A+n-24-xC.A-n+24-xD.A+n+24-x
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠÖ÷ŅŖ³É·Ö²»ŹĒ¶žŃõ»Æ¹čµÄŹĒ
A.Āźč§B.Ė®¾§C.¹č½ŗD.¹čŹÆ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com