
| 0.85cV |
| 10.00mL×ρg/mL |
| 0.085cV |
| ρ |
| 0.085cV |
| ρ |


科目:高中化学 来源: 题型:
 甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去),下列各组物质中不能按图示关系转化的是( )
甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去),下列各组物质中不能按图示关系转化的是( )| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | NaOH | NaHSO3 | Na2SO3 | SO2 |
| B | AlCl3 | NaAlO2 | Al(OH)3 | NaOH |
| C | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 |
| D | C | CO | CO2 | O2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、烧碱的量不足 |
| B、乙醛的量不足 |
| C、硫酸铜的量不足 |
| D、加热时间短 |
查看答案和解析>>
科目:高中化学 来源: 题型:
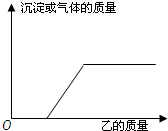 向下表中的甲物质中逐滴加入乙物质至过量,反应生成气体或沉淀的质量与加入的乙的质量关系符合如图所示曲线描述的是( )
向下表中的甲物质中逐滴加入乙物质至过量,反应生成气体或沉淀的质量与加入的乙的质量关系符合如图所示曲线描述的是( )| 序号 | 甲 | 乙 |
| A | 二氧化锰 | 过氧化氢溶液 |
| B | 氢氧化钠和碳酸钠混合溶液 | 稀盐酸 |
| C | 氯化钠和氢氧化钙的混合溶液 | 碳酸钠溶液 |
| D | 氯化铁和氯化铜溶液 | 氢氧化钠溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CSO的电子式: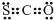 | ||
B、甲烷分子的球棍模型: | ||
C、原子核内有20个中子的氯原子:
| ||
| D、HCO3-的水解方程式为:HCO3-+H2O?CO32-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Cl-的结构示意图: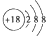 |
B、羟基的电子式: |
| C、过氧化钠、烧碱、纯碱分别属于碱性氧化物、碱、盐 |
| D、Cu、Al、Na可以分别用热还原法、热分解法和电解冶炼 |
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省宿迁市五校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列各组物质中分子数一定相同的是
A.2 g O3和2g O2
B.9g H2O和0.5NA个CO2
C.标准状况下1 mol O2和22.4 L H2O
D.0.2 mol H2和4.48 L HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com