
按照下列元素基态原子的电子排布特征判断元素,并回答问题:A原子中只有一个电子层且只含有一个电子;B原子的3p轨道上得到一个电子后不能再容纳外来电子;C原子的2p轨道上有一个电子的自旋方向与2p轨道上其他电子的自旋方向相反;D原子的第三电子层上有8个电子,第四层上只有1个电子;E原子的价电子排布式为3s23p6。
(1)A~E分别是哪种元素(用元素符号填空):
A:__________;B:________;C:__________;D:________;E:________。
(2)E的原子结构示意图________________。
(3)C的轨道表示式____________________。
(4)B原子的核外电子排布式________________。
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:填空题
下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
(1)在这10种元素中,非金属性最强的是 (填序号);
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为 ,元素②与⑨形成的18e-化合物的电子式 ;
(3)②⑨⑩三种元素形成的化合物M中原子个数比为3:4:2,电子总数为42,M中含有的化学键类型有 ;
(4)比较元素⑦⑧形成的气态氢化物的稳定性: > (用化学式表示)
(5)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式 。
(6)元素④和③形成的化合物属于 化合物,用电子式表示其形成过程 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是 。
(2)已知某粒子的结构示意图为: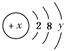 ,试回答:
,试回答:
①当x-y=10时,该粒子为 (填“原子”“阳离子”或“阴离子”)。
②当y=8时,粒子可能为(填名称) 、 、 、 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
光伏并网发电并使用半导体(LED)照明可以节约大量能源。已知发出白光的LED是由氮化镓(GaN)芯片和钇铝石榴石(YAG,化学式:Y3Al5O12)芯片封装在一起做成的,如图所示。
(1)砷与氮位于同主族,砷化镓也是半导体材料,它的化学式为________。
(2)用简单氧化物形式表示YAG的组成:________。
(3)下列有关光伏并网发电的叙述正确的是________(填序号)。
①LED是新型无机高分子材料
②电流从a流向b
③光伏电池是将太阳能直接转化为电能
④图中N型半导体为正极,P型半导体为负极
⑤如果工业上用光伏电池并网发电精炼粗铜,a极连接精铜电极
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
根据下列五种元素的电离能数据(单位:kJ·mol-1),回答下面问题。
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2 080 | 4 000 | 6 100 | 9 400 |
| R | 500 | 4 600 | 6 900 | 9 500 |
| S | 740 | 1 500 | 7 700 | 10 500 |
| T | 580 | 1 800 | 2 700 | 11 600 |
| U | 420 | 3 100 | 4 400 | 5 900 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 | A | B | C | D |
| 性质结构信息 | 原子中最外层电子数为电子层数的2倍。常温下为淡黄色固体,其燃烧热为Q KJ/mol | 单质常温、常压下是气体,能溶于水。原子的M层p轨道有1个未成对的电子 | 单质质软、银白色固体、导电性强。单质在空气中燃烧发出黄色的火焰。 | 原子最外层电子层上s电子数等于p电子数。单质是一种重要的半导体材料。 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D是常见的短周期元素,根据有关信息,按要求回答问题:
信息①:A、B、C、D原子序数依次增大,且原子核外最外层电子数均不少于2;
(1)根据信息①:A一定不是 (填序号);
A.氢 B. 碳 C.氧 D.硫
信息②:上述四种元素的单质常温下均为固体,其最高价氧化物中有两种能溶于稀硫酸,三种能溶于浓氢氧化钠溶液;
(2)这四种元素中是否可能有一种是铝元素 (填“可能”或“不可能”);
信息③:A与D同主族,工业上常用A高温下还原DO2制取D;
(3)A与DO2反应的化学方程式为 ;
信息④:向上述四种元素的单质组成的混合物中加入足量盐酸溶液,固体部分溶解,过滤后向滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀;
(4)白色沉淀物的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是________。
(2)已知某粒子的结构示意图为
试回答:
①当x-y=10时,该粒子为________(填“原子”、“阳离子”或“阴离子”)。
②当y=8时,粒子可能为(填名称)________、________、________、________、________。
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在1961年,本生和基尔霍夫发现了一种新的碱金属元素,根据已学知道解答下列问题,帮助这两位科学家研究该元素。
(1)该元素单质的密度比水的密度大,则该元素可能是_______________________________。
(2)该元素的单质与水反应比钾与水反应剧烈,但没有铯与水反应剧烈,由此可确定该元素是________。其确定依据是_____________________________________________________。
(3)人类制备出该元素的单质比钠单质要晚得多,分析其中的原因:__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com