
分析 ①向一份溶液中加入过量NaOH溶液,产生沉淀,其物质的量为0.3mol,可知氢氧化镁为0.3mol,则含Mg2+为0.3mol,原溶液中一定不能存在CO32-;
②向另一份溶液中加入过量的BaCl2溶液,产生沉淀,其物质的量为0.2mol,可知生成硫酸钡为0.2mol,则一定含SO42-为0.2mol,原溶液中不存在Ba2+,结合电荷守恒来解答.
解答 解:(1)实验①说明溶液中含有Mg2+,没有CO32-,理由是生成沉淀为氢氧化镁,镁离子和碳酸根离子不能共存,
故答案为:Mg2+;CO32-;沉淀为氢氧化镁,镁离子和碳酸根离子不能共存;
(2)实验②说明溶液中含有SO42-,没有Ba2+,理由是由生成沉淀为硫酸钡可知原溶液含硫酸根离子,但硫酸根离子与钡离子不能共存,
故答案为:SO42-;Ba2+;生成沉淀为硫酸钡可知原溶液含硫酸根离子,但硫酸根离子与钡离子不能共存;
(3)SO42-为0.2mol,Mg2+为0.3mol,则0.2×2<0.3×2,阳离子电荷总数大于阴离子电荷总数,由电荷守恒可知,溶液中存在Cl-,故答案为:阳离子电荷总数大于阴离子电荷总数,由电荷守恒可知,溶液中存在Cl-.
点评 本题考查离子推断,为高频考点,把握离子之间的反应、沉淀的判断为解答的关键,侧重分析与应用能力的考查,注意电荷守恒的应用,题目难度不大.


 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:解答题
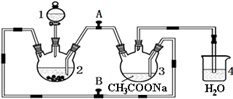 醋酸亚铬水合物[Cr(CH3COO)2]2•2H2O(相对分子质量为376)是一种深红色晶体.不溶于冷水,微溶于乙醇,不溶于乙醚(易挥发的有机溶剂)是常用的氧气吸收剂.实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示,且仪器2中预先加入锌粒.已知二价铬不稳定,极易被氧气氧化,不与锌反应.制备过程中发生的相关反应如下:
醋酸亚铬水合物[Cr(CH3COO)2]2•2H2O(相对分子质量为376)是一种深红色晶体.不溶于冷水,微溶于乙醇,不溶于乙醚(易挥发的有机溶剂)是常用的氧气吸收剂.实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示,且仪器2中预先加入锌粒.已知二价铬不稳定,极易被氧气氧化,不与锌反应.制备过程中发生的相关反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
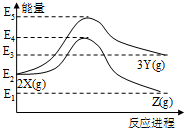
| A. | 由X→Y反应的△H=E5-E2 | |
| B. | 由X→Z反应的△H>0 | |
| C. | 由图可知等物质的量的Y的能量一定比X的能量高 | |
| D. | 升高温度可提高X→Z的反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化钠的电子式: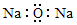 | |
| B. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子的结构示意图: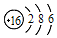 | |
| D. | CCl4的球棍模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 化学平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| A. | 该反应为吸热反应 | |
| B. | 该反应的化学平衡常数表达式为K=$\frac{c(C)•c(D)}{c(A)•c(B)}$ | |
| C. | 其他条件不变时,增大体系的压强,化学平衡常数减小 | |
| D. | 单位时间内生成B和D的物质的量相等时,该反应处于平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该温度下的平衡常数是:K=$\frac{9}{16}$ | |
| B. | 达到平衡时,NO的转化率是60% | |
| C. | 3min末达到平衡,则v(NO)=0.01mol/(L•min) | |
| D. | 升高温度有利于活性炭处理更多的污染物NO |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com